Clear Sky Science · nl
Een ensemble-machine-learningclassificator voor de diagnose van de ziekte van Parkinson met behulp van optische coherentie tomografie-angiografie
Waarom de ogen verborgen hersenziekte kunnen onthullen
De ziekte van Parkinson wordt meestal pas gediagnosticeerd nadat tremoren, stijfheid of vertraagde bewegingen optreden—symptomen die aangeven dat de hersenen al jarenlang veranderen. Deze studie onderzoekt een onverwachte snelweg: het bekijken van kleine bloedvaten achter in het oog met een pijnloze beeldvorming en vervolgens het gebruik van kunstmatige intelligentie om mensen te signaleren die mogelijk eerder en objectiever Parkinson hebben dan met de huidige controles mogelijk is.
De hersenen bekijken via het oog
Het lichtgevoelige weefsel achter in het oog, het netvlies, is in feite een toegankelijke deel van de hersenen. Het deelt vergelijkbare zenuwen en bloedvaten en kan niet-invasief in een poliklinische setting worden onderzocht. De onderzoekers gebruikten een technologie genaamd optische coherentie-tomografie-angiografie, of OCTA, die gedetailleerde, kleurstofvrije kaarten van de retinale circulatie oplevert. Omdat Parkinson in verband is gebracht met problemen in kleine bloedvaten elders in het lichaam, vroegen de onderzoekers zich af of subtiele veranderingen in deze retinale netwerken als een “venster” naar vroegtijdige ziekte zouden kunnen fungeren.
Oogscans omzetten in cijfers
In een retrospectieve studie verzamelde het team OCTA-scans van 53 mensen met Parkinson en 39 gezonde, leeftijdsgematchte vrijwilligers. Ze concentreerden zich op twee lagen van retinale vaten: een oppervlakkige laag dicht bij het oppervlak en een diepere laag daaronder. Van elke laag segmenteerden ze automatisch de centrale foveale avasculaire zone—de kleine vaatvrije put die nodig is voor scherp zicht—en de omringende capillairen. Vervolgens zetten ze elke afbeelding om in 22 numerieke metingen. Sommige beschreven de vorm van de foveale zone, zoals hoe rond, glad of onregelmatig de rand was. Andere vingen de algehele dichtheid van de bloedvaten en die in een ring rond de fovea. Samen kwantificeerden deze metingen de microvasculaire gezondheid met veel meer nuance dan het menselijk oog kan beoordelen. 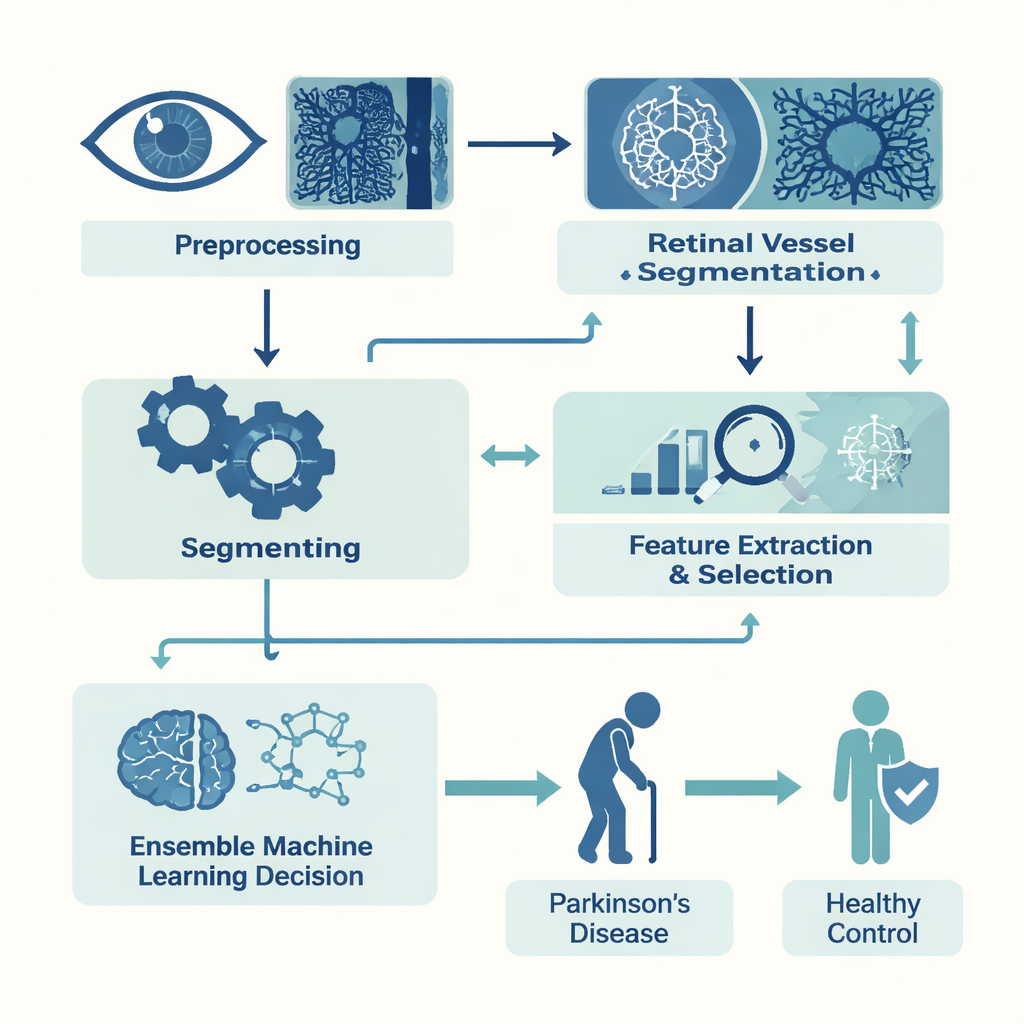
Een AI trainen om patronen van Parkinson te herkennen
Met deze metingen in handen bouwden de onderzoekers computermodellen om Parkinson-scans te onderscheiden van gezonde scans. Omdat hun dataset bescheiden was, gebruikten ze eerst feature-selectietechnieken om de 22 metingen terug te brengen tot de meest informatieve subset, waarmee ruis en overfitting werden verminderd. Daarna trainden ze verschillende gangbare machine-learningalgoritmen, waaronder beslissingsboomgebaseerde methoden en een k-nearest neighbors-classificator. Tot slot combineerden ze de drie sterkste presteerders—XGBoost, Random Forest en K-Nearest Neighbors—in een gewogen "ensemble", zodat ieders stem in verhouding telde tot de verwachte prestatie.
Wat de modellen in het netvlies vonden
Vergeleken met gezonde vrijwilligers toonden mensen met Parkinson duidelijke tekenen van veranderde retinale microcirculatie. Maten voor vatendichtheid waren lager, en de centrale foveale zone neigde naar minder regelmatige vormen—minder rond, minder glad en minder compact—zowel in de oppervlakkige als in de diepe vaatlagen. Bij tests op eerder ongeziene gegevens classificeerde het ensemblemodel ongeveer drie van de vier ogen correct. Het opmerkelijkste was dat het een sensitiviteit van 90% bereikte: het identificeerde negen van de tien Parkinson-gevallen correct. De specificiteit was wat bescheidener, net iets boven de helft, wat betekent dat sommige gezonde personen ten onrechte als ziek werden aangemerkt. De area under the receiver operating characteristic curve, een gebruikelijke samenvatting van diagnostische prestaties, was 0,75, wat wijst op nuttige maar niet definitieve discriminatie. 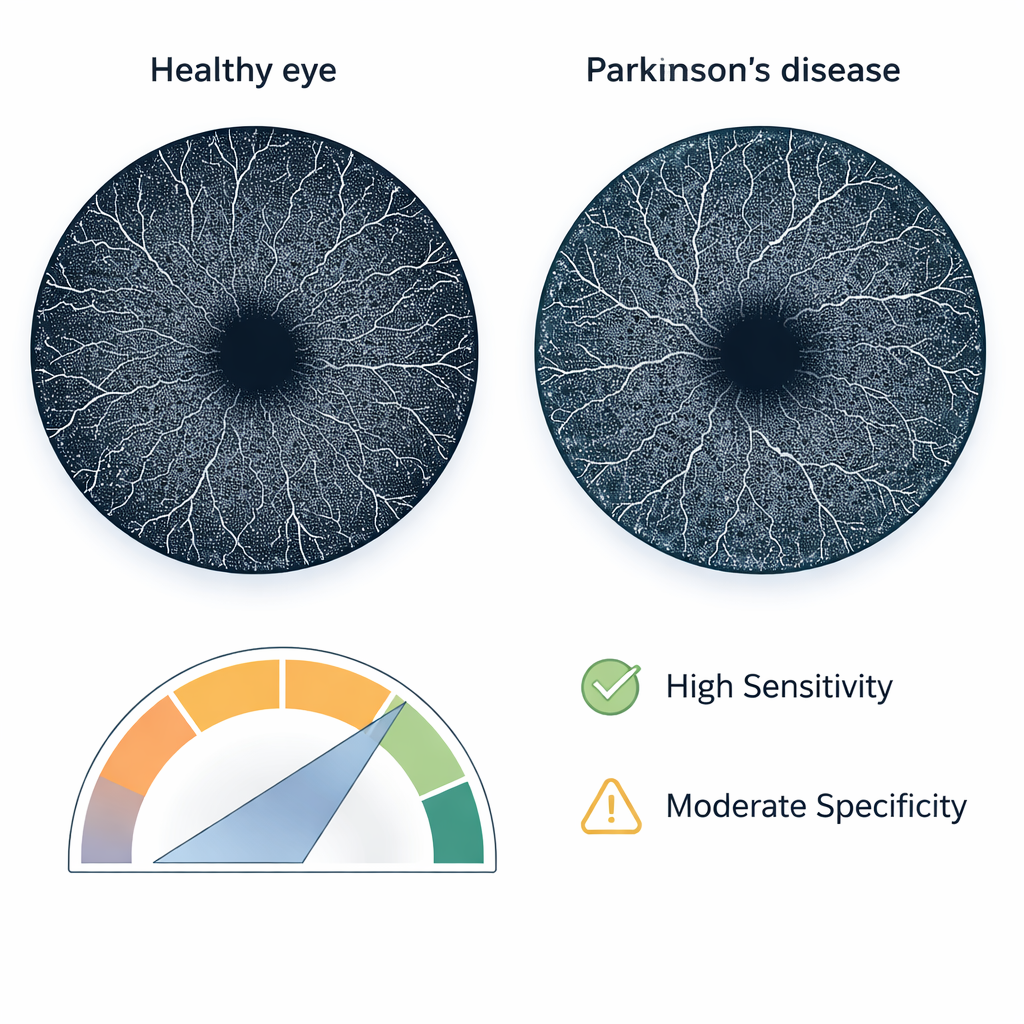
Van algoritme naar kliniek
Om verder te komen dan theorie verpakte het team hun methode in een prototype-softwaretool genaamd Parkinson’s Disease Artificial Intelligence (PDAI). Via een eenvoudige grafische interface kunnen clinici OCTA-scans laden, de automatisch getraceerde bloedvaten en de centrale foveale zone bekijken, de belangrijkste numerieke kenmerken zien en direct een voorspelling krijgen of een scan lijkt op die van Parkinson-patiënten. Omdat het systeem leunt op handgemaakte, duidelijk gedefinieerde metingen in plaats van een ondoorzichtige "black box", zijn de bijdragers aan elke beslissing makkelijker voor clinici te interpreteren en mogelijk te relateren aan onderliggende biologie.
Wat dit betekent voor patiënten
Dit werk biedt nog geen op zichzelf staande test voor Parkinson, maar het laat zien dat een snelle, niet-invasieve oogscan, geanalyseerd met zorgvuldig ontworpen machine-learningmethoden, ziektegerelateerde veranderingen met hoge sensitiviteit kan detecteren. In de praktijk zou zo’n hulpmiddel op den duur als screeningsinstrument kunnen dienen—het zou oogartsen en neurologen kunnen helpen te beslissen wie dichter gemonitord of doorverwezen moet worden voor nadere evaluatie, lang voordat invaliderende symptomen optreden. Grotere, multicentrische studies zijn nog nodig, maar de studie suggereert dat de ogen inderdaad een praktisch vroegwaarschuwingssignaal voor de ziekte van Parkinson kunnen leveren.
Bronvermelding: Hasanshahi, M., Mehdizadeh, A., Mahmoudi, T. et al. An ensemble machine learning classifier for Parkinson’s disease diagnosis using optical coherence tomography angiography. Sci Rep 16, 7297 (2026). https://doi.org/10.1038/s41598-026-38407-9
Trefwoorden: Ziekte van Parkinson, retinale beeldvorming, OCTA, machine learning, vroegtijdige diagnose