Clear Sky Science · nl
Prognostisch model op basis van machine learning voor stamheid- en angiogenese-gerelateerde genen om prognose en immuuninfiltratie bij patiënten met HCC te voorspellen
Waarom dit onderzoek belangrijk is voor patiënten met leverkanker
Hepatocellulair carcinoom, de meest voorkomende vorm van leverkanker, komt vaak terug of zaait uit, zelfs na behandeling. Deze studie onderzoekt waarom dat gebeurt en hoe artsen beter kunnen voorspellen welke patiënten het grootste risico lopen. Door grote genetische datasets te combineren met moderne machine‑learning bouwden de onderzoekers een instrument dat twee krachtige kankereigenschappen verbindt — “stamheid” (cellen die zich als hardnekkige zaadjes gedragen) en de aanmaak van nieuwe bloedvaten — met de overlevingskansen van patiënten en hun waarschijnlijke reactie op immuuntherapieën.
Kanker-„zaadcellen” en nieuwe bloedvaten
Veel tumoren bevatten een kleine groep cellen die zich als zaadjes gedragen. Deze kankerstamcellen kunnen zichzelf vernieuwen, zijn bestand tegen behandeling en kunnen de tumor opnieuw opstarten na chirurgie of chemotherapie. Tegelijkertijd moeten tumoren nieuwe bloedvaten vormen om zuurstof en voedingsstoffen aan te voeren zodat ze kunnen groeien en uitzaaien. Recente studies tonen aan dat deze twee processen met elkaar verweven zijn: stamachtige kankercellen geven signalen af die de bloedvatgroei stimuleren, terwijl een vaatrijke omgeving die zaadcellen helpt te overleven. Het begrijpen en gezamenlijk aanpakken van deze samenwerking is bijzonder belangrijk bij leverkanker, die zowel sterk gevasculariseerd is als gevoelig voor recidief.
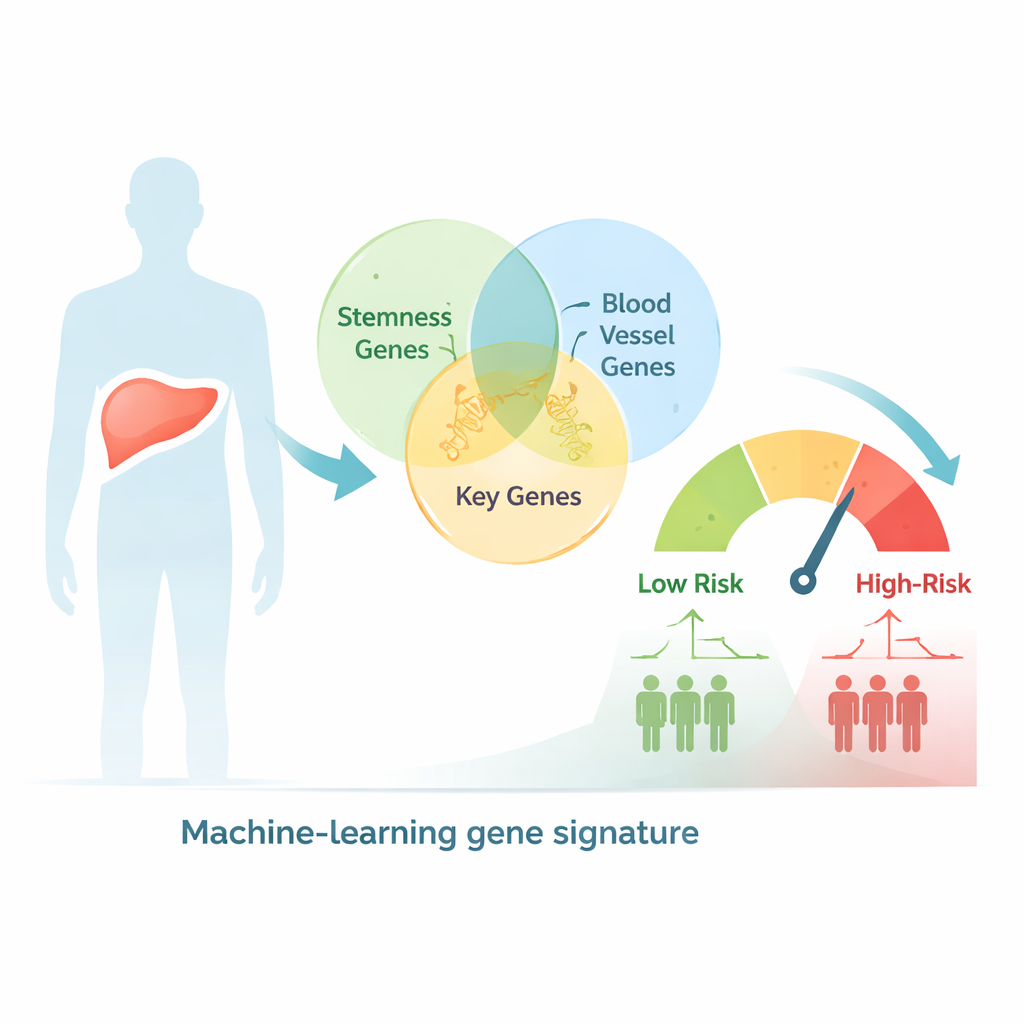
Grote datasets gebruiken om patiënten naar risico te sorteren
De onderzoekers begonnen met het doorzoeken van een grote menselijke genendatabase op genen die zowel met stamachtig gedrag als met bloedvatvorming geassocieerd zijn, wat leidde tot meer dan 2.600 overlappende kandidaatgenen. Vervolgens onderzochten ze leverkankermonsters van honderden patiënten waarvan de tumor-genactiviteit en klinische uitkomsten in openbare kankerdatabases waren vastgelegd. Met statistische tests en clusteranalyse groepeerden ze patiënten in twee genetische subtypes die duidelijke verschillen lieten zien in stadium, tumorgrootte en overleving, wat suggereert dat gecombineerde stamheid- en vaat-gerelateerde signalen zinvolle biologische informatie in deze ziekte vangen.
Opbouw van een risico‑score op basis van negen genen
Uit deze grote genpool gebruikte het team een machine‑learningbenadering om terug te brengen tot slechts negen sleutelgenen waarvan de gecombineerde activiteit het beste voorspelde hoe lang patiënten leefden. Deze negen genen werden gebruikt om voor iedere persoon een risico‑score te berekenen. Patiënten met een hoge score hadden een significant kortere totale overleving, zowel in de originele dataset als in een onafhankelijke groep leverkankerpatiënten die voor validatie werd gebruikt. De nauwkeurigheid van het model concurreerde met of was beter dan veel bestaande instrumenten, en wanneer de score werd gecombineerd met eenvoudige klinische informatie zoals tumorstadium in een nomogram, verbeterde de voorspelling van 1-, 3- en 5‑jaars overleving verder.
Verbanden met het immuunsysteem en behandelrespons
Het team onderzocht ook wat de negen‑genenscore onthulde over de immuunomgeving van de tumor. Laag‑risico tumoren waren geneigd meer “geïnflameerd” te zijn, met hogere niveaus van verschillende immuuncellen en sterkere signalen van aanvalspaden. Hoog‑risico tumoren vertoonden daarentegen patronen die overeenkomen met immuunevasiemechanismen en hogere mutatiesnelheden in belangrijke genen zoals TP53. Met gevestigde computationele hulpmiddelen die inschatten hoe tumoren kunnen reageren op moderne immuuntherapieën, suggereerde de studie dat laag‑risico patiënten mogelijk beter reageren op immuuncheckpointblokkers dan hoog‑risico patiënten. Hoewel deze voorspellingen nog in echte behandelomstandigheden moeten worden getest, wijzen ze op een praktische manier om patiënten te identificeren die het meest van dergelijke middelen zouden kunnen profiteren.
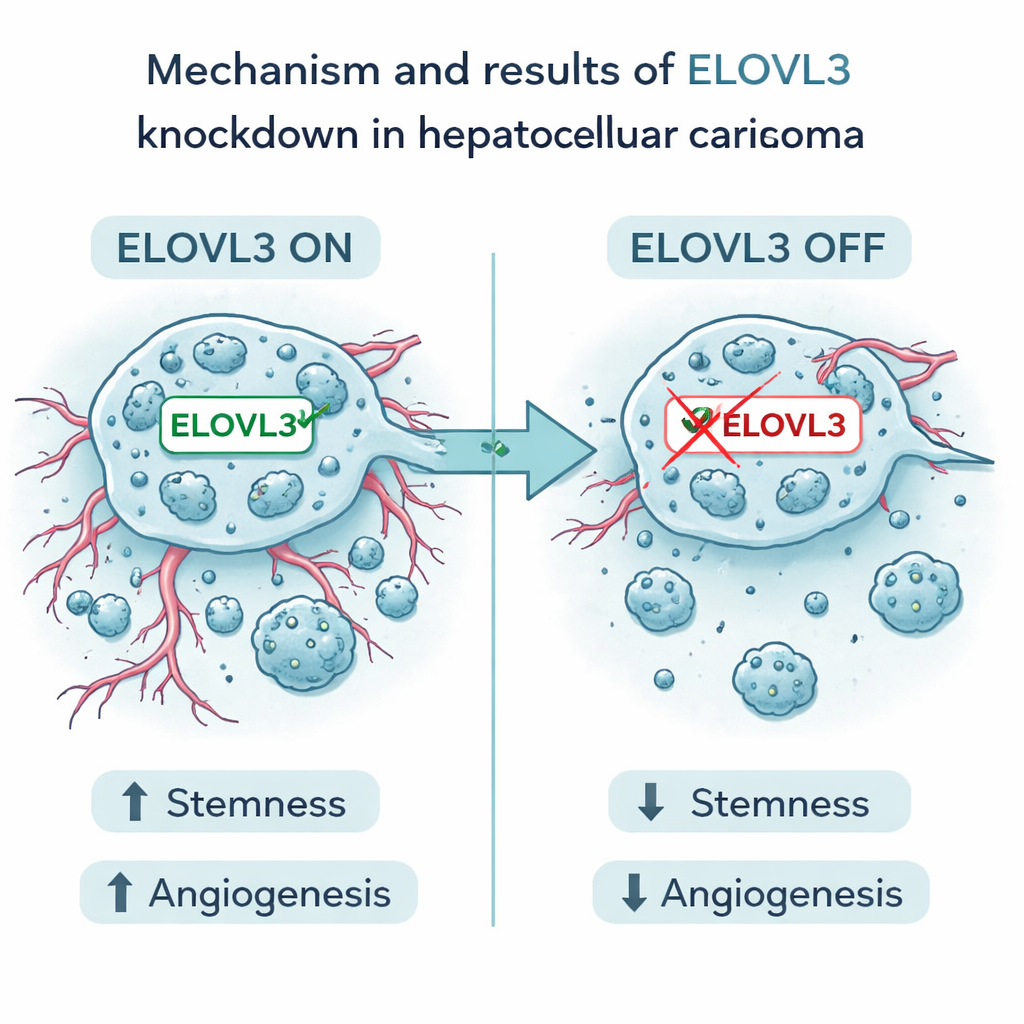
Inzoomen op één veelbelovend doelwit
Onder de negen genen viel eentje op: ELOVL3. Hoge expressie van dit gen was gekoppeld aan slechtere overleving. In laboratoriumexperimenten verminderden de auteurs ELOVL3 in menselijke leverkankercellen. Dit maakte de cellen minder goed in staat stamachtige klonten te vormen en verlaagde de niveaus van bekende stamheidmarkers. Ook verminderde het de productie en afgifte van twee belangrijke vaatbevorderende factoren, VEGFA en FGF2. De kankercellen groeiden, migreerden en invadeerden minder, en in muismodellen waren tumoren met verminderde ELOVL3 kleiner en vertoonden ze minder kenmerken van agressieve ziekte. Deze bevindingen ondersteunen het idee dat ELOVL3 zowel het zaadachtige gedrag van leverkankercellen als hun vermogen om ondersteunende bloedvaten te vormen, voedt.
Wat dit kan betekenen voor toekomstige zorg
In eenvoudige bewoordingen levert dit werk twee hoofdboodschappen. Ten eerste kan een eenvoudige negen‑genen score, afgeleid van tumormonsters, leverkankerpatiënten in hogere en lagere risicogroepen indelen en een aanwijzing geven voor hun mogelijke reactie op immuungebaseerde behandelingen. Ten tweede lijkt één van de genen in die score, ELOVL3, op een kruispunt te zitten tussen het regeneratieve vermogen van de kanker en het vermogen om nieuwe bloedvaten te laten groeien, waardoor het een aantrekkelijk doelwit voor toekomstige medicatie is. Hoewel het model en het doelwit bevestiging nodig hebben in prospectieve klinische onderzoeken, openen ze de deur naar meer gepersonaliseerde zorg bij leverkanker en naar combinatiestrategieën die zowel kankerstamcellen als hun bloedtoevoer blokkeren.
Bronvermelding: Cheng, F., Shi, Y., Gao, X. et al. Machine learning-based prognostic model of stemness and angiogenesis-related genes for predicting prognosis and immune infiltration in patients with HCC. Sci Rep 16, 7271 (2026). https://doi.org/10.1038/s41598-026-38379-w
Trefwoorden: hepatocellulair carcinoom, kankerstamcellen, angiogenese, prognostisch genhandtekening, ELOVL3