Clear Sky Science · nl
Variabiliteit van referentiegenen over leeftijd en geslacht in 5XFAD-muizen benadrukt normalisatie-uitdagingen in Alzheimer‑modellen
Waarom deze muizenstudie van belang is voor Alzheimer-onderzoek
Wanneer wetenschappers zoeken naar vroege waarschuwingssignalen of behandelingseffecten bij de ziekte van Alzheimer, meten ze vaak in hoeverre verschillende genen in de hersenen aan- of uitgezet zijn. Om te bepalen of een gen echt veranderd is, hebben ze echter eerst een betrouwbare "maatstaf" nodig: referentiegenen die geacht worden constant te blijven. Dit artikel laat zien dat, in een snel voortschrijdend muismodel van Alzheimer, die zogenaamd constante genen veel minder stabiel zijn dan veel onderzoekers aannemen — vooral tussen verschillende leeftijden, hersengebieden en tussen mannetjes en vrouwtjes.
Hoe wetenschappers de genetische activiteit van de hersenen lezen
Modern hersenonderzoek vertrouwt vaak op een techniek genaamd RT-qPCR, die telt hoeveel van het boodschapper-RNA van een bepaald gen aanwezig is in een weefselmonster. Omdat monsters nooit exact dezelfde totale hoeveelheid materiaal bevatten, normaliseren onderzoekers hun metingen ten opzichte van een of meer referentiegenen, vaak "huishoudgenen" genoemd, waarvan verwacht wordt dat ze constant zijn onder verschillende condities. In de praktijk veranderen ziekten zoals Alzheimer echter cellulaire samenstelling, stofwisseling en ontsteking in de hersenen drastisch, wat stilletjes de niveaus van deze referentiegenen kan verschuiven. Als de referentie zelf verschuift, kan elke daarop gebaseerde meting misleidend zijn en echte biologische veranderingen over- of onderbelichten.
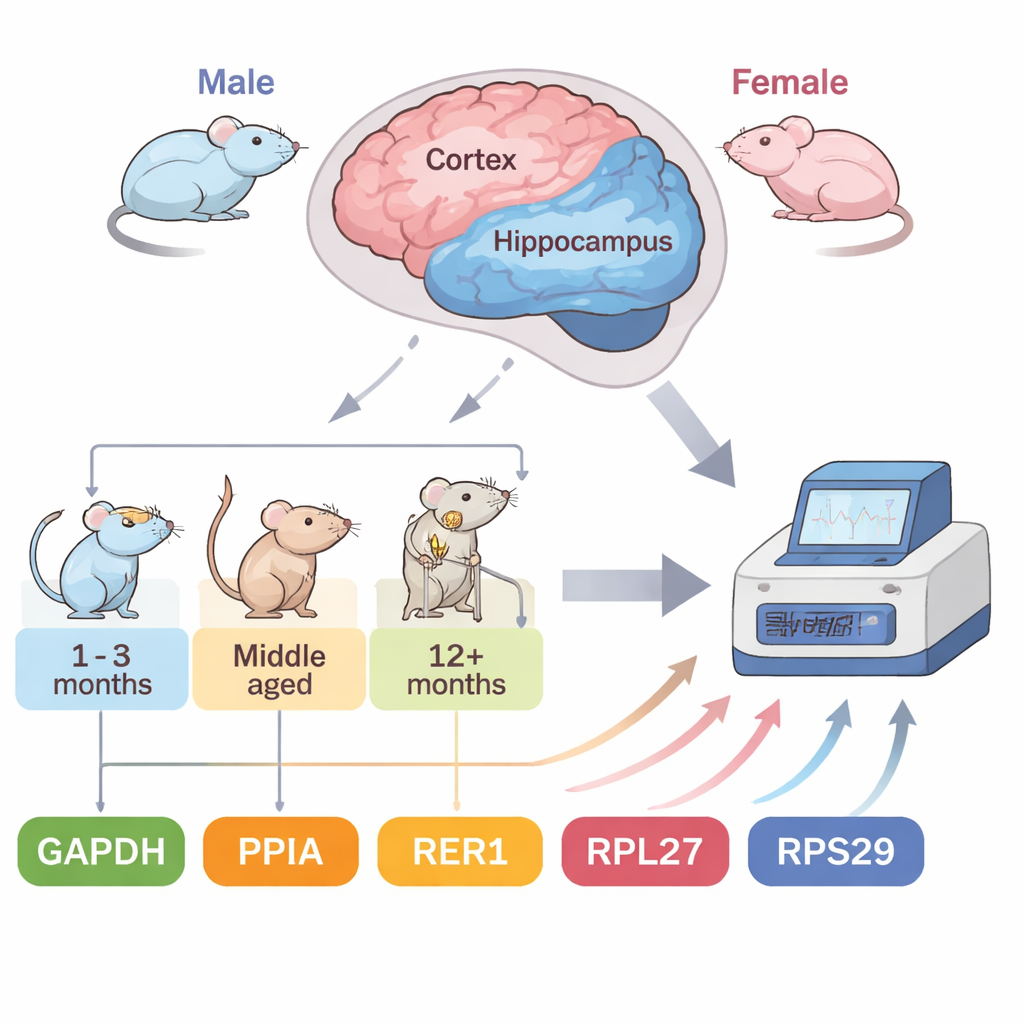
Een snelverlopend muismodel van Alzheimer
Het team richtte zich op 5XFAD-muizen, een veelgebruikt model dat vijf menselijke mutaties draagt die gekoppeld zijn aan familiaire Alzheimer. Deze dieren ontwikkelen amyloïde plaques — eiwitophopingen die kenmerkend zijn voor de aandoening — bijzonder vroeg: rond twee maanden leeftijd, met zware plaque-opbouw rond vier tot vijf maanden. Deze versnelde tijdlijn stelt onderzoekers in staat ziektegerelateerde veranderingen in maanden in plaats van jaren te volgen. De auteurs onderzochten twee kwetsbare hersengebieden, de cortex en de hippocampus, bij zowel mannelijke als vrouwelijke muizen in vier stadia: vroeg (2 maanden), in ontwikkeling (4 maanden) en meer gevorderd (7 en 10 maanden). Ze testten vijf veelgebruikte referentiegenen en gebruikten vier onafhankelijke statistische methoden om te rangschikken hoe stabiel elk gen zich gedroeg onder deze wisselende condities.
Referentiegenen zijn geen universele oplossing
De resultaten tonen aan dat geen enkel gen overal perfect constant bleef. In plaats daarvan hing stabiliteit af van waar in de hersenen het monster vandaan kwam, of de muis mannelijk of vrouwelijk was, en hoe ver de ziekte gevorderd was. Sommige genen, zoals Gapdh — een klassieke werkpaard in veel studies — presteerden relatief goed in meerdere omstandigheden, vooral in de cortex op jongere leeftijden, maar lieten meer variabiliteit zien in latere stadia of in bepaalde hippocampusmonsters. Andere kandidaten, zoals Rps29, Ppia, Rpl27 en Rer1, kwamen naar voren als betere partners in specifieke combinaties, en deze "beste paren" verschilden met leeftijd en geslacht. Over het geheel genomen trok de cortex vaker meer variatie dan de hippocampus, en latere ziektefasen, met name bij mannelijke muizen, verstoorden de veronderstelde stabiliteit van verschillende referentiegenen.
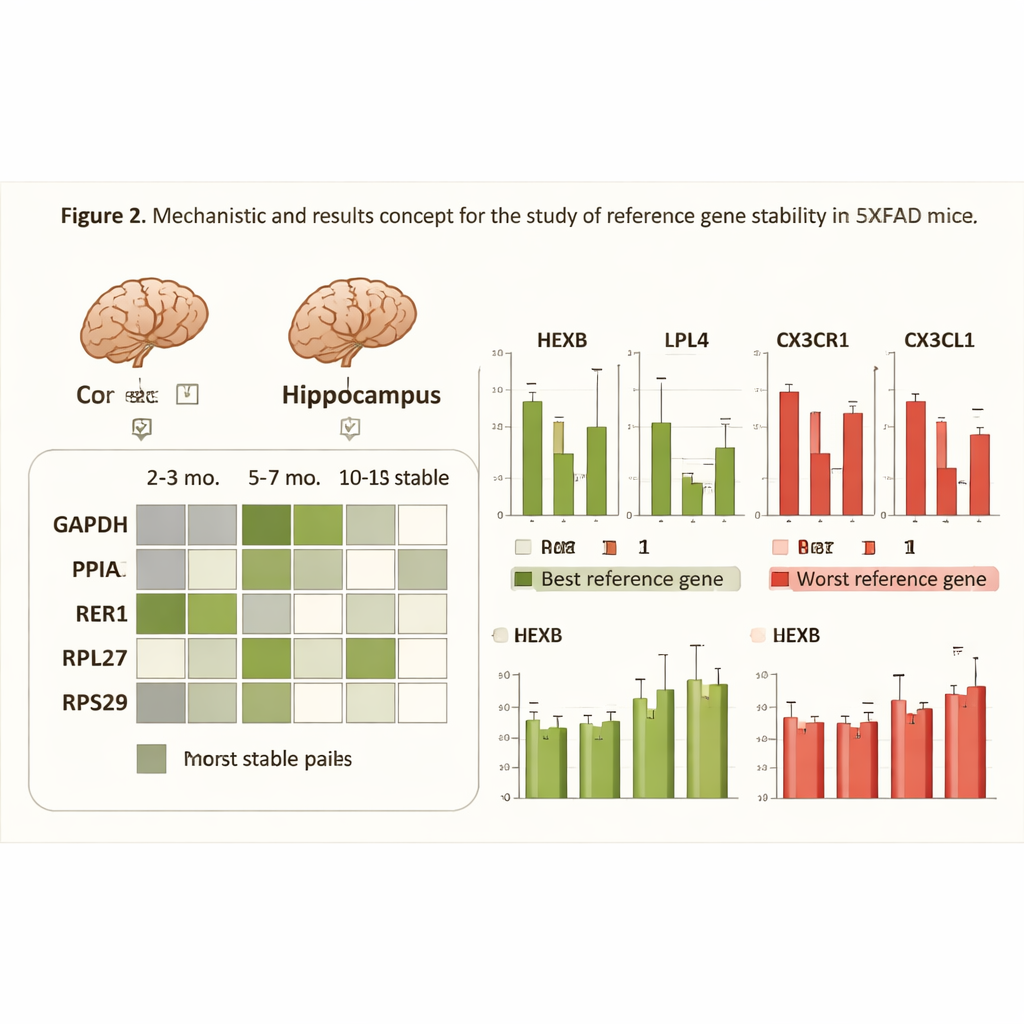
Wat er gebeurt als de maatstaf buigt
Om te demonstreren waarom zorgvuldige keuze van referentiegenen belangrijk is, bekeken de onderzoekers vier hersengenen die betrokken zijn bij ontsteking, stofwisseling en immuunsignalisatie — processen die diep geworteld zijn in Alzheimer. Ze vergeleken hoe de ogenschijnlijke veranderingen in deze doelgenen verschilden wanneer genormaliseerd met óf het meest stabiele referentiepaar, óf het minst stabiele enkele gen, of met alle vijf genen samen. Wanneer zwakke referentiegenen werden gebruikt, werden de gegevens rumoeriger en leken sommige biologisch relevante verschuivingen zwakker of zelfs statistisch niet-significant. Daarentegen verminderde het gebruik van het best passende paar voor elke conditie de spreiding in de metingen en versterkte het de detectie van echte verschillen tussen gezonde en zieke muizen, vooral in de latere stadia van de pathologie.
Heldere signalen voor een complexe ziekte
Voor niet-specialisten is de kernboodschap eenvoudig: zelfs de basale meetlatten die in genstudies worden gebruikt, kunnen vervormen onder de druk van een snel veranderende hersenziekte zoals Alzheimer. Dit werk biedt een praktische leidraad om betere referentiegenen te kiezen in een belangrijk muismodel en benadrukt dat onderzoekers hun "maatstaven" moeten valideren voor elk hersengebied, elke leeftijd en elk geslacht dat ze bestuderen. Daarmee kunnen wetenschappers zuiverdere, betrouwbaardere uitslagen verkrijgen van welke genen werkelijk veranderen tijdens Alzheimer‑achtige degeneratie — een essentiële stap om de mechanismen van de ziekte te begrijpen en potentiële behandelingen te beoordelen.
Bronvermelding: Daini, E., Antonioni, K., Piemontese, M. et al. Reference gene variability across age and sex in 5XFAD mice highlights normalization challenges in Alzheimer’s models. Sci Rep 16, 7302 (2026). https://doi.org/10.1038/s41598-026-38346-5
Trefwoorden: Ziekte van Alzheimer, genexpressie, 5XFAD-muizen, referentiegenen, RT-qPCR