Clear Sky Science · nl
DGCR8 reguleert meerdere processen van transcriptie-gekoppelde nucleotide-excisieherstel
Hoe zonlicht met onze genen spreekt
Elke keer dat we in de zon staan, slaan onzichtbare ultraviolet (UV)-stralen op onze huid en beschadigen het DNA in onze cellen. Meestal herstellen onze cellen die schade stilletjes voordat het problemen veroorzaakt. Deze studie onthult een verrassende speler in dat beschermingssysteem: een eiwit genaamd DGCR8, eerder bekend vanwege zijn rol bij de aanmaak van microRNA’s. De onderzoekers tonen aan dat DGCR8 na UV-blootstelling van taak kan wisselen en verschillende stappen coördineert van een belangrijk DNA-herstelpad dat helpt kanker en andere ziekten te voorkomen.
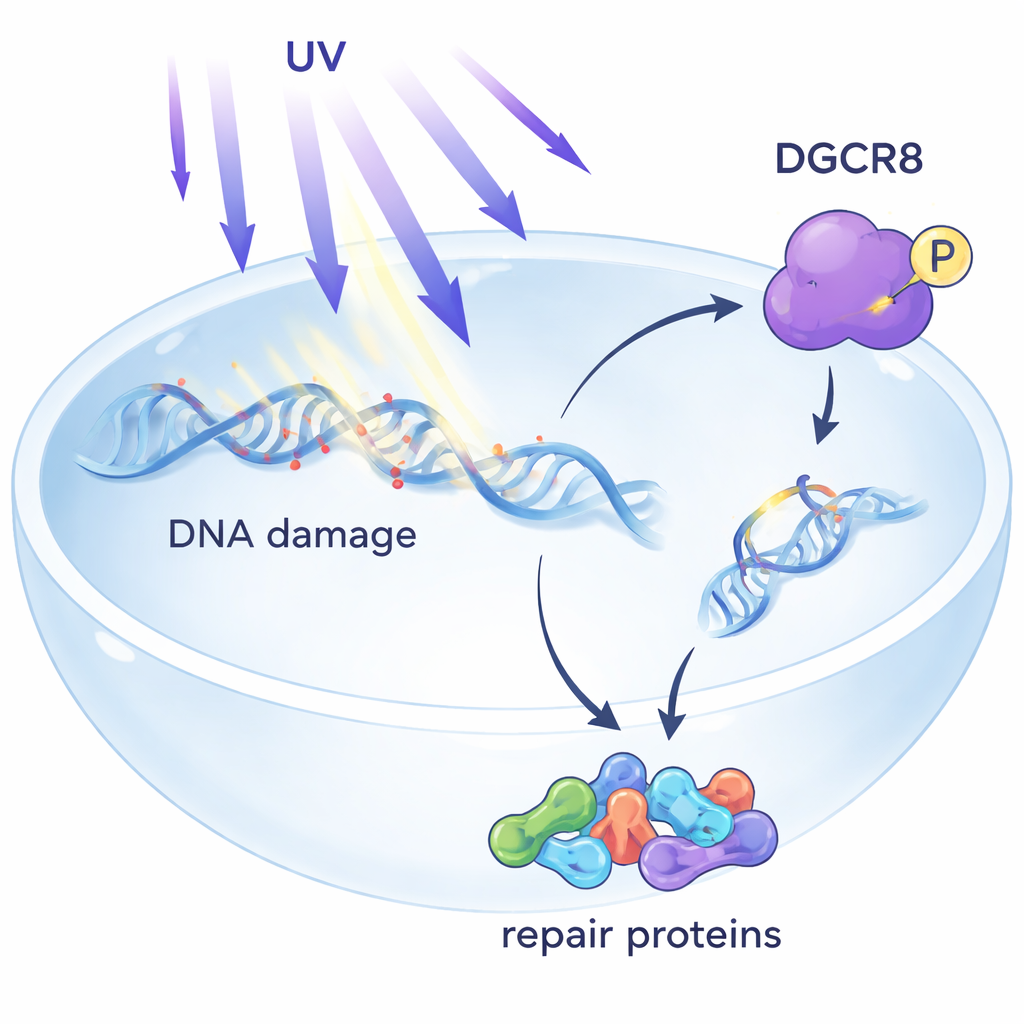
Een verborgen bewaker binnen DNA-herstel
UV-licht veroorzaakt kleine beschadigingen in het DNA die de moleculaire machines die genen aflezen kunnen blokkeren. Een van de belangrijkste verdedigingen van het lichaam is transcriptie-gekoppeld nucleotide-excisieherstel, of TC-NER, dat zich richt op schade die het aflezen van genen stillegt. Tot nu toe stond DGCR8 vooral bekend om zijn rol bij de verwerking van microRNA’s, korte RNA-moleculen die de genactiviteit fijnafstellen. Eerder werk suggereerde al dat DGCR8 cellen beschermt tegen UV, maar hoe dat werkte was onduidelijk. Dit artikel laat zien dat DGCR8 na UV-blootstelling fysiek samenwerkt met centrale TC-NER-factoren en fungeert als organisator die herstelcomponenten samenbrengt precies daar waar het aflezen van genen vastloopt.
Een moleculair aan/uit‑schakelaartje voor DGCR8
De sleutel tot DGCR8’s nieuwe rol is een enkele chemische markering op een van zijn bouwstenen, het aminozuur serine op positie 153. Wanneer deze plaats wordt gefosforyleerd—dat wil zeggen dat er een fosfaatgroep wordt toegevoegd—krijgt DGCR8 het vermogen om te binden aan kernspelers van TC-NER, waaronder RNA-polymerase II (het gen-aflezende enzym) en herstelproteïnen genaamd CSB, CSA en UVSSA. Cellen die ontworpen waren met een versie van DGCR8 die niet op deze plaats gefosforyleerd kan worden (de S153A-mutant) toonden zwakke of afwezige interacties tussen deze herstelproteïnen, en de normale UV-geïnduceerde assemblage van het herstelcomplex faalde. Een “fosfomimetische” variant die zich gedraagt alsof ze altijd gefosforyleerd is, had het tegenovergestelde effect en versterkte sleutelinteracties zelfs zonder UV. Deze resultaten geven aan dat fosforylering op Ser153 fungeert als een aan/uit-schakelaar die DGCR8 omzet van zijn gebruikelijke RNA-verwerkingsrol in een coördinator van DNA-herstel.
Het ontwarren van gevaarlijke DNA–RNA‑knopen
Naast het bijeenbrengen van herstelproteïnen helpt DGCR8 ook bij het beheersen van structuren die R-lussen worden genoemd—korte stukken waarin nieuwgemaakt RNA opnieuw hecht aan het DNA waar het van afkomstig is en zo een DNA–RNA-hybride vormt. In kleine hoeveelheden kunnen R-lussen nuttig zijn, maar wanneer ze zich na UV ophopen kunnen ze de DNA-replicatie blokkeren en chromosomen destabiliseren. Met gespecialiseerde antilichamen en fluorescerende sondes vonden de auteurs dat cellen zonder DGCR8, of met de niet-fosforyleerbare S153A-vorm, veel meer R-lussen opbouwen na UV. Gefosforyleerd DGCR8 werd waargenomen op deze hybride structuren, vooral waar ze samenvielen met UV-geïnduceerde beschadigingen, wat suggereert dat het helpt schadelijke R-lussen te voorkomen of op te ruimen precies bij actieve genen onder stress.
De controle over DNA-replicatie behouden
Wanneer DNA-schade of R-lussen het kopiëren van het genoom belemmeren, vertragen cellen normaal gesproken de replicatie via een veiligheidscircuit dat bekendstaat als de ATR–CHK1-checkpoint. Fiber-tracking-experimenten toonden aan dat cellen met normaal DGCR8 hun replicatiesporen vertraagden na UV-blootstelling, wat wijst op een geactiveerd checkpoint. In opvallend contrast bleven cellen zonder DGCR8 of met de S153A-mutatie bijna normaal doorrepliekeren, hoewel ze DNA-schade en R-lussen hadden opgehoopt. Verdere tests lieten zien dat terwijl ATR zelf geactiveerd was, zijn belangrijkste partner CHK1 zwak werd ingeschakeld in deze mutante cellen. Dit geeft aan dat gefosforyleerd DGCR8 helpt het stresssignaal van beschadigd DNA en R-lussen naar CHK1 door te geven, zodat de cel kan pauzeren en replicatie kan stabiliseren.
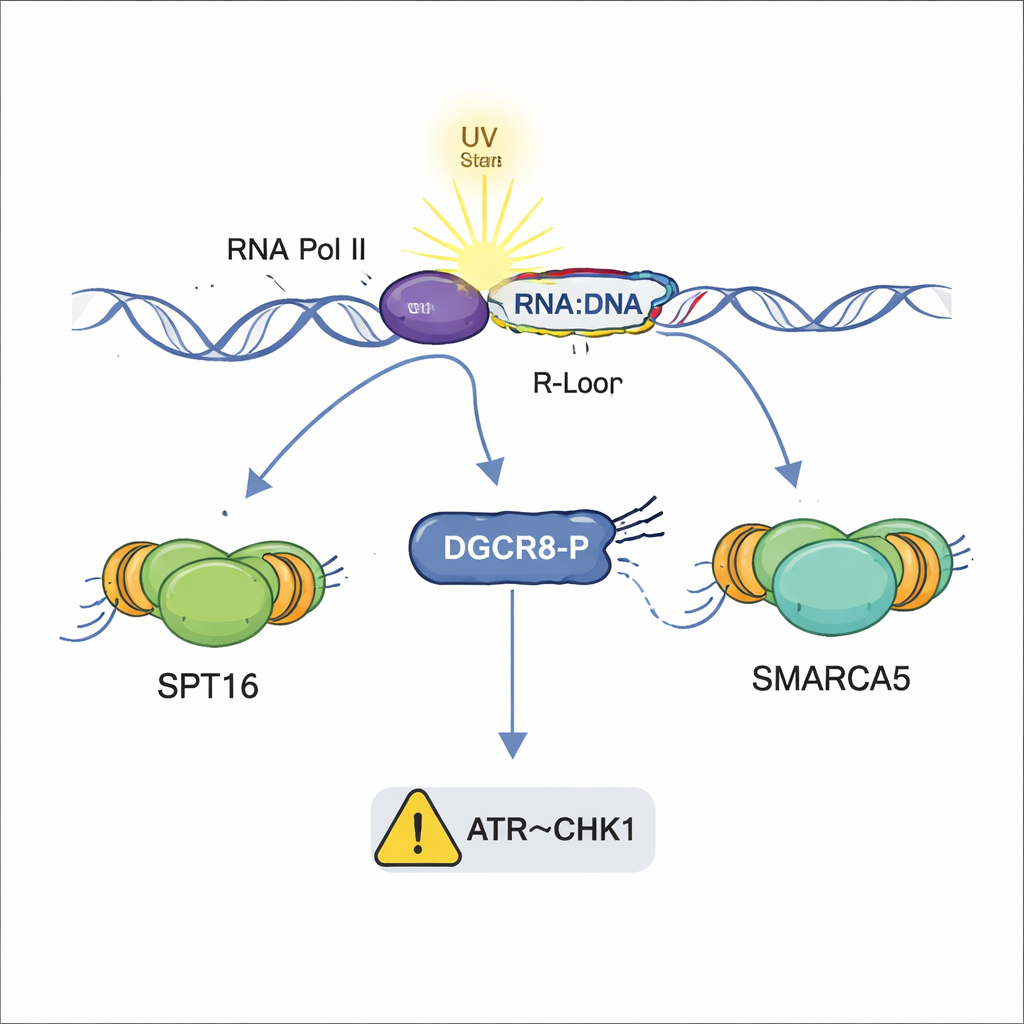
Waarom dit belangrijk is voor gezondheid en ziekte
Gezamenlijk onthullen de bevindingen DGCR8 als een veelzijdige beschermer die meerdere lagen van de UV-schaderespons coördineert: het samenstellen van het TC-NER-herstelteam, het recruteren van chromatine‑remodellers die het DNA opent, het beperken van schadelijke DNA–RNA-hybriden en het helpen activeren van een replicatievertraging via het ATR–CHK1-pad. Cruciaal is dat deze acties losstaan van DGCR8’s traditionele rol in microRNA-biogenese en afhangen van fosforylering van een enkele plaats. Omdat fouten in DNA-herstel en R-luscontrole gekoppeld zijn aan kanker en neurologische ziekten, en DGCR8‑mutaties in sommige tumoren zijn aangetroffen, kan begrip van deze moleculaire schakel nieuwe wegen openen voor diagnose of behandeling van aandoeningen die worden aangedreven door UV‑schade en genoominstabiliteit.
Bronvermelding: Watanabe, T., Yoshinami, D., Yamasaki, H. et al. DGCR8 regulates multiple processes of transcription coupled nucleotide excision repair. Sci Rep 16, 7112 (2026). https://doi.org/10.1038/s41598-026-38338-5
Trefwoorden: UV-DNA-schade, DGCR8, DNA-herstel, R-lussen, genoomstabiliteit