Clear Sky Science · nl
Een nieuwe AI-gekoppelde flowkamermethode die de osmotische fragiliteit van erytrocyten kwantificeert
Waarom de fragiliteit van rode bloedcellen ertoe doet
Elke seconde persen miljoenen van uw rode bloedcellen zich door haardunne vaatjes terwijl ze zuurstof vervoeren. Hoe gemakkelijk deze cellen onder stress barsten — hun “fragiliteit” genoemd — kan wijzen op bloedarmoede, problemen bij bloedopslag en complicaties van ernstige infecties zoals sepsis. Deze studie introduceert een modern, door AI ondersteund microscoopapparaat dat meet hoe snel rode bloedcellen uit elkaar vallen in zoutoplossingen, met als doel deze belangrijke test sneller, preciezer en gemakkelijker uitvoerbaar te maken in onderzoekslaboratoria en op termijn ook in ziekenhuizen.
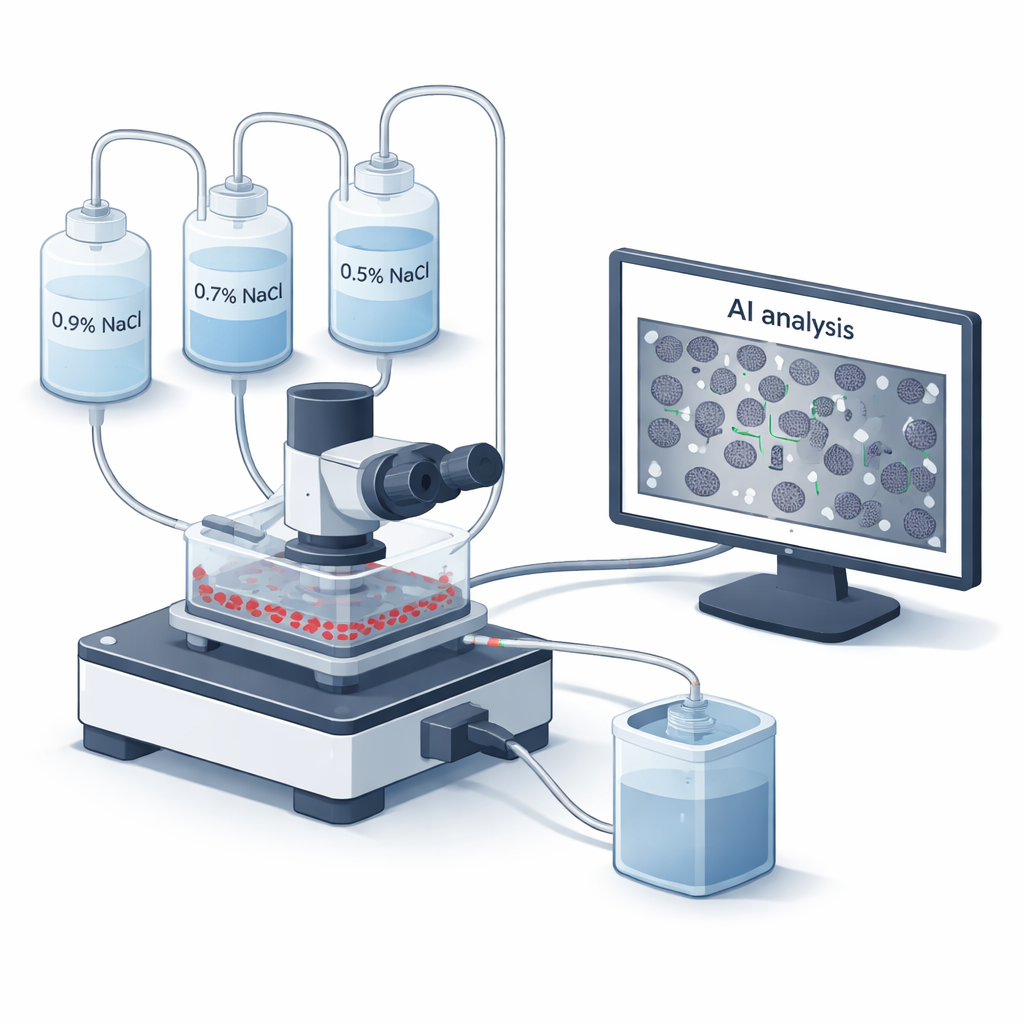
Een nieuwe manier om bloedcellen onder stress te bekijken
Artsen gebruiken sinds de jaren 1940 osmotische fragiliteitstests om te zien hoe stevig de membranen van rode bloedcellen zijn. Traditioneel wordt bloed gemengd met een reeks zoutoplossingen en leest een apparaat af hoeveel hemoglobine naar buiten lekt wanneer cellen barsten. Hoewel betrouwbaar is deze klassieke methode traag, handmatig en blind voor hoe individuele cellen er precies aan toe zijn wanneer ze falen. Het team achter dit artikel bouwde een nieuw microfluïdisch “flowkamer”systeem, BioExP genoemd, dat rode bloedcellen als een dunne monolaag op een behandeld glasplaatje spreidt. Verschillende zoutoplossingen worden over deze laag gepompt terwijl een microscoop en camera in realtime registreren wat er gebeurt, en ingebouwde software gebruikt kunstmatige intelligentie om te tellen hoeveel cellen intact blijven bij elk zoutniveau.
AI en flowregeling op de proef gesteld
Om te beoordelen of BioExP betrouwbaar is, vergeleken de onderzoekers het direct met de ouderwetse spectrofotometerassay met bloed van vier gezonde donoren. Ze concentreerden zich op een sleutelgetal dat MCF₅₀ heet: de zoutconcentratie waarbij de helft van de rode cellen is gehemolyseerd. Eerst moesten ze hun nieuwe systeem afstemmen door de beste “saturatietijd” te vinden — hoe lang cellen aan een bepaalde laagzoutoplossing blootgesteld moeten worden zodat de meest kwetsbare cellen zijn geliseerd zonder te overdrijven. Door bij te houden hoeveel cellen verdwenen bij 0,4% zout over 15 minuten, ontdekten ze dat bijna 80% van de hemolyse in de eerste drie minuten plaatsvond. Dit venster van drie minuten werd hun standaardblootstellingstijd, een compromis tussen snelheid en betrouwbare meting.
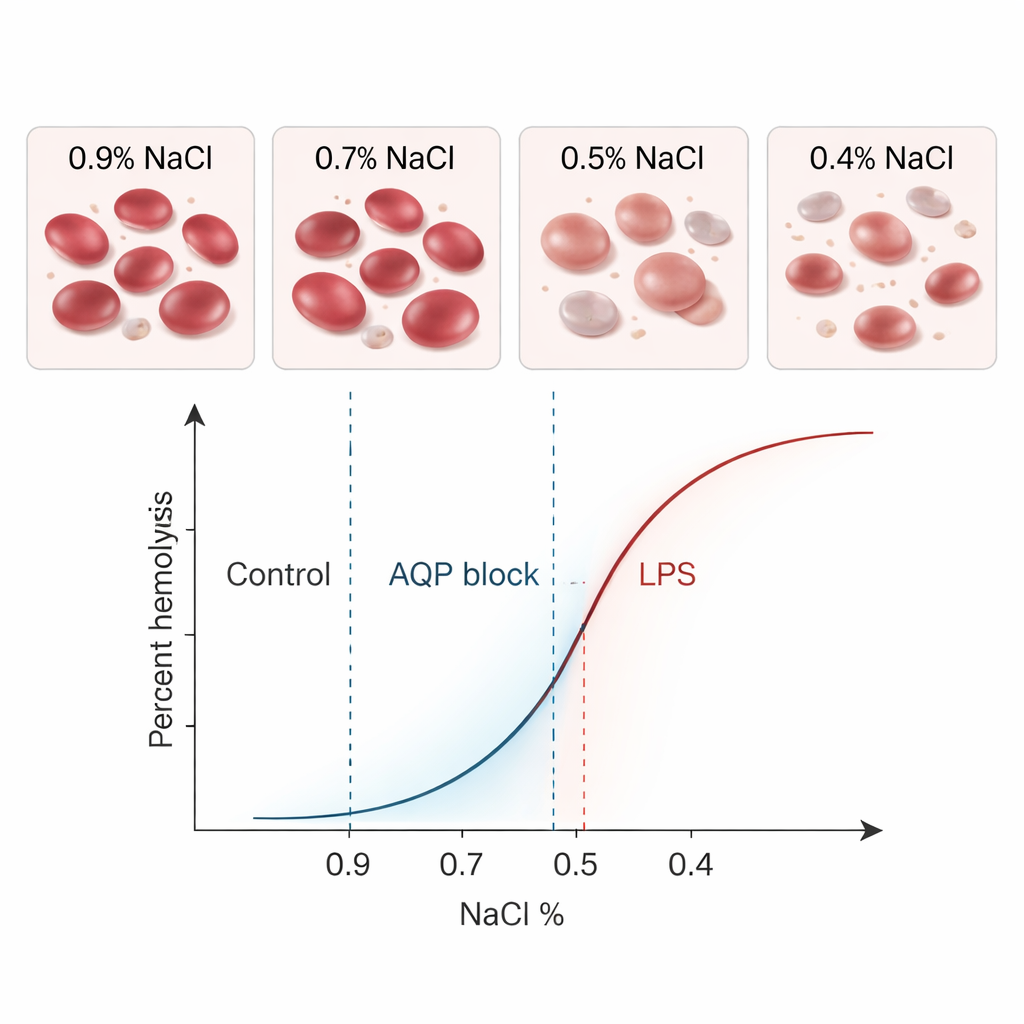
Overeenkomst met de klassieke test en het onderzoeken van echte biologische effecten
Toen ze dezelfde gezonde monsters met beide methoden behandelden, gaven BioExP en de klassieke test vrijwel identieke gemiddelde MCF₅₀-waarden — 0,41% zout — met vergelijkbare variabiliteit. Statistische analyses toonden geen betekenisvol verschil tussen de methoden en de meeste gepaarde resultaten vielen binnen nauwe grenzen van overeenstemming. Met andere woorden: het nieuwe apparaat sprak feitelijk dezelfde taal als de gevestigde assay. De echte kracht van BioExP ligt echter in het vermogen om te onderzoeken hoe verschillende condities de celfragiliteit veranderen. De onderzoekers kozen twee biologisch relevante modulatoren: kwikchloride, dat waterkanaaleiwitten genaamd aquaporines in het celmembraan blokkeert, en bacteriële lipopolysaccharide (LPS), een toxine geassocieerd met sepsis.
Hoe toxinen en waterkanalen de stevigheid van cellen veranderen
Het blokkeren van aquaporines maakte rode bloedcellen moeilijker te laten barsten: de MCF₅₀ verschuifde naar lagere zoutniveaus, wat betekent dat de cellen meer verdunning konden verdragen voordat ze braken. Zowel BioExP als de klassieke methode detecteerden deze verschuiving naar links duidelijk. LPS had het tegengestelde effect. Wanneer rode cellen werden geïncubeerd met een hoge dosis LPS in afwezigheid van plasma, werden ze kwetsbaarder en barstten bij hogere zoutconcentraties. Onder de microscoop veranderden veel cellen van vorm, ze werden bolvormiger of stekelig — visuele tekenen dat hun membranen waren verstoord. Ook hier registreerden beide methoden een sterke, statistisch significante verschuiving naar rechts in de fragiliteitscurven. In al deze tests volgde het nieuwe flowkamersysteem consequent dezelfde biologische trends als de oudere assay, zij het met iets lagere absolute waarden die klein en systematisch waren.
Wat dit betekent voor patiënten en laboratoria
Het BioExP-platform verkort de assa ytijd van meerdere uren tot minder dan een uur, vereist slechts kleine bloedvolumes (mogelijk slechts een vingerprik) en automatiseert het tellen en curve-fitting met AI in plaats van te vertrouwen op veel handmatige stappen. Omdat het dezelfde cellen in de tijd afbeeldt, kan het koppelen hoe cellen eruitzien aan hoe gemakkelijk ze barsten, en het kan veel zoutniveaus of geneesmiddelcondities in één run testen. De studie toont aan dat deze moderne benadering de nauwkeurigheid van de klassieke osmotische fragiliteitstest kan evenaren en daarbij snelheid, flexibiliteit en rijke visuele detail toevoegt. Als het verder gevalideerd wordt in grotere en meer diverse donorpopulaties, zouden dergelijke systemen waardevolle hulpmiddelen kunnen worden voor het diagnosticeren van hemolytische anemieën, het monitoren van opgeslagen bloed in bloedbanken en het onderzoeken hoe infecties of nieuwe geneesmiddelen onze rode bloedcellen verzwakken of beschermen.
Bronvermelding: Fırat, I.S., Alaçayır, Ö., Creutz, T. et al. A novel AI-coupled flow chamber method quantifying erythrocyte osmotic fragility. Sci Rep 16, 7175 (2026). https://doi.org/10.1038/s41598-026-38322-z
Trefwoorden: rode bloedcellen, osmotische fragiliteit, microfluïdica, sepsis, kunstmatige intelligentie