Clear Sky Science · nl
Selectieve Lis1‑inactivatie verstoort migratie en positionering van corticale somatostatine‑interneuronen
Waarom piepkleine hersencellen en één gen ertoe doen
In onze hersenen moeten miljarden zenuwcellen precies op de juiste plek terechtkomen voor gedachten, emoties en geheugen goed kunnen functioneren. Deze studie richt zich op een kleine maar invloedrijke groep hersencellen, de somatostatine‑interneuronen, en op een gen dat Lis1 heet—al bekend omdat mutaties een ernstige "gladde hersenen"‑aandoening veroorzaken. Door te onderzoeken wat er gebeurt wanneer Lis1 alleen in deze kleine celpopulatie wordt uitgeschakeld, laten de onderzoekers zien hoe subtiele fouten in celbeweging tijdens de ontwikkeling sleutelgebieden van de hersenen kunnen herstructureren die betrokken zijn bij stemming, geheugen en psychische ziekten.
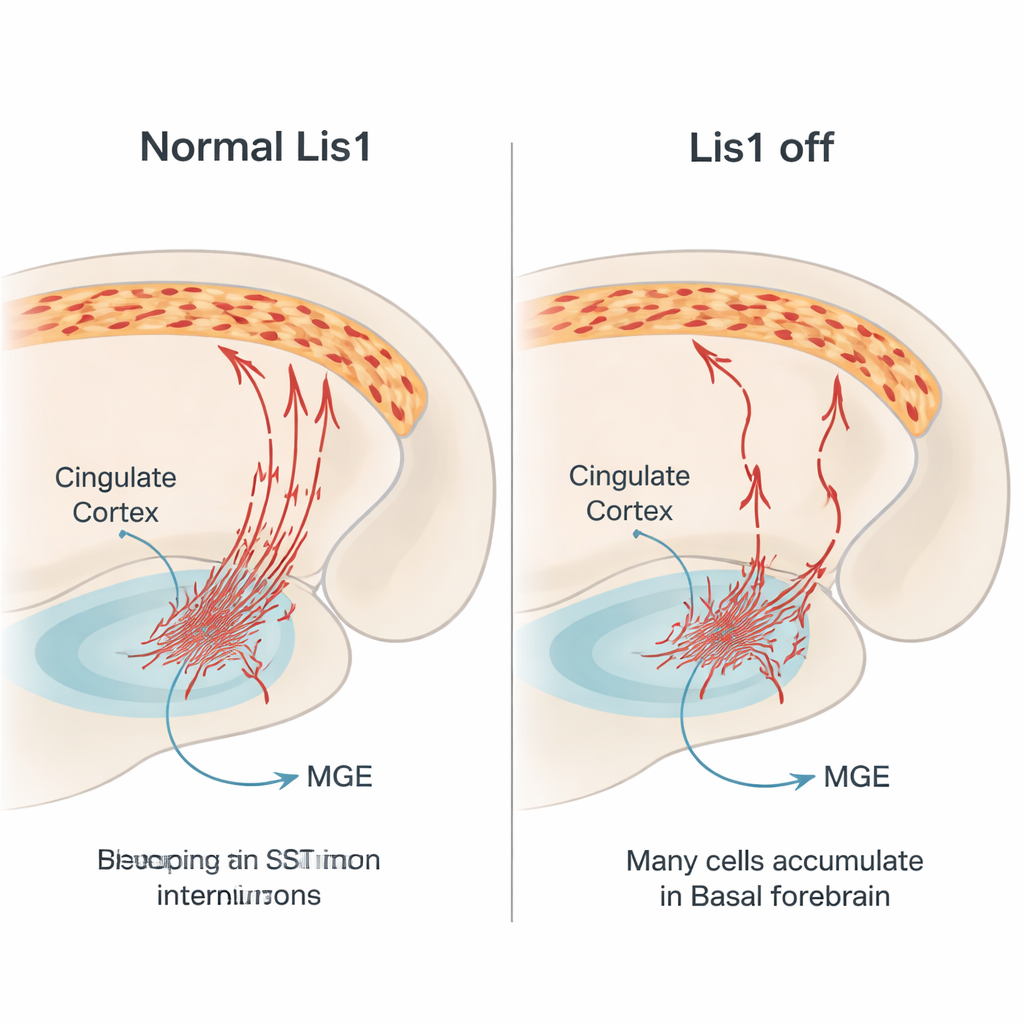
Belangrijke spelers in het remsysteem van de hersenen
Somatostatine‑interneuronen vormen een onderdeel van het remsysteem van de hersenen. Ze geven het remmende signaal GABA en het peptide somatostatine af, en richten zich voornamelijk op de vertakkingen van exciterende piramidale neuronen. Dit helpt de hersenactiviteit in balans te houden, wat essentieel is voor normale waarneming, besluitvorming en emotionele controle. Veel van deze interneuronen ontstaan in een diep embryonaal gebied, de mediale ganglionaire eminentie. Van daaruit reizen ze zijdelings over lange afstanden naar de cerebrale cortex, waaronder de cingulate cortex, een knooppunt voor emotie, pijn en geheugen. Omdat die reis complex en nauw getimed is, zijn genen die celbeweging sturen cruciaal. Lis1 is zo’n gen: het reguleert het interne steigerwerk en het motorsysteem van de cel dat de kern verplaatst en de celvorm tijdens migratie bepaalt.
Een gerichte genetische "uitschakel"‑proef
Om te achterhalen wat Lis1 specifiek doet in somatostatine‑interneuronen, creëerden de auteurs muizen waarin Lis1 alleen wordt verwijderd in cellen die het somatostatine‑gen aanzetten. Ze gebruikten ook een fluorescerend rood eiwit om deze cellen blijvend te markeren en tijdens de ontwikkeling te volgen. Dit ontwerp stelde het team in staat effecten binnen de somatostatinecellen zelf te onderscheiden van veranderingen elders in de hersenen. Vervolgens onderzochten ze twee cingulategebieden—de anterior cingulate cortex en de retrospleniale cortex—ongeveer een maand na de geboorte, een tijd waarin corticale circuits redelijk volwassen maar nog plastisch zijn. Zorgvuldige telmethoden werden gebruikt om zowel het absolute aantal als de dichtheid van somatostatine‑interneuronen in elke corticale laag te schatten.
Minder interneuronen en een verschoven corticaal patroon
Bij jong‑volwassen muizen zonder Lis1 in somatostatine‑interneuronen bevatten zowel de anterior cingulate als de retrospleniale cortex veel minder van deze cellen dan bij controledieren. De vermindering was groot en consistent over alle onderzochte lagen, wat wijst op daadwerkelijk verlies in plaats van een eenvoudige herverdeling. Bij nadere bestudering van de rangschikking van de overgebleven cellen vonden de onderzoekers een verandering in het gebruikelijke laagpatroon. In gezonde muizen concentreren somatostatine‑interneuronen zich doorgaans meer in de diepere lagen van de cortex. Bij de mutanten was dit gradiënt omgekeerd: relatief meer cellen in de bovenste lagen en minder in de diepste laag. Belangrijk is dat de totale omvang van de cingulategebieden niet kleiner werd, zodat de lagere dichtheid daadwerkelijk ontbrekende interneuronen weerspiegelt en niet een samengedrukte weefselvolume.
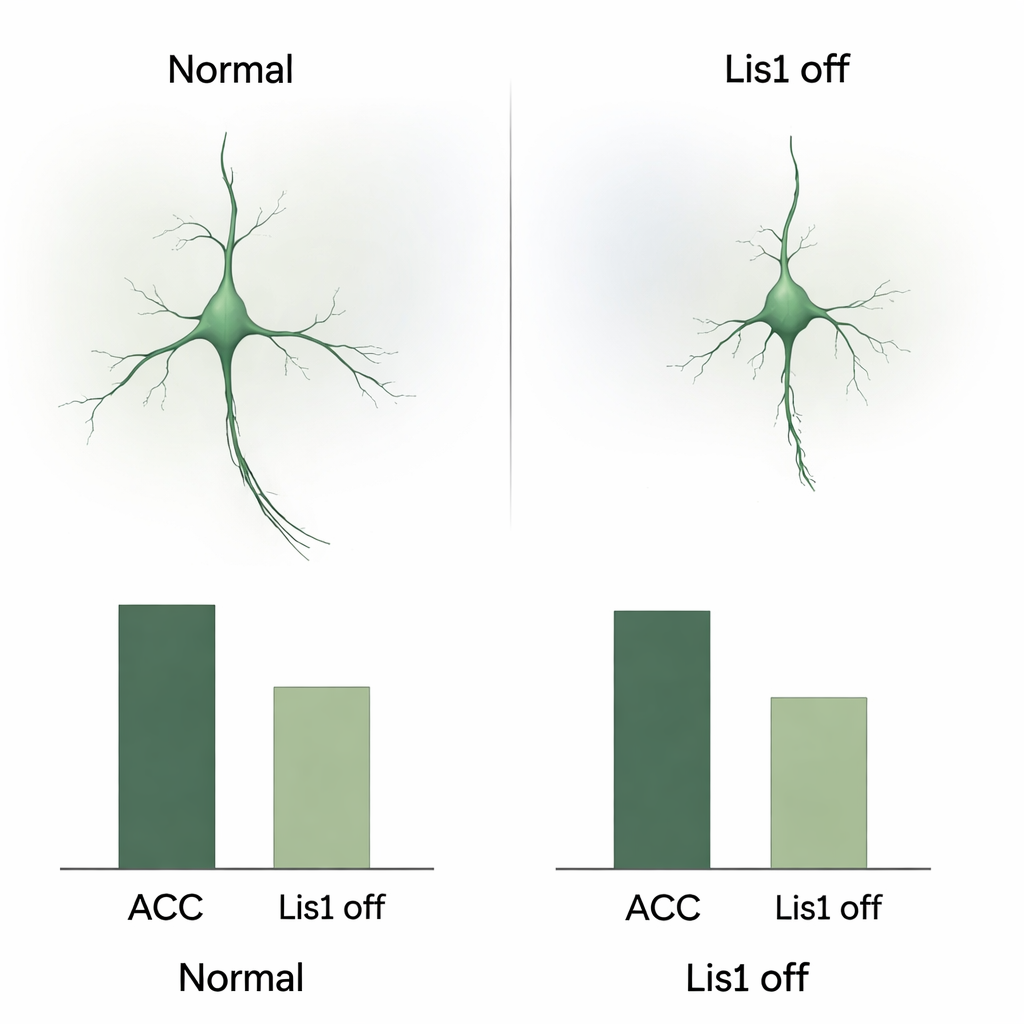
Een ontwikkelingsreis die misgaat
Om te begrijpen hoe dit verlies ontstaat, volgde het team de rood gemarkeerde somatostatinecellen in embryo’s. Ze bevestigden dat Lis1‑verwijdering begint nadat deze cellen niet meer delen, waarmee een direct effect op hun geboorte werd uitgesloten. In plaats daarvan deed het probleem zich voor tijdens hun lange migratie. In de midden‑embryonale fasen werden veel minder gemarkeerde cellen gevonden die via de normale paden naar de cortex trokken, en velen leken vast te lopen in de basale voorhersenen, een ventraal gebied dat ze moeten doorkruisen. De migrerende cellen die wel bewogen toonden gewijzigde vormen: kortere voorste uitlopers, minder vertakkingen en kleinere, rondere cellichamen—allemaal aanwijzingen dat hun interne transportmechaniek verstoord is. In latere stadia bevatte het ventrale gebied bij mutanten meer cellen met merkers van geprogrammeerde celdood, wat suggereert dat veel vastgelopen interneuronen sterven voordat ze de cortex bereiken.
Wat dit betekent voor hersengezondheid
Simpel gezegd: wanneer Lis1 alleen in somatostatine‑interneuronen wordt uitgeschakeld, starten veel van deze cellen hun reis normaal maar bereiken ze hun eindbestemming in de cingulate cortex niet. Sommige hopen zich op en sterven onderweg, en degenen die wel aankomen zijn talrijker in minderheid en ongelijk verdeeld over de corticale lagen. Omdat somatostatinesystemen herhaaldelijk in verband zijn gebracht met depressie, schizofrenie, epilepsie en neurodegeneratieve ziekten, benadrukt dit werk een directe, celspecifieke route waarop Lis1‑disfunctie kan bijdragen aan verstoorde hersenritmes en psychiatrische symptomen. De studie toont aan dat zelfs een betrekkelijk kleine neuronale populatie, gestuurd door één gen, cruciaal kan zijn voor het vormen van de gebalanceerde circuits die gezond denken en gedrag mogelijk maken.
Bronvermelding: Pombero, A., García-López, R., Geijo-Barrientos, E. et al. Selective Lis1 inactivation disrupts migration and positioning of cortical somatostatin interneurons. Sci Rep 16, 7330 (2026). https://doi.org/10.1038/s41598-026-38316-x
Trefwoorden: somatostatine‑interneuronen, Lis1‑gen, neurale migratie, cingulate cortex, neuro‑ontwikkelingsstoornissen