Clear Sky Science · nl
Ontwikkeling en karakterisering van geïmmortaliseerde muis-darmepitheelcelijnen
Waarom nieuwe darmcelmodellen belangrijk zijn
De bekleding van de darm is een drukke grens waar voedsel, nuttige microben en gevaarlijke kiemen samenkomen met ons lichaam. Om te bestuderen hoe deze barrière zich vormt, herstelt en infecties bestrijdt, hebben wetenschappers betrouwbare cellen nodig die ze in het laboratorium kunnen kweken. De huidige driedimensionale “mini‑darm” culturen zijn krachtig maar duur, kwetsbaar en technisch veeleisend, wat hun toegankelijkheid beperkt. Deze studie introduceert een praktischer reeks muis‑darmcelijnen die gemakkelijk te kweken zijn, genetisch goed te manipuleren en toch dichtbij echt weefsel blijven voor veel belangrijke biologische en ziektegerelateerde vragen.
Van muisdarm naar labvriendelijke cellen
De onderzoekers begonnen met kleine segmenten van de muisdunne darm en de dikke darm, en isoleerden kleine celclusters die onder andere intestinale stamcellen bevatten. Deze clusters, spheroïden genoemd, hebben normaal een rijk mengsel van groeifactoren en een gelachtige draaglaag nodig om te overleven. Het team gebruikte een viraal afleversysteem om een gen genaamd SV40 large T‑antigeen in te brengen, waardoor cellen zich onbeperkt blijven delen en zo “geïmmortaliseerde” lijnen ontstaan. Vervolgens leidden ze de cellen geleidelijk af van het complexe medium en de gelondersteuning, en pasten ze aan om te groeien als eenvoudige platte lagen op standaard plastic schotels in gangbare voedingsoplossingen. Klonen werden geselecteerd op basis van hun verschijningsvorm—ofwel meer velachtig en epitheliaal ofwel meer fibroblastachtig—en gecontroleerd op afwezigheid van veelvoorkomende verontreinigingen zoals mycoplasma. 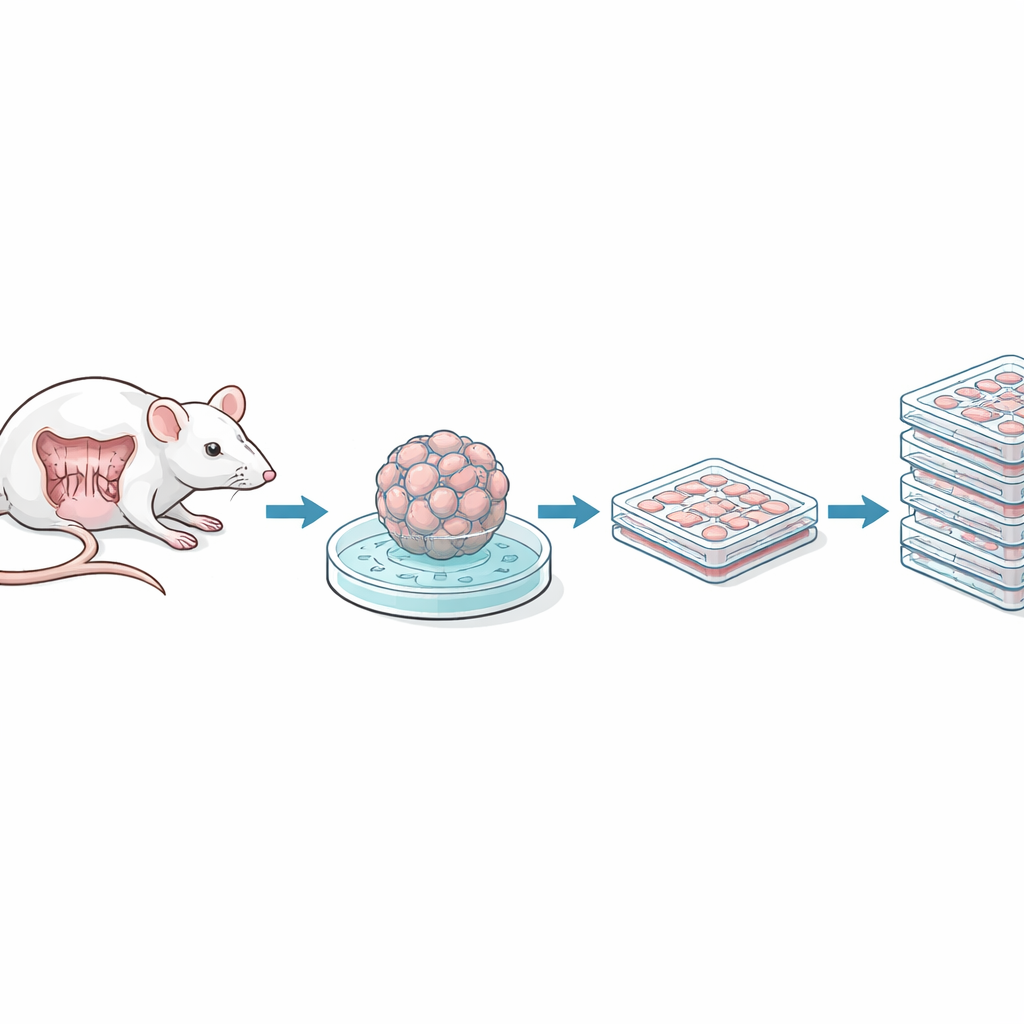
Bevestigen van identiteit en genetische gezondheid
Het geïmmortaliseerd maken van cellen kan ongewenste genetische veranderingen veroorzaken, dus het team verifieerde zorgvuldig wat ze hadden gemaakt. Met DNA‑vingerafdrukmethoden toonden ze aan dat de nieuwe cellijnen nog steeds sterk overeenkwamen met het oorspronkelijke C57BL/6‑muisweefsel en dat er geen menselijk DNA was binnengeslopen. Chromosoomspreidingen toonden enkele extra of herschikte chromosomen, wat gebruikelijk is bij langdurig gekweekte lijnen, maar over het geheel genomen waren de nieuwe lijnen minder sterk veranderd dan veelgebruikte muisdarmen‑kankerlijnen. Wanneer ze werden gekweekt in een veeleisender lucht‑vloeistofinterface‑opstelling die normaal volledige intestinale differentiatie bevordert, vormden de geïmmortaliseerde cellen een basale enkelvoudige laag met een borstelrand‑achtig oppervlak, hoewel ze niet volledig uitgroeiden tot alle gespecialiseerde celtypen die in natief darmweefsel voorkomen. Dit suggereert dat ze het meest lijken op actief delende voorlopercellen in plaats van volledig gedifferentieerde cellen.
Moleculaire persoonlijkheid: tussen epitheel en herstelmodus
Om deze cellen op het niveau van genexpressie te begrijpen, vergeleek het team hun RNA‑profielen met die van de oorspronkelijke spheroïden en met normale darmceltypen. De geïmmortaliseerde cellen hadden klassieke epitheliale merkers omlaag gereguleerd en genen geactiveerd die geassocieerd zijn met een proces dat epitheel‑mesenchymale transitie heet, waarbij cellen hun verbindingen versoepelen en mobieler worden—een toestand die vaak wordt gezien tijdens wondgenezing en in kanker. Toch bleven ze veel junctionele eiwitten tot expressie brengen en behielden ze duidelijke signaturen die aangaven of ze afkomstig waren van de dunne darm of de dikke darm. In het algemeen leken de lijnen op ‘transit amplifying’ voorlopercellen—snel delende tussenstadia tussen stamcellen en rijpe darmcellen—wat suggereert dat ze een regeneratief, op herstel gericht epitheel modelleren.
Gemakkelijk te herprogrammeren en te belasten met microben
Een belangrijk voordeel van deze nieuwe lijnen is hoe gemakkelijk ze genetische en omgevingsmanipulaties accepteren. De onderzoekers konden DNA in de cellen brengen met standaard transfectiereagentia en met lentivirale vectoren, wat sterke fluorescerende reporter‑signalen opleverde. Ze testten vervolgens hoe goed de cellen gast‑microbe‑ontmoetingen modelleren. Bij infectie met vesiculair stomatitisvirus ondersteunden de cellen virale replicatie, maar ze konden dosisafhankelijk beschermd worden door voorafbehandeling met interferon, een sleutelantivirale signaalmolecuul. Dezelfde cellen schakelden snel klassieke interferon‑gestimuleerde genen aan, wat een intact antiviraal antwoord bevestigde. In afzonderlijke experimenten lieten de cellen invasie en overleving van Salmonella‑bacteriën toe en reageerden ze op bacteriële componenten door de NF‑κB‑route te activeren en een reeks ontstekingsbevorderende cytokinen en chemokinen te afscheiden, gedragingen die passen bij een waakzame darmbarrière. 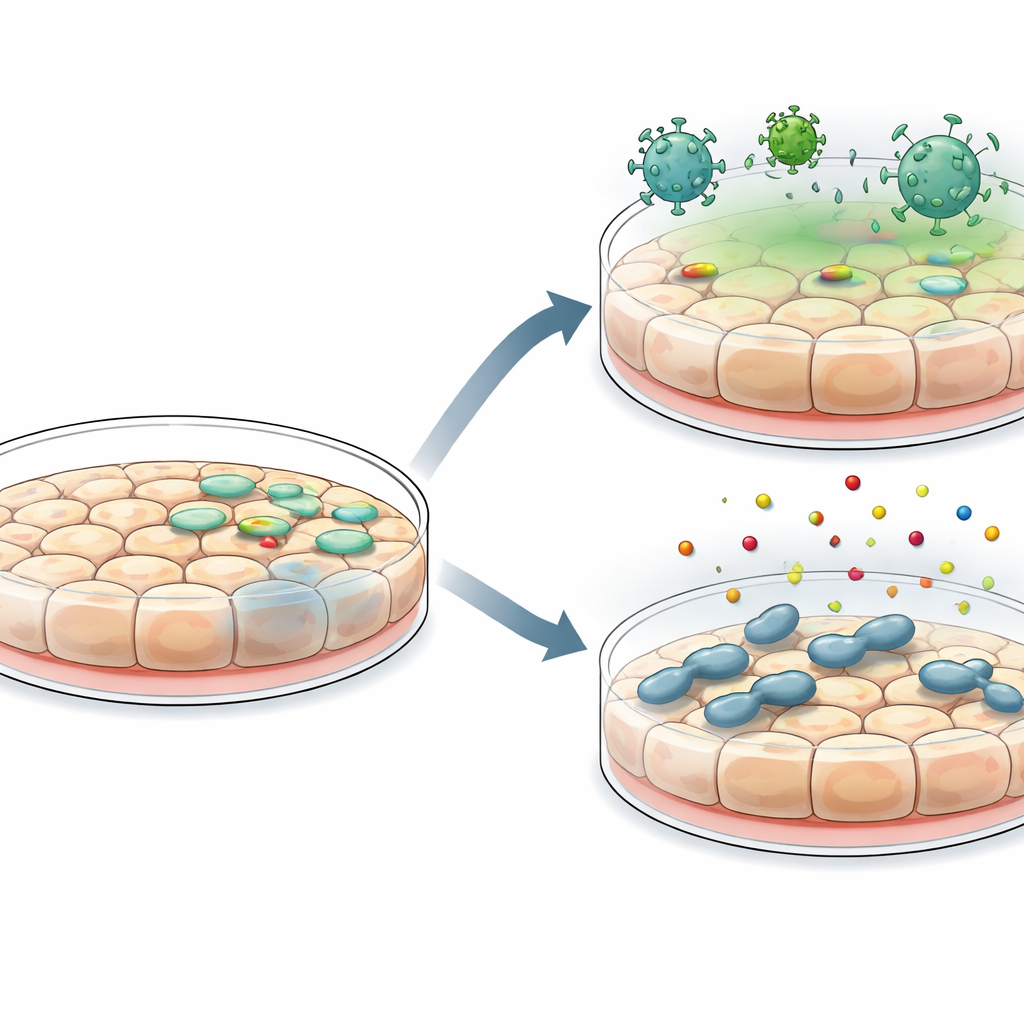
Kosten verlagen en mogelijkheden vergroten
Aangezien deze geïmmortaliseerde lijnen op standaard plastic in eenvoudig medium groeien, zijn ze veel goedkoper en makkelijker hanteerbaar dan driedimensionale mini‑darmen. De auteurs schatten dat het uitvoeren van een screeningscampagne met 10.000 verbindingen tientallen tot honderden keren minder zou kosten met hun systeem dan met primaire spheroïden of organoïden, en dat het minder tijd en gespecialiseerde vaardigheden vereist. Hoewel de cellen niet perfect de volledige diversiteit en structuur van de native darm nabootsen en enkele kenmerken van gedeeltelijke transformatie vertonen, vullen ze een belangrijke nis: een op muizen gebaseerde, genetisch goed te manipuleren en fysiologisch geïnformeerde platform voor high‑throughput ontdekkingen. In de praktijk kunnen deze lijnen dienen als een eerste, schaalbare testomgeving, waarbij veelbelovende bevindingen later worden bevestigd in complexere mini‑darmculturen of in dieren.
Wat dit betekent voor darmonderzoek
Simpel gezegd levert de studie een nieuwe reeks muis‑darmcelijnen op die gemakkelijk te kweken en te modificeren zijn, en die reageren op virussen, bacteriën en immuunsignalen op manieren die overeenkomen met echt darmweefsel. Ze bevinden zich tussen eenvoudige maar slecht gedefinieerde kankerlijnen en veeleisende maar hoogrealistische orgaansystemen. Door zowel technische als financiële drempels te verlagen, zijn deze geïmmortaliseerde intestinale epitheelcellen klaar om onderzoek naar darmontwikkeling, infectie, ontsteking en geneesmiddelresponsen te versnellen, waardoor onderzoekers sneller van basisvragen naar inzichten kunnen gaan die getest worden in modellen met hogere fideliteit en uiteindelijk in levende organismen.
Bronvermelding: Zhou, J.Y., Espenschied, S.T., Lu, Q. et al. Development and characterization of immortalized mouse intestinal epithelial cell lines. Sci Rep 16, 8297 (2026). https://doi.org/10.1038/s41598-026-38295-z
Trefwoorden: intestinal epithelial cells, immortalized cell lines, mouse gut models, host–pathogen interactions, innate immunity