Clear Sky Science · nl
Meervoudige aandacht DeepLab V3+ met EfficientNetB0 voor segmentatie van GI‑tractusorganen in MRI‑opnames
Nauwkeuriger richten op tumoren
Wanneer artsen kanker van het spijsverteringsstelsel met bestraling behandelen, staan ze voor een delicaat evenwicht: de tumor krachtig raken terwijl naburige gezonde organen zoals maag en darmen worden gespaard. Vandaag de dag kan het met de hand omlijnen van die organen op elke MRI‑scan oplopen tot een uur per patiënt per dag. Deze studie introduceert een computervisie‑systeem dat deze organen automatisch in MRI‑beelden volgt, wat snellere, betere behandelplanning en minder bijwerkingen voor patiënten belooft.
Waarom het in kaart brengen van het maag‑darmsysteem telt
Gastro‑intestinale kankers komen veel voor en zijn vaak dodelijk, met een algeheel overlevingspercentage van ongeveer 30 procent. Radiotherapie is een pijler van de behandeling, maar het spijsverteringskanaal ligt dicht opeengepakt in de buik en gezonde organen kunnen van dag tot dag een beetje verschuiven. Om schade aan maag, dunne darm en dikke darm te vermijden, moeten specialisten precies weten waar die organen zich bevinden vóór elke behandelsessie. Handmatig omlijnen is traag en gevoelig voor variatie tussen experts. Een geautomatiseerde, betrouwbare manier om deze grenzen te tekenen zou afspraken kunnen verkorten, artsen in staat stellen meer patiënten te behandelen en de veiligheid en nauwkeurigheid van stralingsdoses verbeteren.
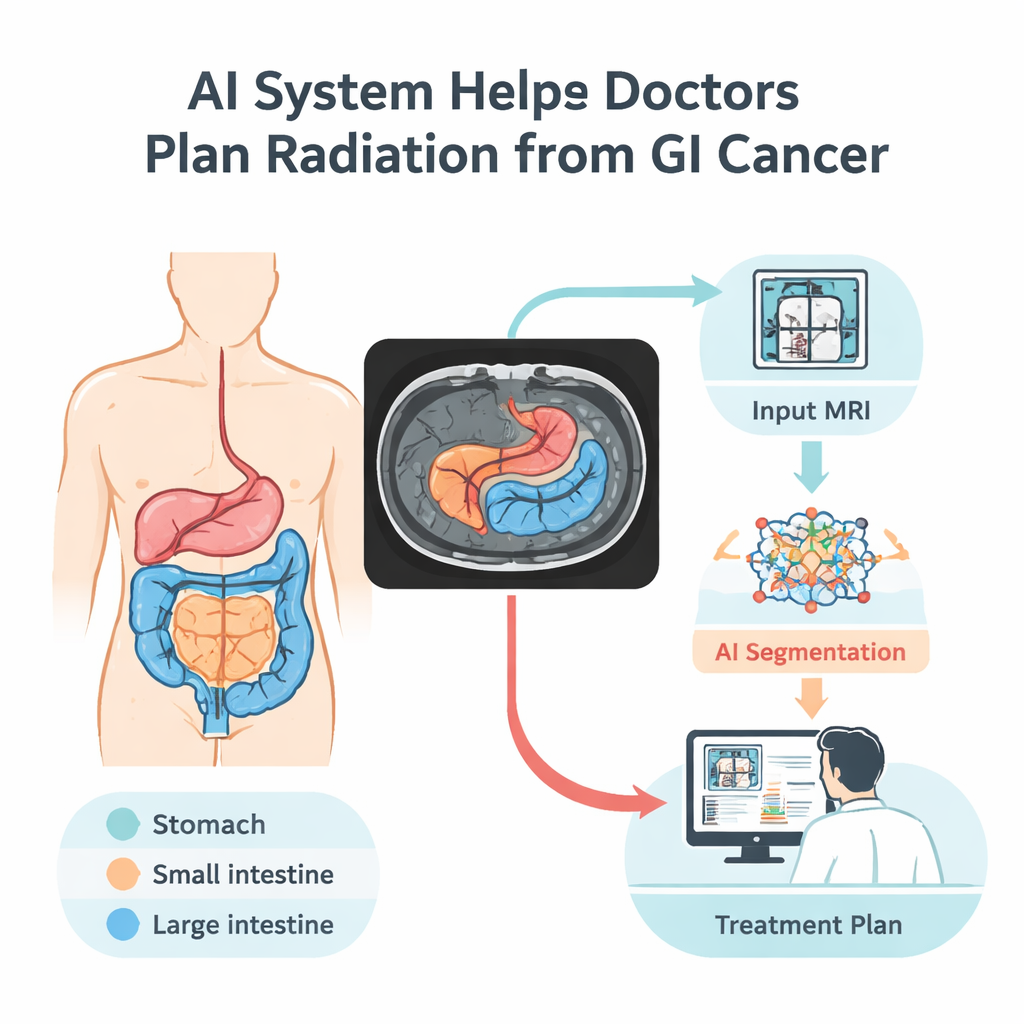
Computers leren MRI‑scans lezen
De onderzoekers bouwden een kunstmatig‑intelligentie‑model dat leert drie belangrijke spijsverteringsorganen op MRI‑scans te herkennen: de maag, de dunne darm en de dikke darm. Ze trainden het op de UW–Madison GI Tract dataset, de enige openbare verzameling met gedetailleerde organenomlijningen op buik‑MRI. Deze dataset bevat 38.496 beelden van 85 patiënten, samen met zorgvuldig voorbereide labels die aangeven waar elk orgaan verschijnt — of waar geen orgaan aanwezig is. Om het maximale uit deze relatief kleine steekproef te halen, splitste het team de data per patiënt (zodat het model nooit dezelfde persoon in zowel training als test ziet) en vergrootte de dataset door beelden te spiegelen, te roteren, helderder te maken en licht te vervormen. Deze gecontroleerde veranderingen helpen het systeem omgaan met realistische variaties in patiëntpositie, beeldhelderheid en subtiele vormverschillen.
Hoe het nieuwe AI‑model patronen ziet
Binnen het model worden verschillende ideeën uit moderne beeldherkenning gecombineerd om het ‘oog’ voor anatomie te verscherpen. Eerst scant een compact netwerk genaamd EfficientNet B0 elke afbeelding en bouwt lagen visuele kenmerken op — van eenvoudige randen tot complexe orgaansilhouetten — terwijl de rekeneisen bescheiden blijven. Vervolgens bekijkt een structuur bekend als DeepLab V3+ het beeld op meerdere schalen, een beetje zoals in‑ en uitzoomen om zowel fijne details als de algemene context te begrijpen. Daarbovenop voegen de auteurs een ‘attention’‑mechanisme op verschillende detailniveaus toe. In eenvoudige termen helpt attention het systeem te beslissen welke delen van de afbeelding en welke interne signalen meer gewicht verdienen, zodat het zich kan concentreren op subtiele maar belangrijke aanwijzingen die bijvoorbeeld de maag onderscheiden van lussen van de dunne darm. Ten slotte hecht een decoderfase deze aanwijzingen weer aan elkaar tot een nette, volledige maskerweergave van de drie organen.
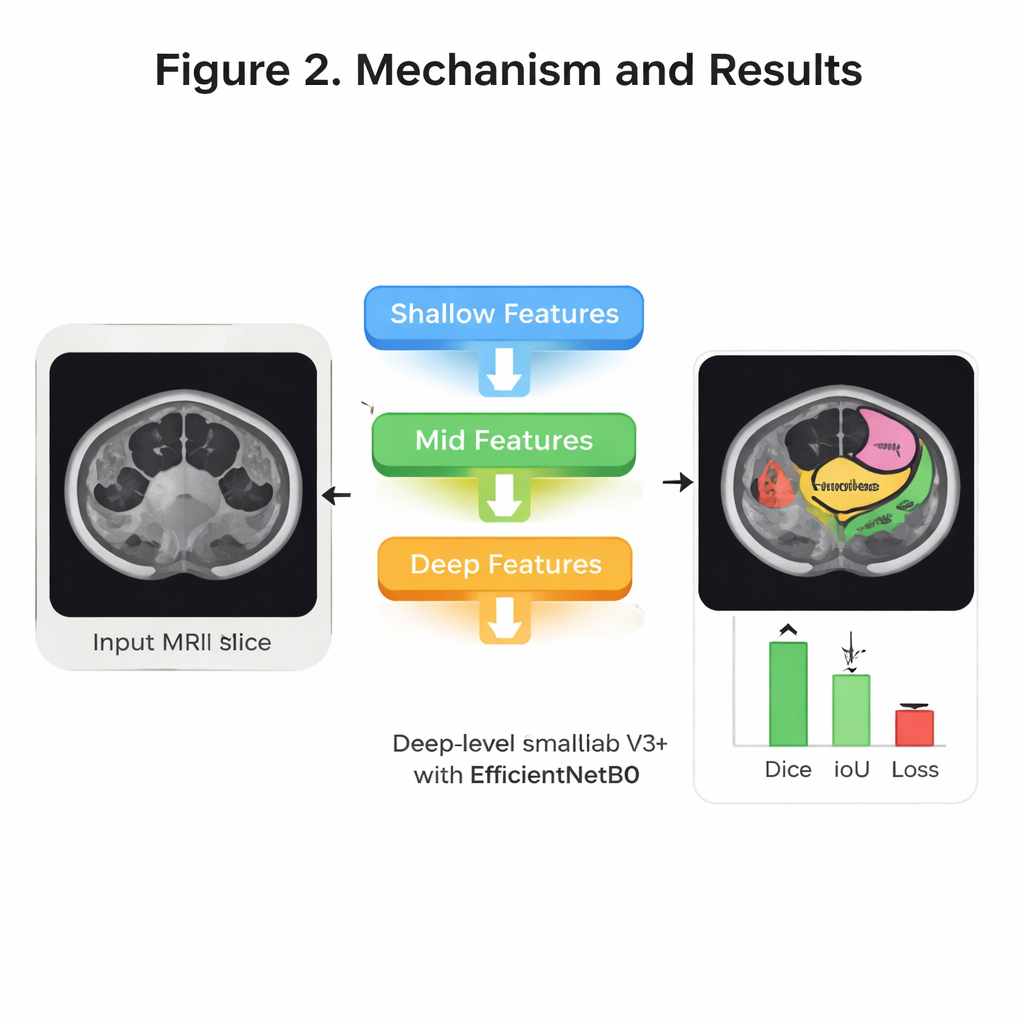
Testen van nauwkeurigheid en efficiëntie
Het team stemde systematisch af hoe ze het systeem trainden — met verschillende optimalisatiemethodes, aantallen trainingsrondes en manieren om de data voor validatie te splitsen. Hun beste configuratie gebruikte een optimizer genaamd RMSprop, vierdelige cross‑validatie en 30 trainingsronden. Op uitgehouden testpatiënten labelde het model meer dan 99 procent van de pixels correct in totaal en liet het een zeer sterke overlap zien met door experts getekende contouren. Een veelgebruikte overlapmaat, de Dice‑score, bereikte gemiddeld ongeveer 94 procent over de drie organen, terwijl een verwante maat, Intersection over Union, rond de 92 procent lag. Even belangrijk voor klinisch gebruik is dat het systeem relatief lichtgewicht is: het heeft ongeveer 8,3 miljoen trainbare parameters en kan een typische 224×224 MRI‑slice verwerken in ongeveer 31 milliseconden, snel genoeg voor vrijwel realtime ondersteuning tijdens dagelijkse behandelplanning.
Wat dit voor patiënten kan betekenen
Simpel gezegd toont deze studie aan dat een zorgvuldig ontworpen AI betrouwbaar de maag en darmen op MRI‑beelden kan volgen, vergelijkbaar met experts maar veel sneller en consistenter. Die mogelijkheid kan radiotherapeuten helpen stralen preciezer rond gevoelige weefsels te richten, waardoor onbedoelde schade en bijwerkingen tijdens de behandeling afnemen. Hoewel het huidige model is getraind op scans van één centrum en voornamelijk gezonde anatomie, biedt het een solide basis voor toekomstige systemen die zieke organen en gegevens uit meerdere ziekenhuizen omvatten. Met verdere tests en verfijning zouden dergelijke hulpmiddelen routineassistenten kunnen worden in de bestraling‑planning, stilletjes zorgend dat levensreddende stralen precies daar terechtkomen waar ze het meest nodig zijn.
Bronvermelding: Sharma, N., Gupta, S., Al-Yarimi, F.A.M. et al. Multi-level attention DeepLab V3+ with EfficientNetB0 for GI tract organ segmentation in MRI scans. Sci Rep 16, 7546 (2026). https://doi.org/10.1038/s41598-026-38247-7
Trefwoorden: gastro-intestinale kanker, MRI‑segmentatie, planning van radiotherapie, deep learning in de geneeskunde, medische beeldanalyse