Clear Sky Science · nl
Een efficiënt diep CNN-gebaseerd BiLSTM-kader met RanA-optimalisatie voor accurate detectie van hartritmestoornissen
Waarom slimere hartcontroles ertoe doen
Hartritmestoornissen zijn wereldwijd een belangrijke oorzaak van plotselinge ziekte en overlijden. Artsen vertrouwen vandaag de dag sterk op elektrocardiogrammen (ECG’s) — die bekende kronkellijnen op een monitor — om gevaar te signaleren. Langdurige ECG‑opnames visueel doornemen is echter traag, vermoeiend en foutgevoelig, vooral wanneer gevaarlijke gebeurtenissen kort of subtiel zijn. Dit artikel beschrijft een nieuw systeem voor kunstmatige intelligentie dat grote ECG‑opnames kan doorzoeken en twee belangrijke aandoeningen — atriale fibrillatie en congestief hartfalen — met opvallende nauwkeurigheid detecteert, en zo continu en real‑time hartmonitoring betrouwbaarder kan maken.
Verschillende hartritmes, verschillende risico’s
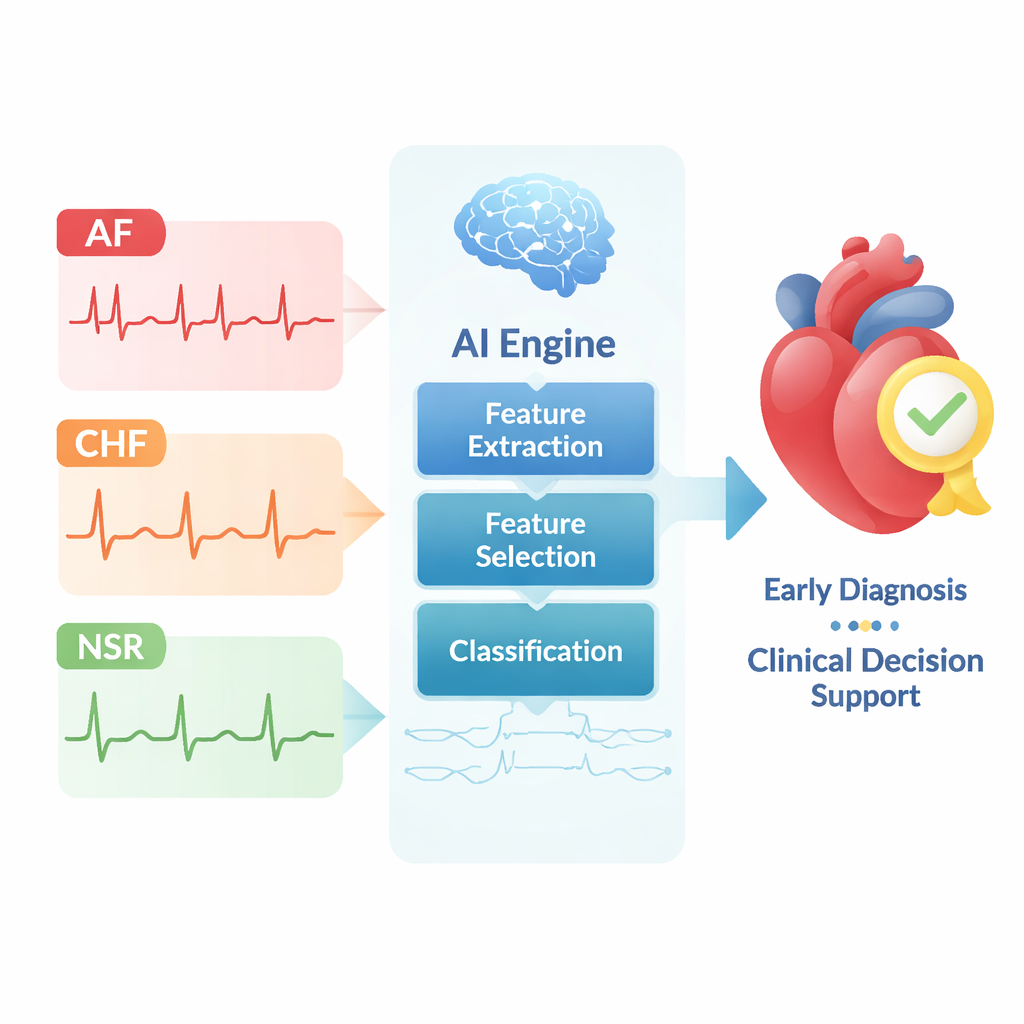
Niet alle hartritmes zijn hetzelfde. Atriale fibrillatie (AF) is een onregelmatig, vaak snel ritme in de bovenste hartkamers dat het risico op beroerte en hartfalen sterk verhoogt. Congestief hartfalen (CHF) is een chronische aandoening waarbij het hart niet genoeg bloed kan pompen, wat leidt tot vermoeidheid, vochtophoping en, indien onbehandeld, overlijden. Normaal sinusritme (NSR) daarentegen is het stabiele ritme dat door de natuurlijke pacemaker van het hart wordt gegenereerd. De auteurs richten zich op twee praktische vragen: kan een computer betrouwbaar AF van NSR onderscheiden, en CHF van NSR, uitsluitend op basis van ECG‑gegevens? Een oplossing hiervoor zou eerdere diagnose, nauwere bewaking van risicopatiënten en snellere respons op verborgen waarschuwingstekens ondersteunen.
Machines leren hartslagen lezen
Moderne ECG‑opnames kunnen miljoenen datapunten per persoon bevatten. Handmatig bruikbare patronen uit deze zee van cijfers halen is praktisch onmogelijk. Daarom bouwen de onderzoekers een meertraps deep‑learning‑pipeline. Eerst verzamelen ze drie bekende ECG‑datasets uit de PhysioNet‑repository: AF‑opnames, CHF‑opnames en opnames van personen met normale ritmes. Ze knippen deze lange signalen vervolgens in kortere segmenten zodat een computer ze efficiënt kan analyseren. Daarna gebruiken ze een type neuraal netwerk dat een Capsule Network wordt genoemd om elk segment te comprimeren tot een kleinere reeks getallen, terwijl de algemene vorm en structuur van de hartslag behouden blijven. Statistische tests tonen aan dat deze stap zieke ritmes beter scheidt van normale ritmes dan standaard reductiemethoden zoals hoofdcomponentenanalyse.
De meest sprekende signalen vinden
Zelfs na compressie blijven veel kenmerken van de ECG‑segmenten redundant of zwak gerelateerd aan ziekte. Om zich te concentreren op wat echt telt, past het team meerdere krachtige beeld‑georiënteerde neurale netwerken toe — EfficientNet B3, ResNet152, DenseNet201 en VGG19 — als intelligente filters. Deze netwerken zijn oorspronkelijk ontworpen om objecten in afbeeldingen te herkennen; hier worden ze hergebruikt om te rangschikken welke ECG‑kenmerken het beste AF, CHF en normale slagen onderscheiden. EfficientNet B3 springt er hierbij uit. Het balanceert diepte en breedte van het netwerk om alleen de meest informatieve patronen te benadrukken, en levert consequent kenmerken die sterker met ziektelabels samenhangen en duidelijker scheidbaar zijn tussen gezonde en ongezonde ritmes.
Luisteren naar ritme in de tijd
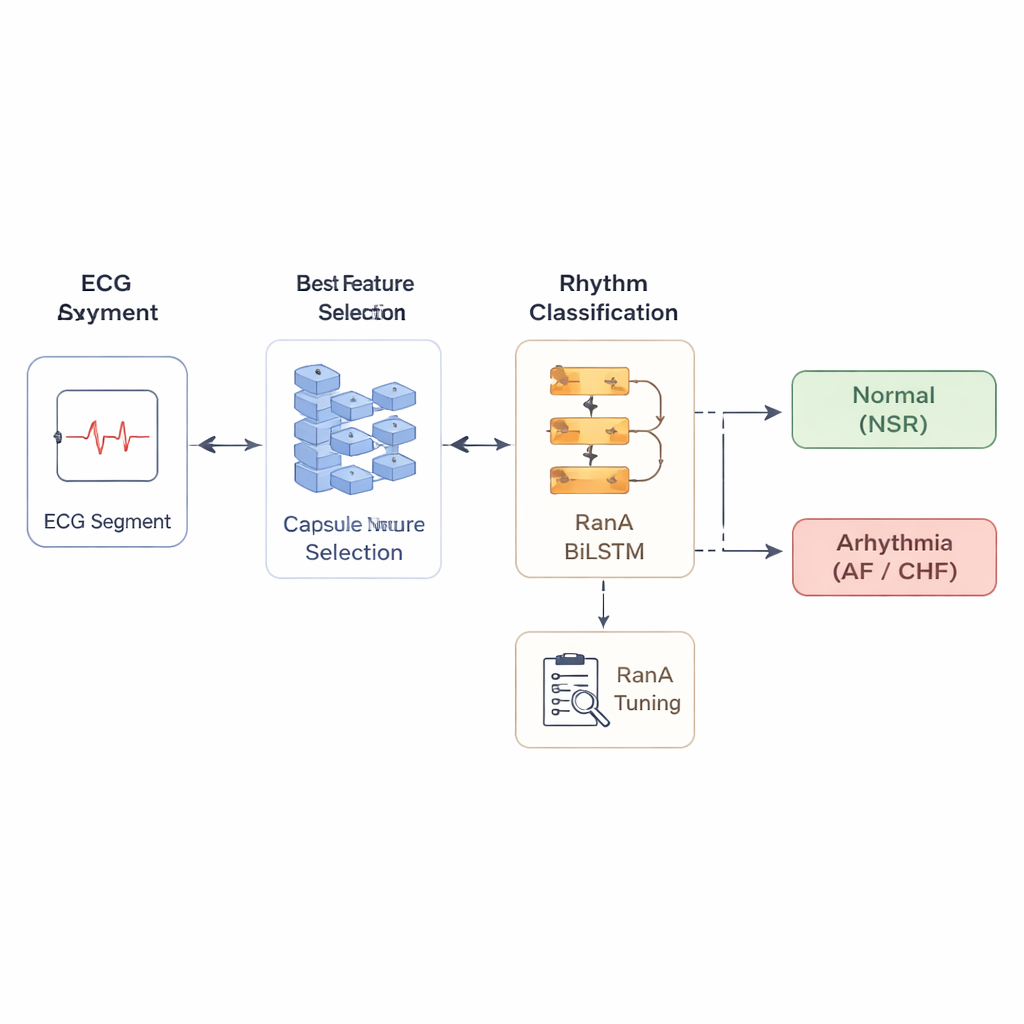
Aangezien hartsignalen zich als sequenties ontvouwen, wordt de eindbeslissing genomen door een model dat goed leert van geordende gegevens: een bidirectioneel long short‑term memory‑netwerk, of BiLSTM. Dit model "luistert" naar elk segment zowel in voorwaartse als achterwaartse richting en legt subtiele temporele relaties vast die op een ritmestoornis kunnen wijzen. Om extra prestaties te winnen, stemmen de auteurs de vele interne instellingen van dit model af met een strategie die zij Randomized Adam (RanA) noemen, die gecontroleerde willekeur in het leerproces injecteert. Dit helpt het systeem te voorkomen dat het vastloopt in suboptimale oplossingen en verbetert het vermogen om te generaliseren naar nieuwe patiënten. De onderzoekers testen de volledige opzet rigoureus met tienvoudige cross‑validatie en een 70/30 train‑testverdeling.
Hoe goed werkt het in de praktijk?
Na optimalisatie behaalt het gecombineerde EfficientNet B3 + BiLSTM + RanA‑systeem opvallende prestaties. Het onderscheidt AF van normaal ritme correct in 99,48% van de gevallen, en CHF van normaal ritme in 99,32% van de gevallen — iets beter dan of vergelijkbaar met de beste resultaten in eerdere studies. Maatstaven die vooral belangrijk zijn voor onevenwichtige medische gegevens, zoals de F1‑score, de Matthews correlatiecoëfficiënt en de oppervlakte onder de ROC‑curve, liggen allemaal zeer dicht bij hun ideale waarden. Tegelijk verwerkt het model elk ECG‑segment in slechts enkele milliseconden en gebruikt het een relatief bescheiden aantal parameters, wat suggereert dat het uiteindelijk op draagbare apparaten of bedmonitoren zou kunnen draaien. De auteurs merken op dat het uitbreiden van de aanpak naar meer verschillende aritmieën, het omgaan met lawaaierigere signalen en het verder verlagen van de rekencomplexiteit belangrijke volgende stappen zijn.
Wat dit betekent voor patiënten en artsen
Voor niet‑experts is de kernboodschap eenvoudig: dit werk laat zien dat een zorgvuldig ontworpen deep‑learning‑systeem als een uiterst nauwkeurige "tweede paar ogen" op ECG‑gegevens kan fungeren. Door gevaarlijke onregelmatige ritmes en signalen van hartfalen automatisch te scheiden van normale slagen, en dat bijna in real‑time te doen, kunnen dergelijke hulpmiddelen clinici sneller waarschuwen, continue monitoring thuis ondersteunen en de kans verkleinen dat een stil maar ernstig probleem onopgemerkt blijft. Hoewel verdere validatie in bredere, realistische omgevingen nodig is, wijst de studie op een toekomst waarin geavanceerde algoritmen stilletjes onze hartslagen op de achtergrond scannen en zowel patiënten als artsen eerder waarschuwen en meer gemoedsrust bieden.
Bronvermelding: Manivannan, G.S., Talawar, S.V., Vasundhara, M.G. et al. An efficient deep CNN based BiLSTM framework with RanA optimization for accurate cardiac arrhythmia detection. Sci Rep 16, 7156 (2026). https://doi.org/10.1038/s41598-026-38227-x
Trefwoorden: hartritmestoornis, elektrocardiogram, deep learning, atriale fibrillatie, hartfalen