Clear Sky Science · nl
Remming van PERK vermindert multiprogramma-celdood via Nrf2/HO-1-activatie bij diabetische retinopathie met geïntegreerde proteomics en functionele bevestiging in HRECs
Waarom het beschermen van zicht bij diabetes belangrijk is
Voor miljoenen mensen met diabetes is een van de meest gevreesde complicaties het geleidelijke verlies van gezichtsvermogen dat bekendstaat als diabetische retinopathie. Deze schade aan het lichtgevoelige weefsel achter in het oog begint vaak stil en lang voordat klachten optreden. De studie achter dit artikel onderzoekt wat precies de kleine bloedvatcellen doodt die het netvlies gezond houden — en test een nieuwe manier om ze te beschermen. Door de cel-"stressreacties" die door hoge bloedsuiker worden veroorzaakt beter te begrijpen en te temperen, hopen onderzoekers het risico op blindheid bij mensen met diabetes te vertragen of zelfs te voorkomen.
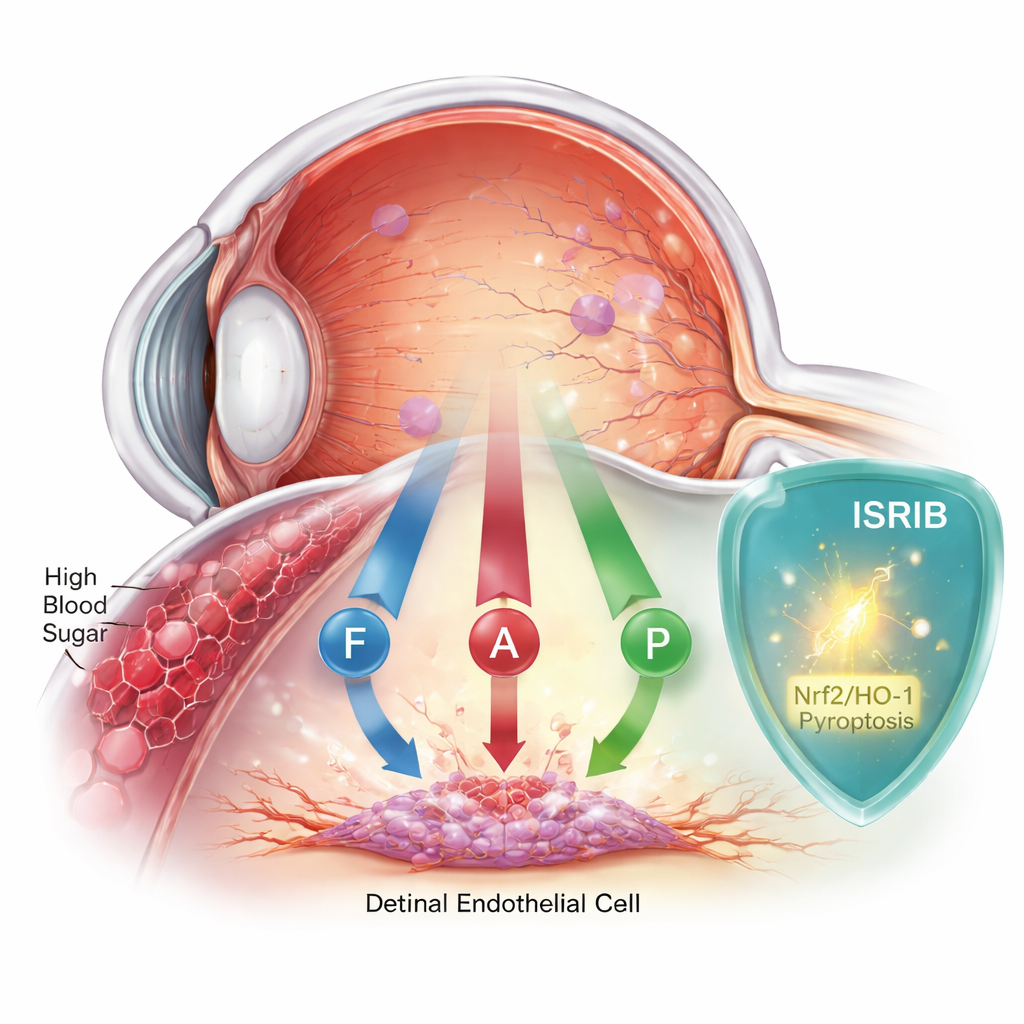
Wanneer bloedsuiker het oog stil beschadigt
Diabetische retinopathie begint wanneer hoge bloedsuiker de kwetsbare binnenbekleding van de netvliesbloedvaten beschadigt. Deze cellen vormen een barrière die het netvlies voedt en beschermt. Jarenlang dachten wetenschappers dat één vorm van celdood, apoptose, vooral de boosdoener was. Toenemend bewijs wijst er echter op dat het verhaal complexer is. Dit team richtte zich op menselijke netvlies-endotheelcellen die in het laboratorium werden gekweekt en blootgesteld aan suikerniveaus vergelijkbaar met die bij slecht gecontroleerde diabetes, en volgde hoe de cellen gedurende twee dagen reageerden.
Drie manieren waarop cellen tegelijk kunnen sterven
Met een krachtige eiwitmeetmethode, proteomics, vonden de onderzoekers dat hoge suikerniveaus honderden eiwitten verstoorden, vooral die betrokken bij stressreacties, stofwisseling en ijzerhuishouding. vervolgtesten toonden aan dat de cellen niet slechts op één manier stierven, maar drie: klassieke geprogrammeerde celdood (apoptose), een vurige, ontstekingsgebonden vorm (pyroptose) en een nieuwere ijzer-gedreven vorm genaamd ferroptose. Merkers van oxidatieve schade, ijzeroverload en uitgeputte antioxidanten namen allemaal toe, terwijl beschermende enzymen afnamen. Samen schetsten deze veranderingen het beeld van cellen die overweldigd werden door stress, ontsteking en toxische ophoping van reactieve moleculen.
Een stressschakelaar in het hart van het probleem
Het team spitste zich vervolgens toe op een sleutelspanner van stress in cellen genaamd PERK, die op het membraan van het endoplasmatisch reticulum zit, een structuur die helpt bij het vouwen en verwerken van eiwitten. Onder hoge suikertoestanden raakte PERK overactief, als een vastgelopen noodalarm dat blijft loeien. Dit leek bij te dragen aan alle drie de doodsprogramma’s. Tegelijkertijd was een natuurlijk verdedigingssysteem dat cellen gewoonlijk helpt omgaan met oxidatieve schade — de Nrf2/HO-1-antioxidantroute — verzwakt. Simpel gezegd: de gevaarsignalen stonden hoog terwijl de interne blusmiddelen laag stonden.
De stress omlaag, de bescherming omhoog
Om te onderzoeken of ze deze destructieve cyclus konden doorbreken, behandelden de onderzoekers de cellen in hoge suiker met ISRIB, een klein molecuul dat de stresssignalering via PERK effectief dempt. De resultaten waren opvallend. ISRIB verbeterde het celsurvival, verminderde merkers van ijzergedreven schade en oxidatieve stress, en verlaagde chemische signalen van zowel apoptose als pyroptose. Tegelijkertijd versterkte het de Nrf2/HO-1-verdedigingsroute, waardoor de cellen hun antioxidantcapaciteit konden herstellen. Een apart medicijn dat specifiek ferroptose blokkeert hielp ook, maar ISRIB stak eruit omdat het alle drie de doodspaden tegelijk kalmeerde in plaats van slechts één.
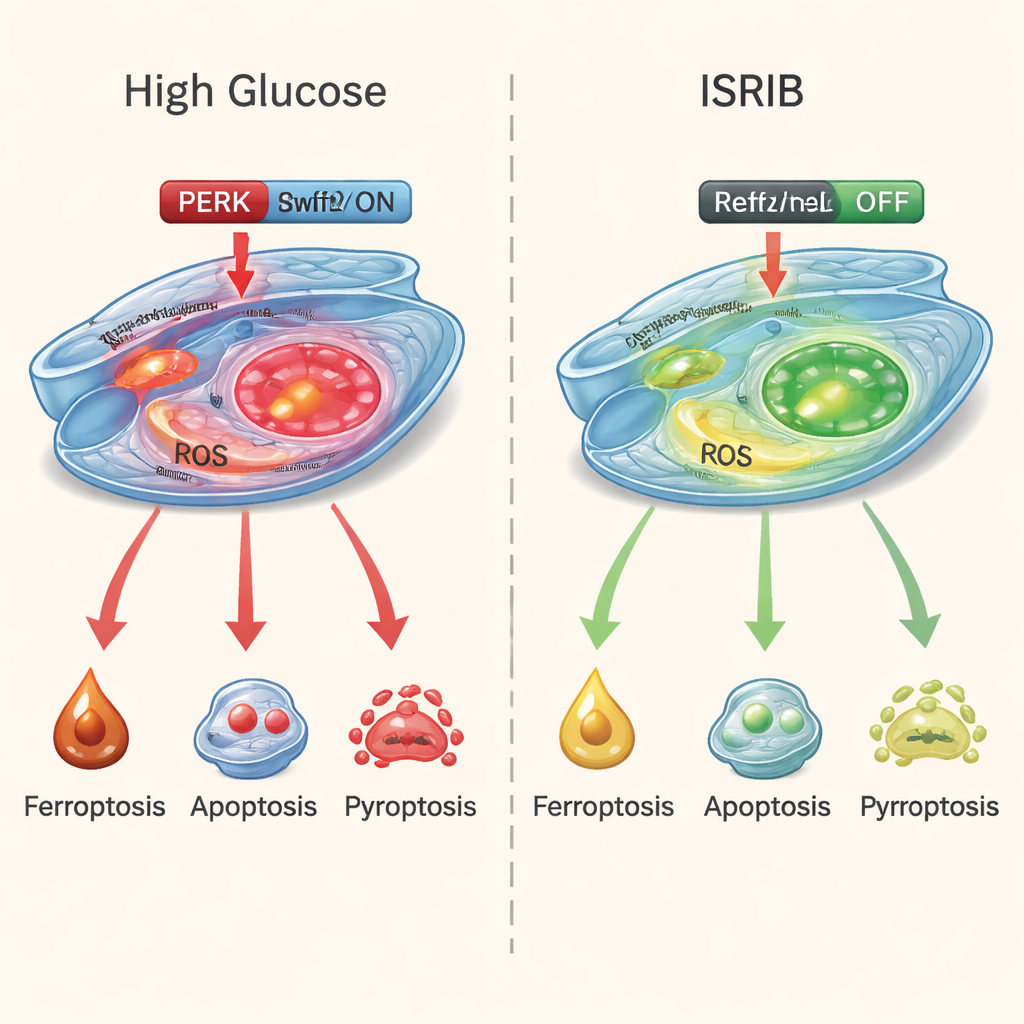
Wat dit zou kunnen betekenen voor mensen met diabetes
Dit werk suggereert dat vroege schade bij diabetische retinopathie niet wordt veroorzaakt door één enkele "schuldige", maar door een samenvloeiing van meerdere elkaar versterkende doodsprogramma’s die worden aangedreven door chronische cellulaire stress. Door de PERK-stressschakelaar omlaag te draaien en de eigen beschermingssystemen van de cel te heractiveren, zouden geneesmiddelen als ISRIB een meer allesomvattende manier kunnen bieden om netvliesbloedvaten in leven te houden. Hoewel deze experimenten in cellen zijn gedaan en nog niet bij patiënten, wijzen ze op toekomstige behandelingen die stressreacties in het oog richten — mogelijk als een aanvullende laag bescherming naast bloedsuikercontrole en de huidige ooginjecties om het gezichtsvermogen bij diabetes te behouden.
Bronvermelding: Xie, L., Zhang, X., Tian, M. et al. PERK inhibition attenuates multi-program cell death through Nrf2/HO-1 activation in diabetic retinopathy with integrated proteomics and functional validation in HRECs. Sci Rep 16, 7225 (2026). https://doi.org/10.1038/s41598-026-38213-3
Trefwoorden: diabetische retinopathie, netvliesceldood, oxiderende stress, PERK-route, Nrf2 HO-1