Clear Sky Science · nl
Remming van het SHH‑pad en co‑cultuur met astrocyten veroorzaken verschillende reacties in glioblastoom en kankerstamcellen
Waarom hersentumoren zo moeilijk te behandelen zijn
Glioblastoom is een van de dodelijkste hersenkankers; zelfs met operatie, bestraling en chemotherapie overleven maar weinig patiënten meer dan vijf jaar. Een reden is dat deze tumoren niet uit één celtype bestaan. Ze bevatten een kleine groep bijzonder hardnekkige “kankerstam”cellen die behandelingen kunnen doorstaan en het gezwel laten teruggroeien. Deze studie stelt een belangrijke vraag: hoe reageren die verschillende tumorcellen wanneer een groeisignaal wordt geblokkeerd, en hoe verandert de aanwezigheid van normale hersensteuncellen, astrocyten genoemd, die respons?
Een nadere blik op de hardste cellen van de tumor
De onderzoekers werkten met twee hoofdtypen cellen uit een gangbaar glioblastoommodel: de bulk tumorcellen en een kleine subpopulatie gemarkeerd door het eiwit CD133, die zich als kankerstamcellen gedragen. Deze stam‑achtige cellen deelden minder, zagen er kleiner en ronder uit en vormden strakkere clusters dan de bulkcellen. Het team kweekte de tumorcellen ook samen met astrocyten, de stervormige cellen die helpen bij het in stand houden van gezond hersenweefsel. Deze gemengde kweek bootst de echte tumorumgeving beter na, waarin kankercellen constant "praten" met hun buren. 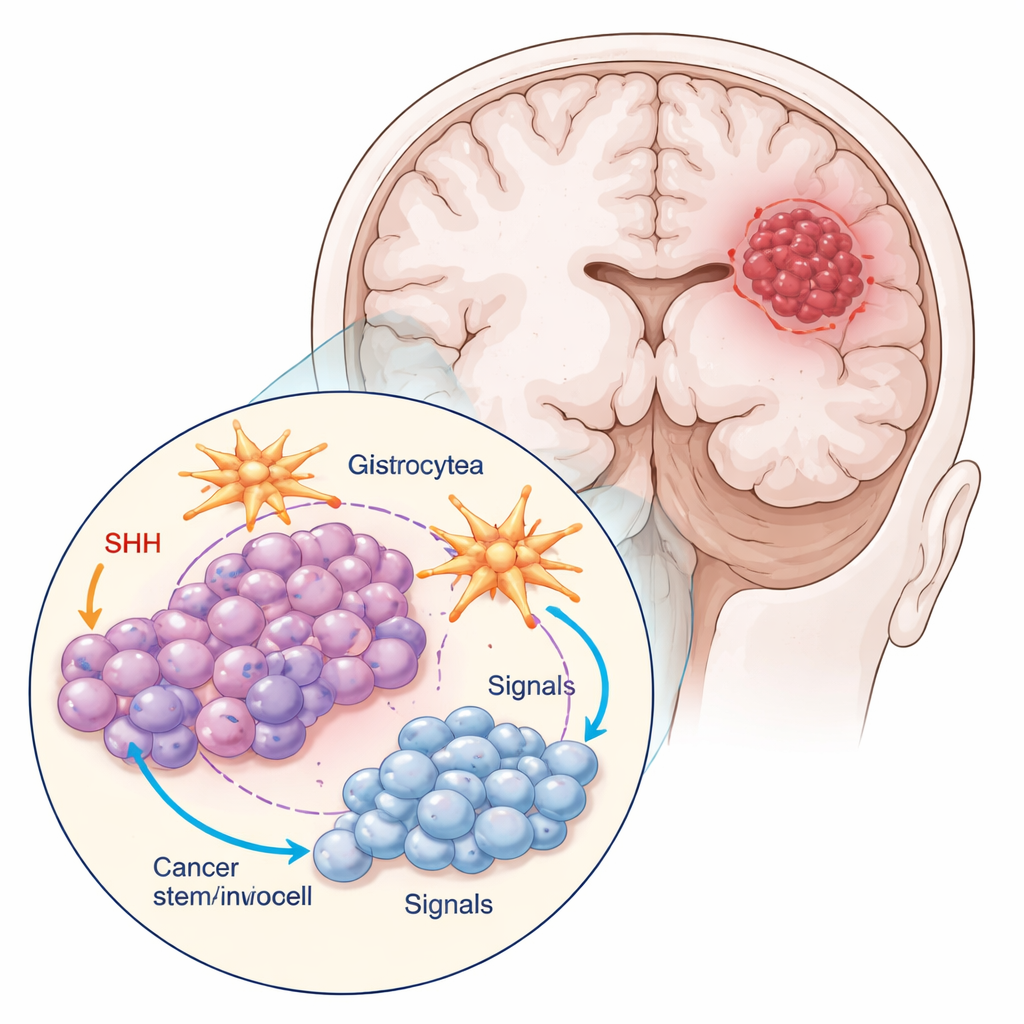
Een ontwikkeld signaal blokkeren dat tumoren hergebruiken
Veel glioblastomen, vooral hun stam‑achtige cellen, kapen een moleculaire communicatieroute genaamd Sonic Hedgehog (SHH), die normaal actief is tijdens hersenontwikkeling. Het team gebruikte cyclopamine, een verbinding die een belangrijk SHH‑component blokkeert, om te zien hoe zowel bulk tumorcellen als kankerstamcellen reageren. Ze maten de activiteit van SHH‑gerelateerde genen en eiwitten, hoe snel cellen door de celcyclus gingen en hoe vaak ze geprogrammeerde celdood (apoptose) ondergingen. Cyclopamine veranderde SHH‑signalering op een manier die sterk afhankelijk was van celtype en van de aanwezigheid van astrocyten. Kankerstamcellen produceerden de meeste SHH‑signalering wanneer ze alleen werden gekweekt, maar deze secretie daalde wanneer ze met astrocyten werden gekweekt en aan het middel werden blootgesteld, wat suggereert dat de omringende hersencellen de chemische "zelf‑ondersteuning" van de tumor kunnen dempen.
Hoe de buurt groei en dood verschuift
Buiten SHH zelf volgde het team ook andere genetische netwerken die bepalen of cellen blijven delen, pauzeren of beginnen te specialiseren. In simpele kweeken met alleen tumorcellen duwde SHH‑remming de bulkcellen naar een stilstand in een latere fase van deling (de G2/M‑fase), terwijl stam‑achtige cellen de neiging hadden op te hopen in een vroegere, rust‑ of toetredingsfase (G0/G1). Toen astrocyten werden toegevoegd, veranderden deze patronen: kankerstamcellen, die eerder meer quiescent waren, verschoven naar G2/M‑arrest, wat wijst op een andere reeks "remmen" die in de gemengde omgeving worden toegepast. De onderzoekers zagen ook dat signalen gekoppeld aan celdoel en weefselvorming—zoals WNT, BMP en TGF‑β‑paden—anders waren afgestemd in bulkcellen en stam‑achtige cellen wanneer astrocyten aanwezig waren, wat betekent dat de micro‑omgeving cellen kan kantelen richting voortgezet stam‑achtig gedrag of juist een meer gedifferentieerde, minder agressieve staat.
Geprogrammeerde celdood opwekken in de meest resistente cellen
De studie bekeek verder hoe gemakkelijk cellen apoptose ondergingen. Genetische uitslagen en een DNA‑schade‑detectietest (TUNEL‑assay) toonden aan dat cyclopamine een externe route naar celdood bevorderde, aangestuurd door een eiwit genaamd CASP8, vooral in de kankerstamcelpopulatie. Interessant genoeg nam in tumorcellen die alleen waren gekweekt de totale celdood soms af na SHH‑blokkade, wat suggereert dat die cellen back‑up overlevingsstrategieën konden activeren. Daarentegen verhoogde cyclopamine bij stam‑achtige cellen die samen met astrocyten werden gekweekt de markers van apoptose, wat aangeeft dat de omringende hersencellen deze anders zo koppige cellen kwetsbaarder kunnen maken zodra SHH‑signalering wordt geblokkeerd. 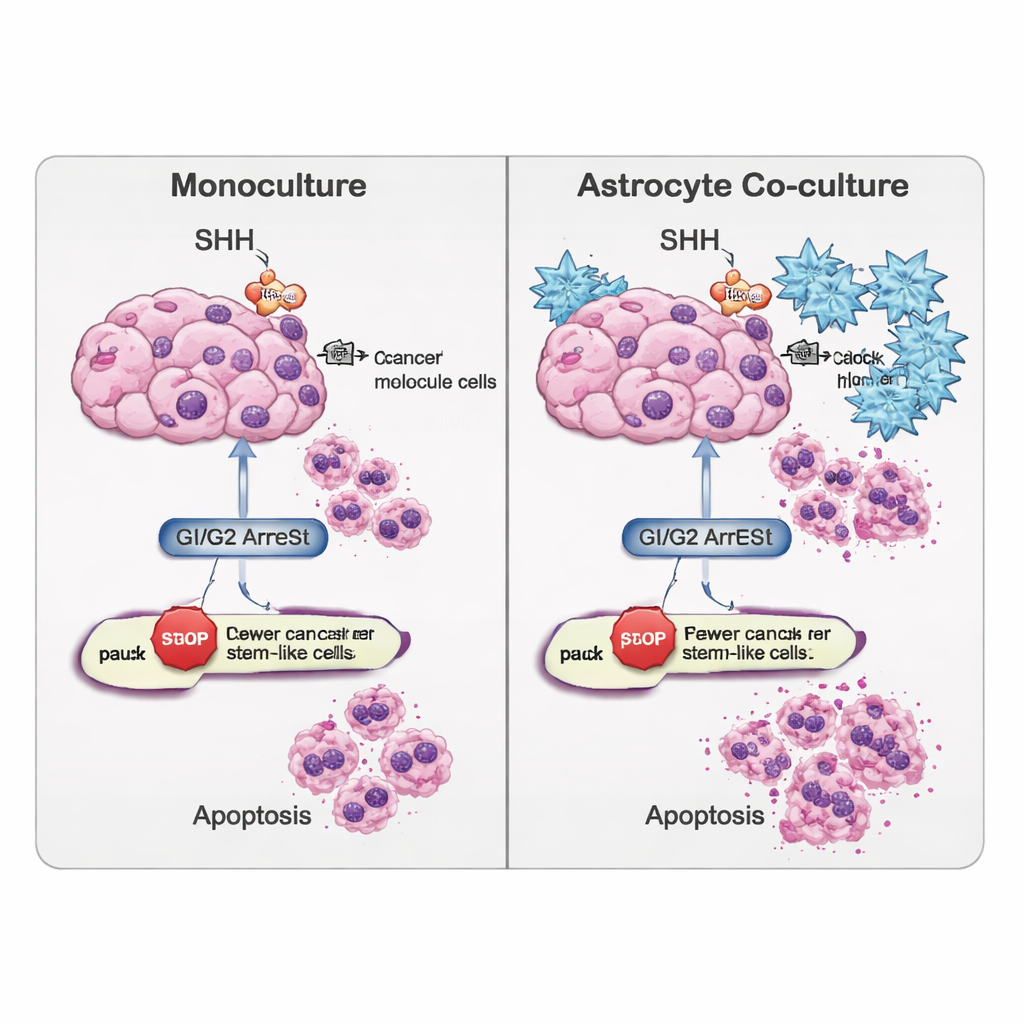
Wat dit betekent voor toekomstige behandelingen van hersenkanker
Voor niet‑specialisten is de kernboodschap dat het richten op één enkel groeisignaal in glioblastoom niet voldoende is als we de buurt van de tumor negeren. Dit werk laat zien dat astrocyten—de normale cellen die ruimte delen met het tumorweefsel—kundig kunnen veranderen hoe zowel bulkkankercellen als kankerstamcellen reageren op SHH‑padblokkade. Kankerstamcellen werden vooral gevoeliger voor celcyclusarrest en een vorm van celdood wanneer astrocyten aanwezig waren. De auteurs concluderen dat geneesmiddelen gericht op SHH en aanverwante paden waarschijnlijker effectief zijn als ze worden getest en uiteindelijk gebruikt op manieren die de echte hersenomgeving weerspiegelen, mogelijk in combinatie met andere behandelingen die de back‑up overlevingsroutes van de tumor aanvallen. Kortom: het begrijpen en benutten van de "conversatie" tussen tumorcellen en hun buren kan leiden tot meer precieze en duurzame strategieën tegen deze anders meedogenloze kanker.
Bronvermelding: Kocaturk, D.C., Ozdil, B., Adali, Y. et al. SHH pathway inhibition and astrocyte co-culture induce distinct responses in glioblastoma and cancer stem cells. Sci Rep 16, 7712 (2026). https://doi.org/10.1038/s41598-026-38199-y
Trefwoorden: glioblastoom, kankerstamcellen, Sonic Hedgehog‑pad, tumormicro‑omgeving, astrocyten