Clear Sky Science · nl
Identificatie en validatie van een nieuw ferroptose-gerelateerd genhandtekening geassocieerd met erfelijke retinale degeneratie bij Rd10-muizen
Waarom stervende oogcellen ons allemaal aangaan
Retinitis pigmentosa is een groep erfelijke oogaandoeningen die geleidelijk iemands gezichtsvermogen wegnemen, vaak beginnend met nachtblindheid en eindigend in compleet verlies van zicht. Er is geen genezing en bestaande gentherapieën helpen slechts een klein deel van de patiënten. Deze studie onderzoekt een andere invalshoek: een speciale vorm van celdood, ferroptose genoemd, aangedreven door ijzer en oxiderende schade, om nieuwe gentargets te vinden die mogelijk op een dag lichtgevoelige cellen in het netvlies kunnen beschermen—ongeacht met welke mutatie iemand is geboren.
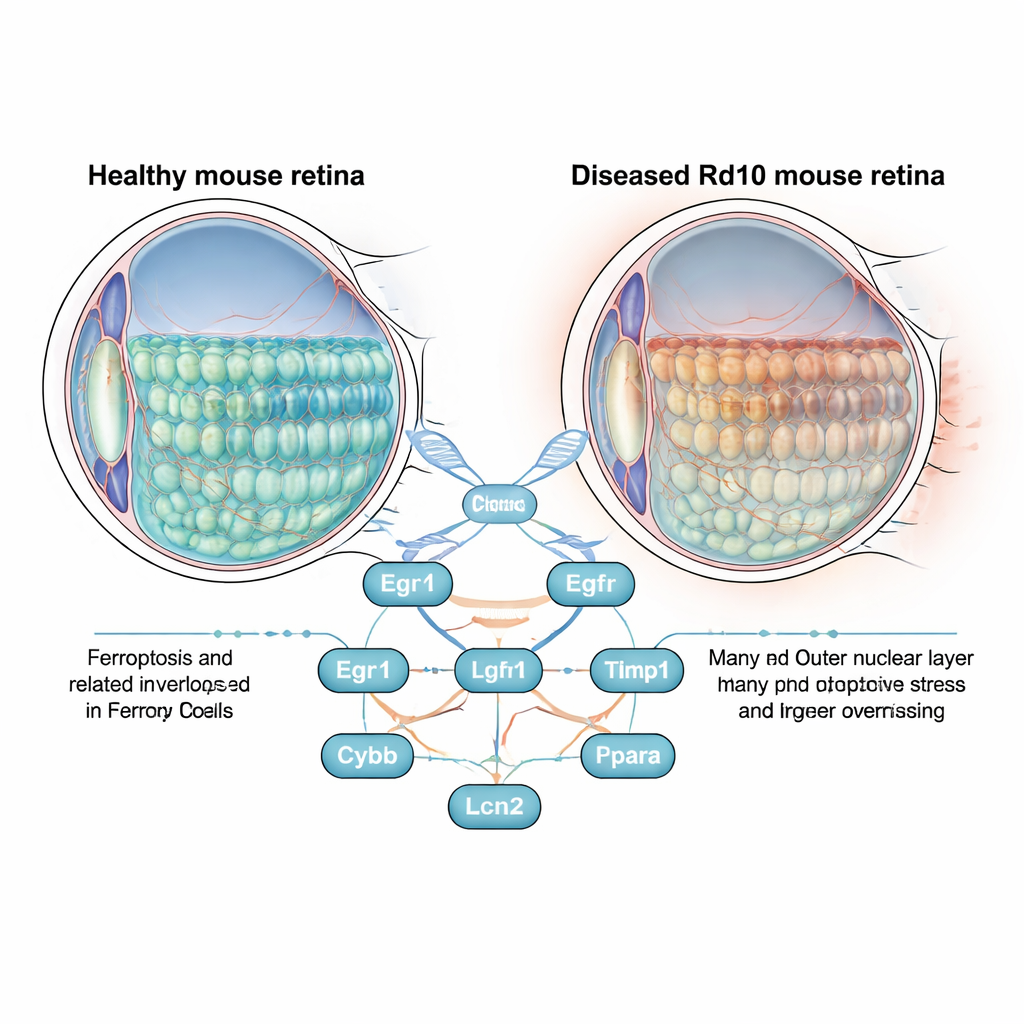
Een nadere blik op een blindmakende oogaandoening
Het netvlies is een dun weefsellag aan de achterkant van het oog met staaf- en kegelfotoreceptoren, de cellen die licht omzetten in elektrische signalen. Bij retinitis pigmentosa sterven deze cellen geleidelijk, waarbij eerst nacht- en zijzicht verloren gaan en later het centrale zicht. Wetenschappers bestuderen dit proces vaak in Rd10-muizen, die een mutatie dragen die de menselijke aandoening nauw nabootst. In plaats van zich uitsluitend te richten op het defecte gen, stelden de auteurs een bredere vraag: naarmate het netvlies degenerereert, welke genen die aan ferroptose gelinkt zijn, worden aan- of uitgezet, en kunnen zij de celdood aansturen?
De sleutelgenen vinden in een zee van data
Het team doorzocht grote openbare gen-expressiedatasets van gezonde en Rd10-muizennetvliezen en nam eigenlijk een globale „momentopname” van welke genen meer of minder actief waren. Ze vonden meer dan 2.000 veranderde genen en controleerden deze vervolgens met een gecureerde lijst van ferroptose-gerelateerde genen. Dit bracht het aantal terug tot 37 kandidaten die verband houden met ijzer-gedreven, oxiderende celdood. Computationele analyses toonden dat deze genen clusteren in processen zoals reactie op oxidatieve stress, regulatie van neuronale celdood en vetmetabolismepaden—kenmerken van ferroptose en bekende stressreacties in degenererende zenuwen.
Acht genen die eruit springen
Om de meest invloedrijke spelers te identificeren bouwden de onderzoekers een eiwitinteractienetwerk en pasten meerdere rangschikkingsalgoritmen toe. Acht „hub”-genen kwamen naar voren: Egr1, Cd44, Egfr, Tlr4, Timp1, Cybb, Lcn2 en Ppara. Zeven daarvan waren actiever in zieke netvliezen, terwijl Ppara minder actief was. De groep bevestigde deze patronen in een onafhankelijk dataset en keek toen nauwkeuriger naar waar de topgenen in het oog verschenen. Met fluorescente kleuring en single-cell RNA-sequencing toonden ze aan dat Egr1 sterk verhoogd is in staaf- en kegelfotoreceptoren, terwijl Cd44 scherp verhoogd is in Müller-cellen, de ondersteunende gliacellen die het netvlies doorkruisen. Dit suggereert dat gestreste fotoreceptoren en hun ondersteunende cellen mogelijk samenwerken—mogelijk op schadelijke wijze—via ferroptose-gerelateerde routes.
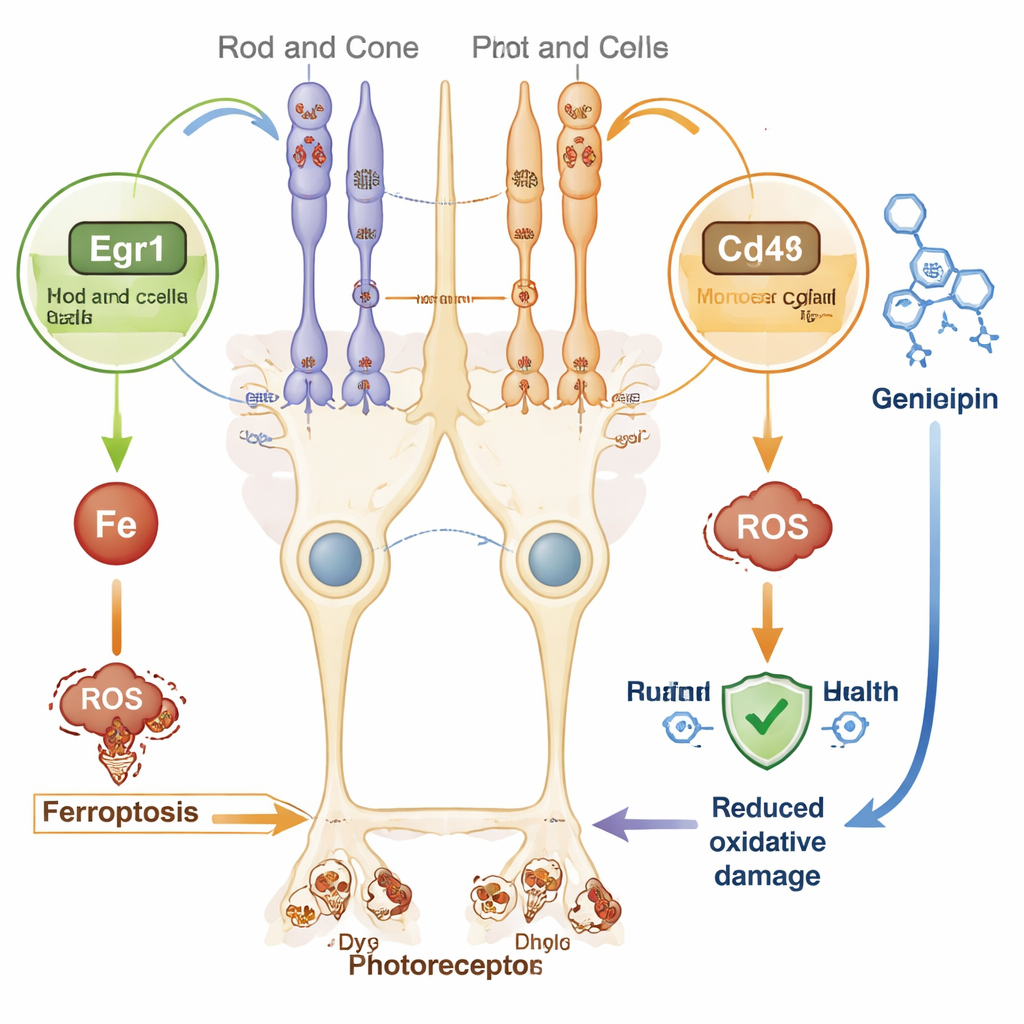
Wat dit betekent voor toekomstige behandelingen
Aangezien gentherapie op maat van elk defect gen complex en duur is, zijn breedwerkende strategieën aantrekkelijk. De nieuw geïdentificeerde genhandtekening wijst op verschillende van zulke wegen. Bijvoorbeeld, Egr1 is een snelwerkende schakelaar die reageert op oxidatieve stress en ferroptose kan bevorderen in andere organen. Cd44, een oppervlaktemolecuul op Müller-cellen, is in verschillende weefsels getoond om ijzerophoping en celdood te verergeren. Tegelijkertijd kan verminderde Ppara, een regulator van vetmetabolisme en energiegebruik, netvliescellen kwetsbaarder maken voor schade. Door deze gedeelde stresspaden aan te pakken, zou het mogelijk kunnen zijn retinale degeneratie te vertragen bij veel verschillende genetische vormen van retinitis pigmentosa.
Geneesmiddelen die het zicht mogelijk kunnen beschermen
Met behulp van een geneesmiddel–gen interactiedatabase zochten de auteurs naar verbindingen die Egr1 of Cd44 zouden kunnen beïnvloeden. Verschillende bestaande moleculen kwamen naar voren, waaronder de natuurlijke verbinding Genipine, die beschermende effecten heeft laten zien in modellen van de ziekte van Parkinson, zenuwdegeneratie en diabetische retinopathie door oxidatieve stress en ontsteking te dempen. Hoewel geen van deze kandidaat-geneesmiddelen nog in dit specifieke muismodel van retinitis pigmentosa is getest, bieden ze veelbelovende beginpunten voor toekomstige laboratorium- en dierstudies gericht op het beschermen van fotoreceptoren tegen ferroptose.
Belangrijkste boodschap voor niet-specialisten
Dit werk toont aan dat ijzer-gedreven, oxiderende celdood nauw verweven is met de veranderingen in genactiviteit die worden gezien in een klassiek model van erfelijke blindheid. Door acht sleutelgenen te onderscheiden, en in het bijzonder het stressgevoelige Egr1 in fotoreceptoren en Cd44 in Müller-cellen, tekent de studie nieuw terrein uit voor potentiële therapieën die niet afhankelijk zijn van het herstellen van één gemuteerd gen. Als toekomstige experimenten bevestigen dat het temperen van ferroptose via deze targets netvliscellen kan behouden, zou dat de deur kunnen openen naar behandelingen die een brede groep patiënten met progressief gezichtsverlies ten goede komen.
Bronvermelding: Qiu, X., Fu, XW., Lei, XL. et al. Identification and validation of a novel ferroptosis-related gene signature associated with inherited retinal degeneration in Rd10 mice. Sci Rep 16, 6992 (2026). https://doi.org/10.1038/s41598-026-38193-4
Trefwoorden: retinitis pigmentosa, ferroptose, fotoreceptoren, retinale degeneratie, Egr1 Cd44