Clear Sky Science · nl
Geïntegreerde metabolomica en 16S rRNA-sequencing onthullen het werkingsmechanisme van totale flavonen van Abelmoschus manihot (L.) Medic tegen leverfibrose
Bloemenkracht voor een geschonden lever
Levernarigheid, of fibrose, is een stille bedreiging die langzaam kan leiden tot cirrose en leverfalen. De moderne geneeskunde heeft nog steeds geen veilige, breedwerkende middelen om dit proces te stoppen of om te keren. Deze studie onderzoekt of natuurlijke verbindingen uit de felgele bloemen van Abelmoschus manihot — een traditioneel Chinees medicinale plant die al voor nierziekten wordt gebruikt — de lever kunnen beschermen tegen langdurige toxische schade, en hoe ze dat mogelijk doen door zowel in te grijpen op de chemie van het lichaam als op de microben in onze darmen.
Een groeiend wereldwijd leverprobleem
Honderden miljoenen mensen wereldwijd leven met chronische leverziekten veroorzaakt door virussen, alcohol, vetophoping of toxines. Wanneer de lever herhaaldelijk wordt beschadigd, reageert ze door littekenweefsel aan te leggen, vergelijkbaar met een wond die nooit volledig geneest. Na verloop van tijd kan deze fibrose het orgaan verharder, de bloedstroom belemmeren en doorgroeien naar cirrose, een belangrijke oorzaak van levergerelateerde sterfgevallen. Omdat veel verschillende triggers tegelijk deze schade kunnen veroorzaken, zijn onderzoekers vooral geïnteresseerd in plantaardige mengsels die op meerdere doelwitten tegelijk kunnen werken, in plaats van enkelvoudige moleculen die slechts één pad beïnvloeden.
Een traditioneel middel testen bij muizen
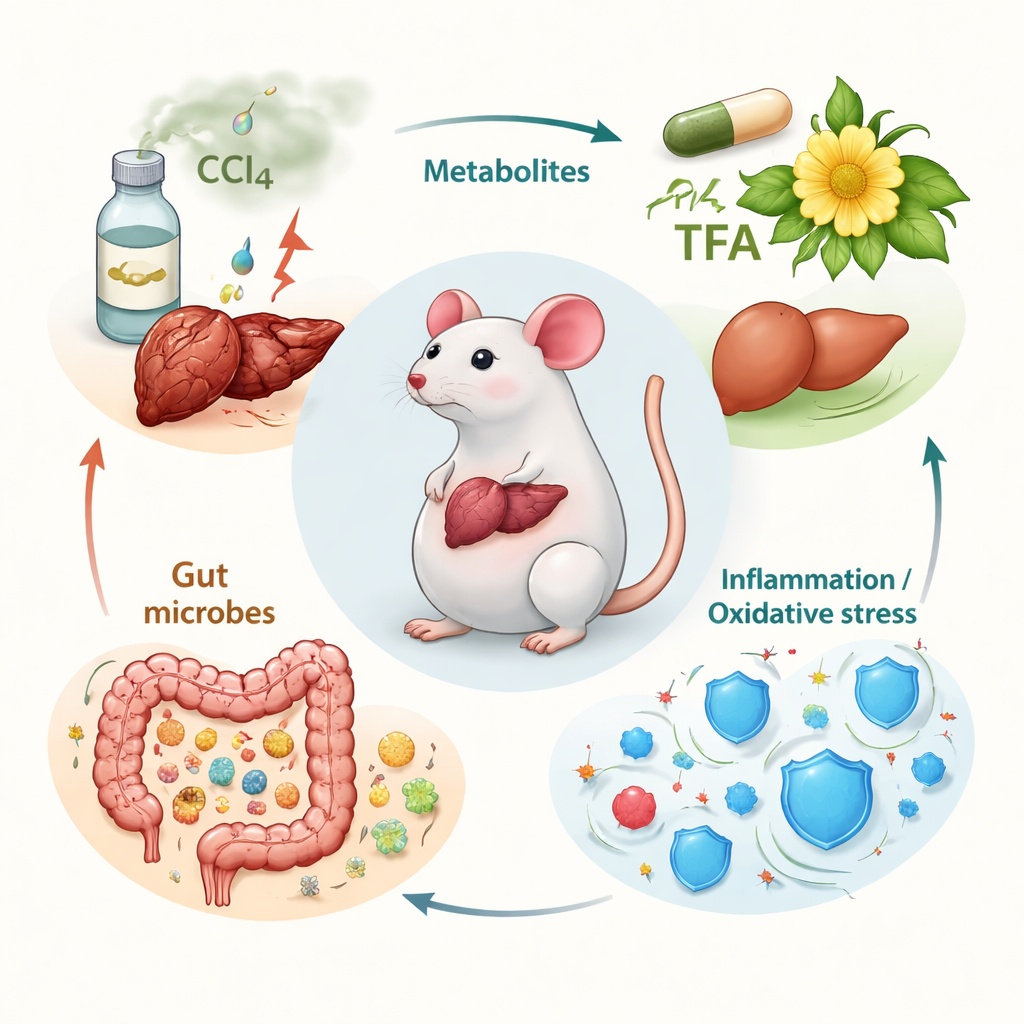
Het team richtte zich op de “totale flavonen” van Abelmoschus manihot (TFA) — een geconcentreerd mengsel van zeven verwante plantaardige verbindingen waarvan eerder is aangetoond dat ze ontstekingsremmend en antioxidant zijn. Ze gebruikten een goed ingeburgerd muismodel waarbij herhaalde blootstelling aan het industriële chemische tetrachloormethaan (CCl4) chronische leverbeschadiging en littekenvorming veroorzaakt die vergelijkbaar is met menselijke fibrose. Mannelijke muizen werden verdeeld in groepen: gezonde controles, CCl4-beschadigde ‘model’-muizen, een standaard medicijngroep en drie TFA-dosisklassen. Na weken van CCl4-blootstelling behandelden de onderzoekers de dieren mondeling met TFA en onderzochten daarna hun bloed, leverweefsel en darminhoud.
Schonere bloedwaarden en gezonder leverweefsel
TFA toonde duidelijke beschermende effecten. De bloedwaarden van leverenzymen ALT en AST — klinische indicatoren van leverschade — stegen sterk bij muizen die aan CCl4 werden blootgesteld, maar daalden met ongeveer de helft bij dieren die TFA kregen. Microscopisch onderzoek bevestigde dit beeld: onbehandelde fibrotische leveren vertoonden verstoorde architectuur, dode cellen, zware collageenafzettingen en inflatoire celophopingen. TFA-behandelde leveren hadden minder litteken-‘pseudolobuli’, minder collageenkleuring en verminderde tekenen van celdood. Markers van oxidatieve stress verbeterden ook: antioxidatieve verdedigingen (SOD en GSH-Px) namen toe, terwijl schadelijke bijproducten (MDA) daalden. Belangrijke ontstekingssignalen, waaronder TNF-α, IL-6 en TGF-β1, werden eveneens verlaagd, samen met chemische markers van fibrose zoals hydroxyproline, collageen IV en hyaluronzuur.
Het herstellen van de chemie van het lichaam en darmmicroben
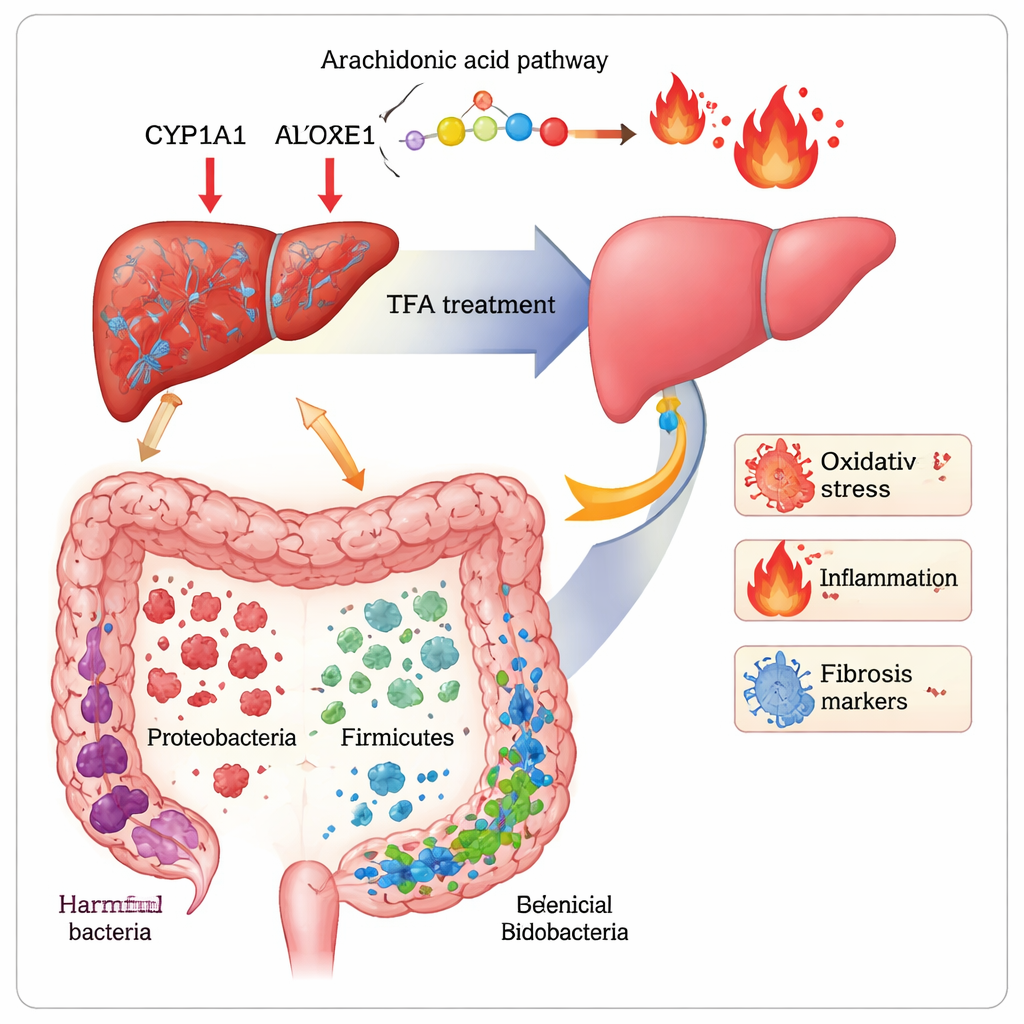
Om te achterhalen hoe TFA deze voordelen teweegbrengt, combineerden de onderzoekers twee krachtige instrumenten: metabolomica, waarmee honderden kleine moleculen in het bloed worden geprofileerd, en 16S rRNA-sequencing, waarmee de soorten bacteriën in de darm in kaart worden gebracht. Bij fibrotische muizen waren tientallen metabolieten die betrokken zijn bij vetverwerking en de afbraak van aminozuren verstoord. TFA herstelde gedeeltelijk het evenwicht in routes die verband houden met celmembranen (glycerofosfolipiden), het met stemming geassocieerde aminozuur tryptofaan, en een vetzuur genaamd arachidonzuur dat ontstekingssignalen voedt. De niveaus van twee arachidonzuurproducten, 20-HETE en 16(R)-HETE — beide gekoppeld aan oxidatieve stress en fibrose — werden teruggeduwd richting normaal. In de lever verlaagde TFA de hoeveelheid van drie enzymen (CYP1A1, CYP2E1, ALOX15) die helpen bij de productie van deze schadelijke moleculen. Tegelijkertijd verstoorde CCl4 het darmmicrobioom, met een afname van gunstige groepen zoals Firmicutes, Lactobacillus en Bifidobacterium en een toename van potentieel schadelijke Proteobacteria. TFA keerde een groot deel van deze verschuiving om, verhoogde de diversiteit en herstelde ‘vriendelijke’ bacteriën die geassocieerd zijn met betere barrièrefunctie en minder ontsteking.
Een multitargetstrategie op de darm‑leveras
Door bacteriële veranderingen te koppelen aan bloedchemie en ziektemarkers, suggereert de studie dat TFA werkt langs de “darm‑leveras” — de drukke snelweg van signalen, voedingsstoffen en toxines die van de darm naar de lever reizen. Schadelijke bacteriën en hun producten lijken samen te hangen met hogere ontsteking en littekenvorming, terwijl gunstige microben correleren met gezondere metabole profielen en minder fibrose. TFA lijkt dit hele systeem weer naar evenwicht te duwen: het versterkt antioxidatieve verdedigingen, dempt ontstekingsroutes aangedreven door arachidonzuur, herschikt de microbiegemeenschap in de darm en verzacht uiteindelijk de littekenrespons in de lever.
Wat dit kan betekenen voor toekomstige behandelingen
Voor niet‑specialisten is de kernboodschap dat een bloemenextract dat al lang in de traditionele geneeskunde wordt gebruikt, echte belofte liet zien in een moderne, rigoureuze test van chronische leverscharring. Bij muizen deed TFA meer dan alleen levercellen beschermen — het zette ook toxische chemie en schadelijke darmmicroben terug naar een meer gunstige toestand. Hoewel deze resultaten nog niet bewijzen dat er voordeel is bij mensen, en alleen zijn verkregen in mannelijke dieren bij één type leverbeschadiging, benadrukken ze een potentiële multitargettherapie die samenwerkt met de netwerken van het lichaam in plaats van zich te richten op één enkel molecuul. Met verder onderzoek zouden zulke plantafgeleide flavonen op een dag onderdeel kunnen worden van een bredere gereedschapskist om leverfibrose te vertragen of zelfs om te keren.
Bronvermelding: Li, D., Ge, H., Zhang, Y. et al. Integrated metabolomics and 16S rRNA sequencing reveal the mechanism of total flavones of Abelmoschus manihot (L.) Medic against liver fibrosis. Sci Rep 16, 7342 (2026). https://doi.org/10.1038/s41598-026-38192-5
Trefwoorden: leverfibrose, darmmicrobioom, metabolomica, flavonoïden, traditionele Chinese geneeskunde