Clear Sky Science · nl
RNA-sequencing onthult differentiële expressie van circulaire RNA's bij menselijk kleincellig longkanker
Waarom kleine RNA-lussen de zorg voor longkanker kunnen veranderen
Kleincellig longkanker is een van de dodelijkste vormen van kanker: het verspreidt zich snel en is vaak resistent tegen chemotherapie. Artsen hebben nog steeds geen goede tests om het vroeg op te sporen of om te voorspellen wie op behandeling zal reageren. Deze studie onderzoekt een ongewone klasse genetische moleculen, circulaire RNA’s—kleine RNA-lussen die verrassend stabiel zijn in onze cellen—om te bepalen of ze bijdragen aan deze agressieve kanker en of ze als nieuwe, betrouwbaardere biomarkers kunnen dienen.
De meest agressieve longkanker begrijpen
Kleincellig longkanker (SCLC) vormt slechts ongeveer één op de vijf longkankergevallen, maar veroorzaakt een onevenredig groot deel van de sterfgevallen omdat het snel groeit, vroeg uitzaait en meestal terugkeert na chemotherapie. De meeste patiënten worden in een gevorderd stadium gediagnosticeerd, wanneer chirurgie geen optie is en weefselmonsters schaars zijn. Hoewel onderzoekers veel DNA-mutaties in SCLC in kaart hebben gebracht, weten ze veel minder over hoe niet-coderende RNA’s—moleculen die geen eiwitten maken maar toch sterk het celd gedrag beïnvloeden—de ziekte vormen. Circulaire RNA’s (circRNA’s) zijn een bijzonder intrigerende groep, omdat hun gesloten lusstructuur ze resistenter maakt tegen afbraak dan gewone RNA’s, wat de hoop wekt dat ze betrouwbaar te meten zijn in weefsel of zelfs in bloed.
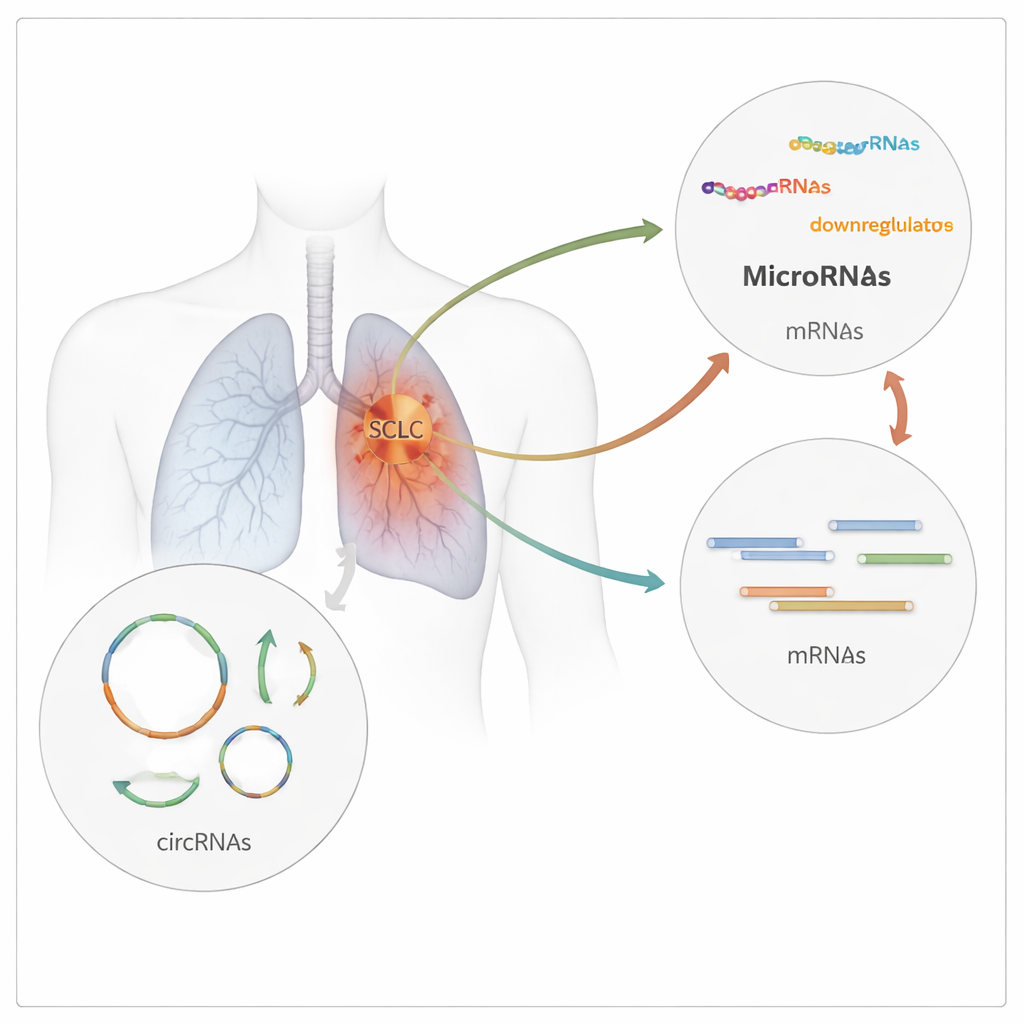
Op zoek naar RNA-lussen in tumorweefsel
Het onderzoeksteam in India verzamelde tumorbiopten van patiënten met pas gediagnosticeerde SCLC en vergeleek deze met normaal longweefsel van personen die een operatie kregen voor vroegstadium niet-kleincellige longkanker. Met behulp van hoogdoorvoer-RNA-sequencing scanden ze meer dan 26.000 juncties waar circulaire RNA’s gevormd kunnen worden, en filtreerden en analyseerden ze de gegevens om vast te stellen welke circRNA’s echt verschillend waren tussen kanker- en niet-kankermonsters. Ze vonden 23 circulaire RNA’s waarvan de activiteit significant veranderde in SCLC: 13 waren meer abundant en 10 minder abundant in tumoren dan in normaal longweefsel. Deze moleculen waren afkomstig van 21 verschillende genen, wat wijst op een brede herschikking van RNA-regulatie in SCLC.
Een driedelig RNA-regulatienetwerk bouwen
Circulaire RNA’s fungeren vaak als moleculaire sponsen: ze binden microRNA’s—korte RNA-fragmenten die normaal specifieke genen onderdrukken. Om dit regelnetwerk in kaart te brengen, gebruikten de onderzoekers openbare databases om te voorspellen welke microRNA’s aan elk van de 23 veranderde circRNA’s konden binden en welke genen die microRNA’s waarschijnlijk reguleren. Het resultaat was een dicht driedelig web dat 23 circulaire RNA’s koppelt aan 241 microRNA’s en ongeveer 7.800 eiwitcoderende genen. Toen ze onderzochten wat deze genen doen, clusterden veel ervan rond celcycluscontrole, eiwitafbraak, stressreacties en bekende kankerpaden zoals p53, MAPK, Hippo en cellulaire veroudering. Met andere woorden: de verkeerd gereguleerde RNA-lussen lijken op kruispunten te zitten van sleutelroutes voor groei en overleving in SCLC-cellen.
Twee opvallende RNA-lussen met diagnostische belofte
Van alle veranderde circRNA’s staken er twee met kop en schouders bovenuit. Eén, circLIFR genoemd, was consequent verlaagd in SCLC-weefsel en in meerdere SCLC-celijnen vergeleken met normale longcellen. Zijn partner-microRNA’s, waaronder miR-1234-3p en miR-375-3p, waren sterk verhoogd, wat past bij het idee dat het verlies van de circRNA-spons meer vrije microRNA’s overlaat om kankergelinkte genen te beïnvloeden. De andere lus, circCAMSAP1, vertoonde het omgekeerde patroon: die was verhoogd in tumoren, terwijl een van zijn gerapporteerde microRNA-partners, miR-145-5p, scherp verlaagd was. Patiënten van wie de kanker verslechterde ondanks eerstelijnschemotherapie hadden doorgaans hogere circCAMSAP1-niveaus, wat wijst op een verband met behandelingsresistentie. Toen het team testte hoe goed deze moleculen SCLC-weefsel onderscheiden van normaal longweefsel, presteerde circLIFR bijzonder goed met een nauwkeurigheidsmaat (AUC) boven 0,9, terwijl circCAMSAP1 en de bijbehorende microRNA’s matige maar nog steeds nuttige diagnostische kracht lieten zien.
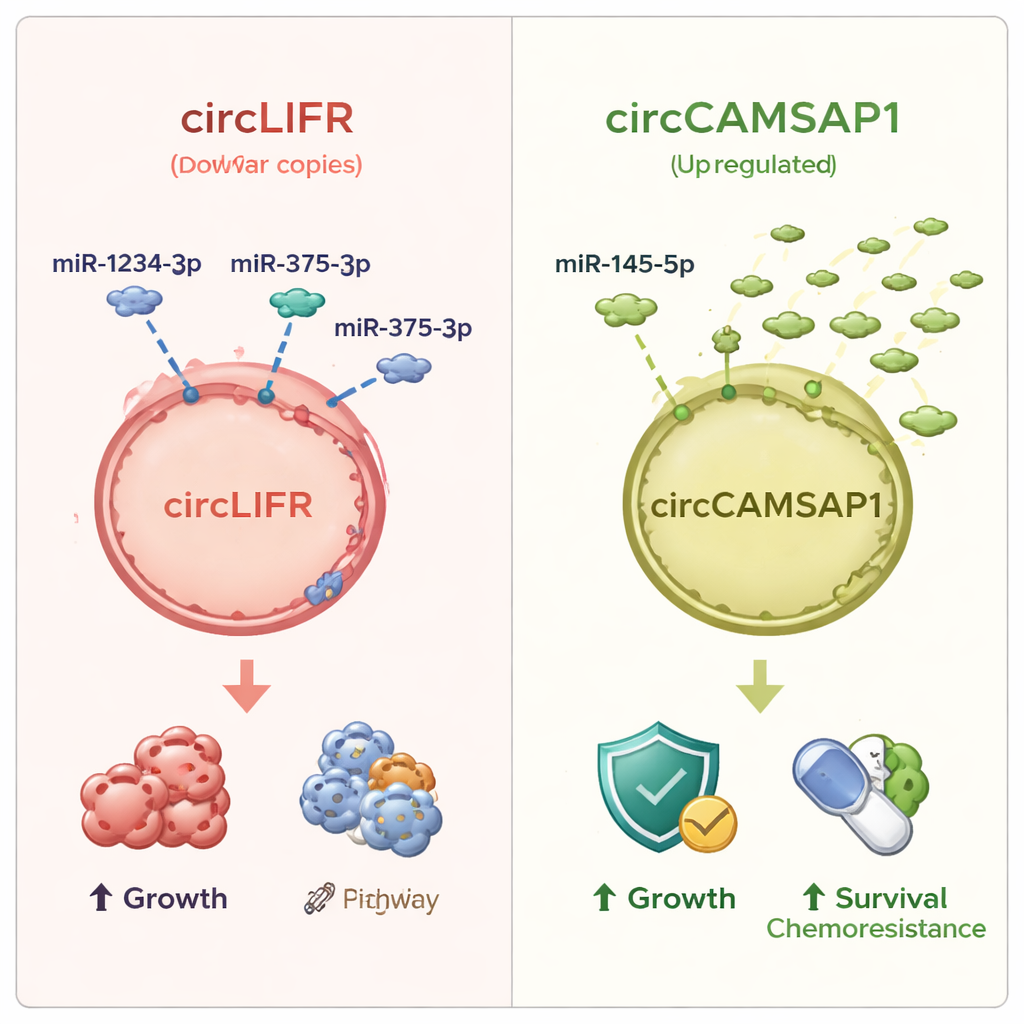
Wat dit voor patiënten kan betekenen
De conclusie voor een lezer zonder specialistische achtergrond is dat deze studie een nieuwe regellaag in kleincellig longkanker onthult—gebouwd uit kleine RNA-lussen en hun partners—die helpt te reguleren hoe snel tumorcellen groeien, hoe ze op stress reageren en mogelijk hoe ze chemotherapie verdragen. Twee specifieke circulaire RNA’s, circLIFR en circCAMSAP1, komen naar voren als bijzonder veelbelovende markers: de één gaat meestal verloren in tumoren, de ander neemt toe, en samen met hun geassocieerde microRNA’s kunnen ze helpen onderscheid te maken tussen kankercellen en normaal weefsel en aanwijzingen geven over hoe de ziekte van een patiënt op behandeling zal reageren. Hoewel deze bevindingen nog labexperimenten vereisen om oorzaak en gevolg aan te tonen en grotere klinische studies om de praktische bruikbaarheid te testen, wijzen ze op toekomstige bloed- of weefseltesten gebaseerd op circulaire RNA’s die de diagnose en het beheer van een van de meest uitdagende vormen van longkanker kunnen verbeteren.
Bronvermelding: Saxena, V., Abhilash, D., Budhraja, A. et al. RNA sequencing reveals differential expression of circular RNAs in human small cell lung cancer. Sci Rep 16, 7134 (2026). https://doi.org/10.1038/s41598-026-38145-y
Trefwoorden: kleincellig longkanker, circulair RNA, microRNA, kanker-biomarkers, RNA-sequencing