Clear Sky Science · nl
Remming van CDK2 bevordert neuronale differentiatie bij neuroblastoom
Waarom deze kinderkankerstudie ertoe doet
Neuroblastoom is een van de meest voorkomende solide tumoren bij jonge kinderen en blijft voor veel hoogrisicopatiënten dodelijk ondanks intensieve behandelingen. Deze studie onderzoekt een nieuwe benadering van de ziekte: in plaats van alleen te proberen kankercellen te doden, vraagt men of we ze kunnen aanzetten om op te groeien tot onschadelijke, zenuwachtige cellen. Het werk richt zich op een eiwit genaamd CDK2 en laat zien dat het blokkeren daarvan zowel de tumorgroei kan vertragen als de kankercellen kan aanmoedigen te rijpen, wat de weg opent naar zachtere, meer gerichte therapieën.
Een probleemveroorzakend eiwit in agressieve tumoren
De onderzoekers begonnen met het analyseren van meerdere grote verzamelingen tumormonsters van kinderen met neuroblastoom. Ze stelden een eenvoudige vraag: wanneer is het CDK2-gen het meest actief? Het antwoord was opvallend. Tumoren met de hoogste CDK2-niveaus bleken vaak gevorderd van stadium, geclassificeerd als hoog risico, en hadden meer kans terug te keren na behandeling. Kinderen van wie de tumor veel CDK2 vertoonde, deden het over het algemeen slechter na verloop van tijd. Deze kankers droegen vaak extra kopieën van een ander krachtig kankergen, MYCN, en zagen er onder de microscoop primitiever uit en minder als normale zenuwcellen. Samen suggereerden deze patronen dat CDK2 nauw verbonden is met de gevaarlijkste vormen van de ziekte.
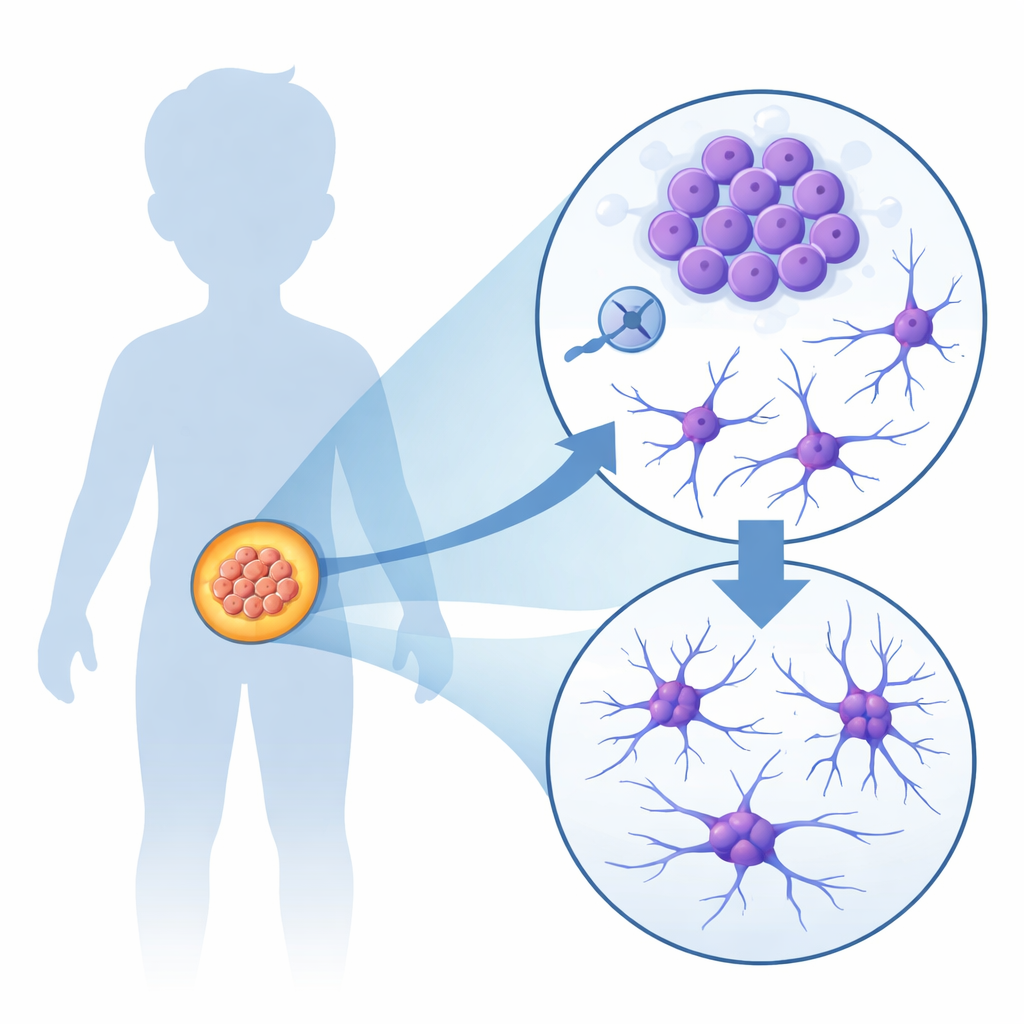
Van snel delende cellen naar zenuwachtige uitlopers
Om te begrijpen wat CDK2 daadwerkelijk doet in tumorcellen, gebruikte het team menselijke neuroblastoomcelijnen die in het laboratorium werden gekweekt. Ze schakelden ofwel het CDK2-gen uit, of blokkeerden het CDK2-eiwit met medicijnachtige moleculen. In beide gevallen gebeurde iets opmerkelijks: in plaats van zich eindeloos te delen zoals kankercellen gewoonlijk doen, begonnen veel cellen lange, dunne uitlopers te vormen die lijken op de vertakkingen van zich ontwikkelende zenuwcellen. Genen die geassocieerd zijn met zenuwgroei en communicatie werden aangezet, terwijl genen die samenhangen met celdeling en DNA‑herstel werden geremd. Deze veranderingen waren het sterkst in cellen met extra MYCN, het subtype dat de meest agressieve ziekte bij kinderen veroorzaakt.
CDK2 en MYCN: een versterkende lus
Dieper graven leverde de bevinding op dat CDK2 en MYCN in een feedbacklus met elkaar verbonden zijn. MYCN bindt rechtstreeks aan het DNA nabij het CDK2-gen en verhoogt de activiteit ervan, waardoor de CDK2-niveaus in tumorcellen hoog blijven. Wanneer MYCN werd verminderd, daalden ook de CDK2-niveaus. Op hun beurt verzwakte het verlies van CDK2 het bredere MYC‑signaleringsprogramma dat snelle groei aanstuurt. Dit betekent dat in veel hoogrisicotumoren MYCN en CDK2 samenwerken om cellen in een snel delende, onrijpe staat te houden en hun natuurlijke neiging tot rijping in zenuwcellen te blokkeren.
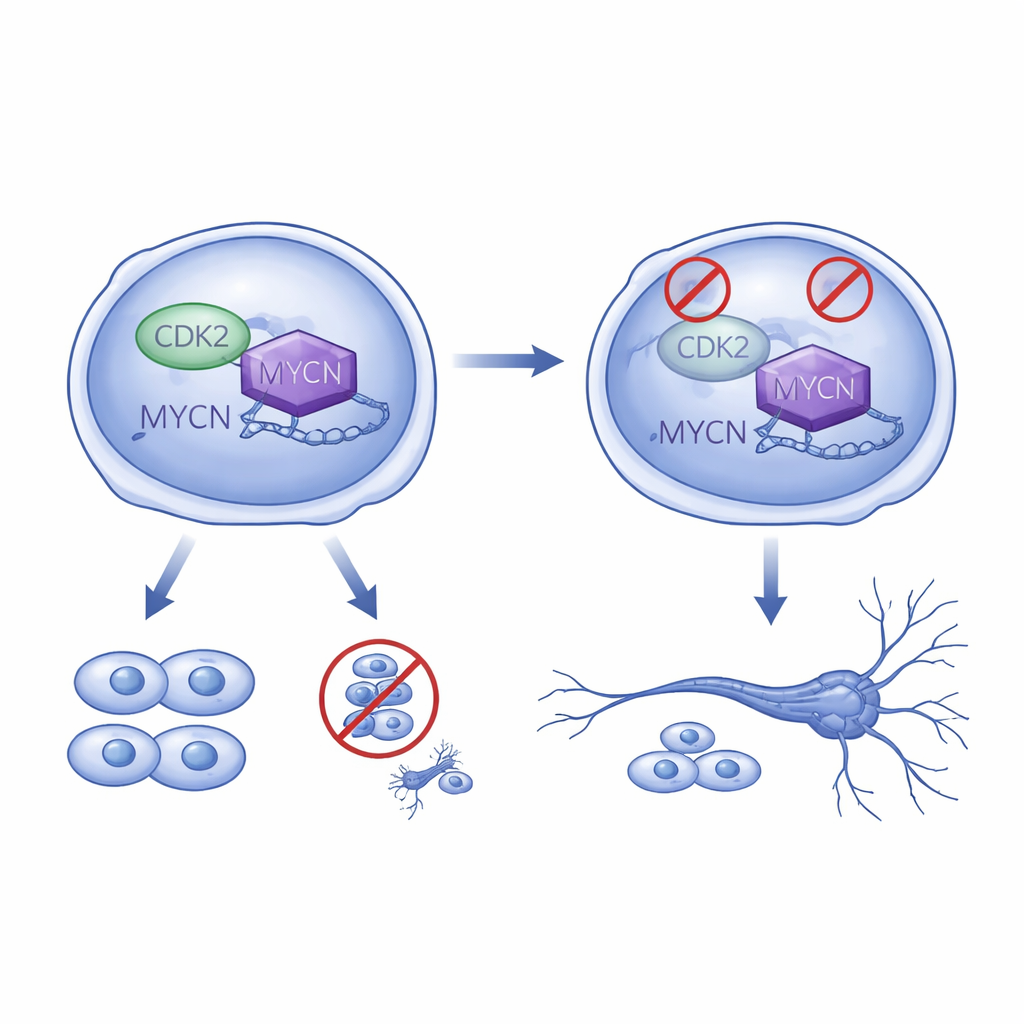
Huidige behandelingen versterken door cellen te laten rijpen
Aangezien CDK2 en MYCN samenwerken, testten de onderzoekers combinaties van CDK2-blokkerende middelen met experimentele verbindingen die op MYC richten. In verschillende neuroblastoomcelmodellen verminderden deze combinetherapieën de overleving van cellen meer dan elk middel afzonderlijk en veroorzaakten ze vaak meer zenuwachtige uitlopers, wat op sterkere differentiatie wijst. Ze combineerden ook CDK2-remming met all‑trans‑retineïnezuur (ATRA), een vitamine A‑verwant medicijn dat al wordt gebruikt om neuroblastoomcellen te helpen rijpen na chemotherapie. In kweekschalen gaf de combinatie van CDK2‑blokkers en ATRA hogere "differentiatiescores"—langere uitlopers en sterkere zenuwmarkers—dan enkelvoudige behandelingen, wat wijst op een mogelijke manier om een bestaande standaardtherapie te verbeteren.
Wat dit zou kunnen betekenen voor kinderen met neuroblastoom
In eenvoudige bewoordingen toont deze studie dat hoge CDK2-niveaus met name agressieve, onrijpe neuroblastoomtumoren kenmerken, en dat het verlagen van CDK2-activiteit kankercellen kan aansporen zich meer als normale zenuwcellen te gedragen en soms te sterven. Omdat CDK2 is ingebed in hetzelfde groeinetwerk als MYCN, kan het tegelijk aanpakken van beide—of het combineren van CDK2‑blokkers met retinoïde medicijnen zoals ATRA—op termijn een effectievere, op differentiatie gerichte behandelingsstrategie opleveren. Hoewel deze bevindingen nog in celkweekstadia verkeren en zorgvuldig getest moeten worden in diermodellen en klinische proeven, schetsen ze een veelbelovende route naar therapieën die niet alleen tumorcellen aanvallen, maar ze aansporen op te groeien en tot rust te komen.
Bronvermelding: Alzrigat, M., Mahmoud, L., Topçu, A.N. et al. CDK2 inhibition promotes neuronal differentiation in neuroblastoma. Sci Rep 16, 5255 (2026). https://doi.org/10.1038/s41598-026-38123-4
Trefwoorden: neuroblastoom, CDK2-remming, neurale differentiatie, MYCN, retinoïde therapie