Clear Sky Science · nl
Bovin serumalbumine-nanodeeltjes verbeteren de stabiliteit van bacteriofagen en de antimicrobiële werking tegen Pseudomonas aeruginosa
Waarom het beschermen van nuttige virussen ertoe doet
Naarmate antibioticaresistentie toeneemt, raken artsen zonder opties om gevaarlijke infecties te behandelen. Een hardnekkige boosdoener is Pseudomonas aeruginosa, een bacterie die vaak de longen infecteert bij mensen met verminderde afweer en die tegen veel middelen bestand is. Deze studie onderzoekt een creatieve strategie: het gebruik van behulpzame virussen die bacteriën aanvallen, bacteriofagen genoemd, en het beschermen daarvan in piepkleine eiwitbolletjes gemaakt van een veelvoorkomend bloedeiwit, bovien serumalbumine (BSA). Het doel is deze virussen stabiel en actief genoeg te houden om hardnekkige longinfecties beter te bestrijden.
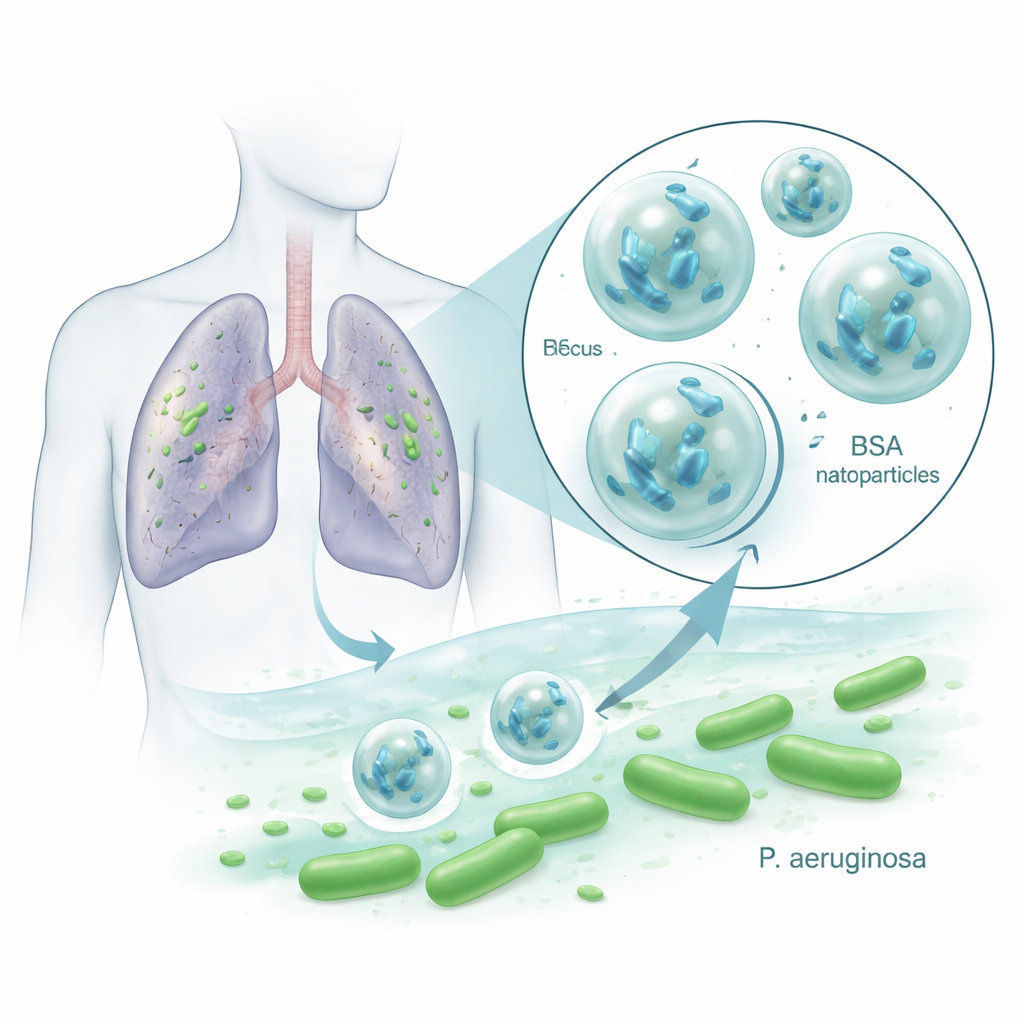
Miniatuurlijke bondgenoten tegen hardnekkige longkiemen
Pseudomonas aeruginosa is berucht in ziekenhuizen omdat het meerdere antibiotica kan weerstaan en slijmerige biofilms vormt die het tegen behandeling afschermen. Bacteriofagen, of fagen, zijn virussen die specifieke bacteriën infecteren en doen barsten, terwijl menselijke cellen en nuttige microben grotendeels ongemoeid worden gelaten. Ze kunnen zich vermenigvuldigen waar hun bacteriële gastheer aanwezig is, wat ze een aantrekkelijke aanvulling of alternatief voor antibiotica maakt. Maar fagen zijn kwetsbaar: hitte, zuurheid, enzymen en het immuunsysteem kunnen ze snel inactiveren, wat hun succes bij echte patiënten heeft beperkt. De onderzoekers vroegen zich af of het verpakken van een Pseudomonas-dodende fag genaamd VAC1 in BSA-nanodeeltjes deze kon beschermen en de behandeling effectiever kon maken.
Het bouwen van een beschermend eiwitomhulsel
Het team moest eerst een deeltje ontwerpen dat de fag niet zou beschadigen. Ze testten gangbare oplosmiddelen die gebruikt worden om BSA-nanodeeltjes te vormen en ontdekten dat ethanol en methanol VAC1 vernietigden, terwijl aceton dat niet deed; daarom gebruikten ze aceton in hun proces. Ze mengden de fag met een BSA-oplossing en voegden vervolgens voorzichtig aceton toe om het eiwit tot nanoschaalbolletjes te laten samenklonteren, en stabiliseerden deze met een crosslinkend reagens. Deze fag-beladen deeltjes, NPPha genoemd, hadden gemiddeld een diameter van ongeveer 220 nanometer—veel kleiner dan een menselijke cel—en vingen meer dan 95% van de fag in. Elektronenmicroscoopbeelden toonden onregelmatig gevormde BSA-deeltjes met dichtere regio’s die waarschijnlijk overeenkomen met fag, en tests bevestigden dat actieve virussen gedurende minstens twee dagen bij lichaamstemperatuur langzaam vrijkwamen zonder infectiviteit te verliezen.
Krachtiger bacteriedodende werking in het lab
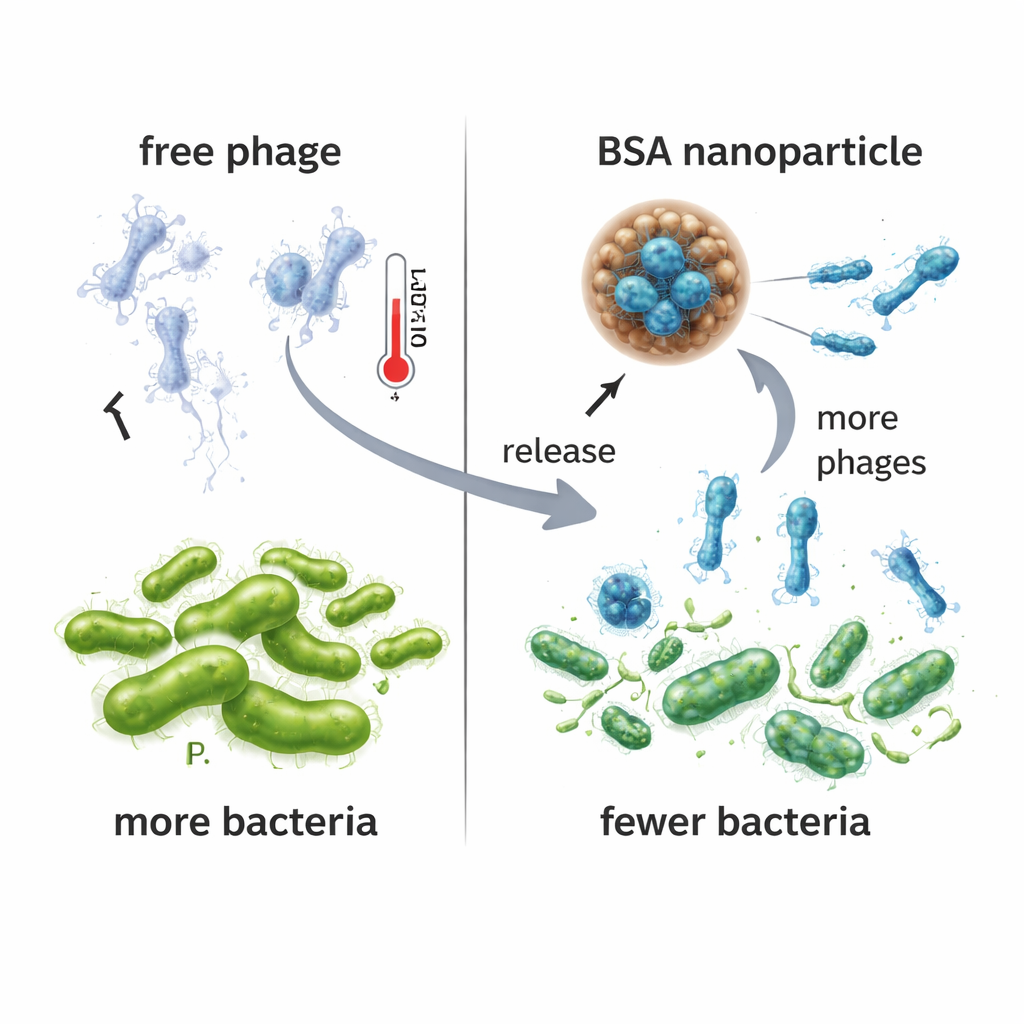
De onderzoekers vergeleken vervolgens hoe goed vrije VAC1 en NPPha Pseudomonas in vloeibare kweek controleerden. Wanneer bacteriën werden blootgesteld aan NPPha, werd hun groei veel sterker onderdrukt dan bij dezelfde hoeveelheid fag alleen of met lege nanodeeltjes. Over 24 uur produceerden culturen behandeld met NPPha ongeveer honderdduizend keer meer nieuwe fagdeeltjes dan culturen behandeld met vrije VAC1, wat suggereert dat de gestage afgifte vanuit de nanodeeltjes zorgde voor een meer aanhoudende virus–bacterieconfrontatie. Belangrijk is dat de BSA-nanodeeltjes—gevuld met fag of leeg—menselijke leverafgeleide cellen niet schaadden in toxiciteitstesten, wat hun potentiële veiligheid als afleveringsmiddel ondersteunt. Stabiliteitsexperimenten bij 37 °C toonden dat vrije fag snel activiteit verloren binnen twee dagen, terwijl fag ingebed in NPPha tot vijf dagen infectieus bleven.
De aanpak testen in geïnfecteerde muizen
Om te onderzoeken of deze voordelen zich in levende dieren vertaalden, gebruikte het team een muismodel van acute Pseudomonas-longinfectie. Muizen werden via de neus geïnfecteerd en kregen een uur later behandeld met NPPha, vrije VAC1, lege nanodeeltjes of een zoutoplossing. In dit zeer ernstige model overleden alle dieren, ongeacht behandeling, binnen 12 uur, dus de overleving verbeterde niet. Echter, bij inspectie van de longen bleek dat muizen die NPPha kregen minder bacteriën hadden en vaker nog detecteerbare fagen huisvestten dan die behandeld met vrije VAC1. Weefselplakken van longen behandeld met NPPha toonden minder structurele schade, dunnere wanden tussen luchtzakjes en verminderde ophoping van ontstekingscellen vergeleken met andere geïnfecteerde groepen, wat aangeeft dat de infectie enigszins werd afgezwakt, ook al was dat niet voldoende om de dieren onder deze zware omstandigheden te redden.
Wat dit betekent voor toekomstige infectiebehandelingen
Voor niet-specialisten is de belangrijkste boodschap dat het verpakken van bacteriofagen in kleine eiwitgebaseerde belletjes ze langer levend en krachtig kan houden, waardoor ze beter in staat zijn hardnekkige bacteriën zoals Pseudomonas aeruginosa aan te vallen. In kweekschalen en in muizenlongen verhoogden BSA-nanodeeltjes het aantal fagen, verminderden ze bacteriële groei en beperkten ze longschade, hoewel ze in dit agressieve infectiemodel nog geen sterfte konden voorkomen. Het werk suggereert dat albumine-nanodeeltjes een eenvoudige, goedkope en ogenschijnlijk veilige manier bieden om therapeutische fagen te stabiliseren. Met verfijnde dosering, timing en mogelijk gebruik bij minder extreme of meer chronische infecties zouden dergelijke nano-gepakte fagen een waardevol hulpmiddel naast antibiotica kunnen worden in de strijd tegen multiresistente bacteriën.
Bronvermelding: Cunha, G.A.d., Marangoni, G.S., Durante, M.F.R. et al. Bovine serum albumin nanoparticles improve bacteriophage stability and antimicrobial activity against Pseudomonas aeruginosa. Sci Rep 16, 7146 (2026). https://doi.org/10.1038/s41598-026-38106-5
Trefwoorden: fagetherapie, nanodeeltjes, Pseudomonas aeruginosa, antibioticaresistentie, longinfectie