Clear Sky Science · nl
Obinutuzumab induceert lysosomale destabilisatie via sfingomyeline-afhankelijke remming van TRPML2
Waarom dit antilichaamverhaal ertoe doet
Voor veel mensen met B-cellymfomen hebben moderne antilichaamtherapieën van een ooit consequent dodelijke diagnose een behandelbare ziekte gemaakt. Toch zijn niet alle antilichamen gelijk: sommige doden kankercellen krachtiger en betrouwbaarder dan andere. Dit artikel onderzoekt waarom één van die middelen, obinutuzumab, beter is in het rechtstreeks doden van lymfomacellen dan zijn voorganger rituximab, door in te zoomen op een onverwachte boosdoener diep in de cel — de eigen recyclingcentra van de cel, de lysosomen, en een precair evenwicht van vetten en ionkanalen in hun membranen.
Van oppervlaktedoel naar interne zelfvernietiging
Zowel rituximab als obinutuzumab herkennen hetzelfde doelwit op B-cellen, een eiwit genaamd CD20. De auteurs tonen echter aan dat obinutuzumab veel sneller en efficiënter in de cel wordt opgenomen. Zodra het aan CD20 op het celoppervlak van de kankercel gebonden is, worden de antilichaam–receptorcomplexen via endocytose naar zure compartimenten, waaronder lysosomen, getransporteerd. Daar veroorzaakt obinutuzumab permeabilisatie van het lysosomale membraan: het normaal robuuste lysosomale membraan wordt lekkend, waardoor verteerbare enzymen zoals cathepsines in de cel lekken en celdoodroutes activeren. Veranderingen in de zout- en waterbalans van deze compartimenten, die lysosomen doen opzwellen, bleken dit dodelijke effect sterk te versterken.
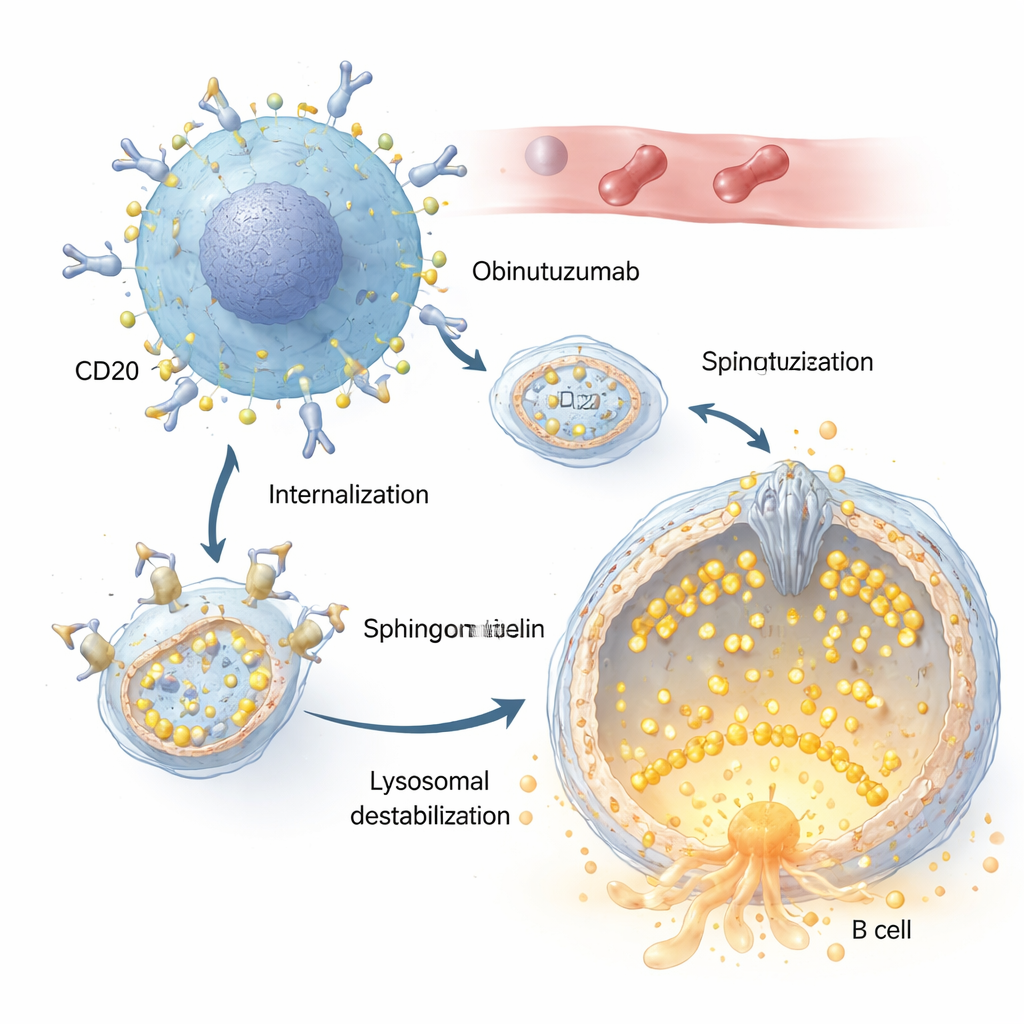
De rol van een piepklein poortwachterkanaal
Centraal in dit verhaal staat TRPML2, een calciumkanaal ingebed in het lysosomale membraan. Onder normale omstandigheden helpt TRPML2 lysosomen om te gaan met mechanische en osmotische stress door calcium vrij te geven, wat membraanherstel, verkeer en volumeregulatie ondersteunt. Met behulp van fluorescerende calciumsensoren en geconstrueerde calciumwaarnemende versies van TRPML2 laten de onderzoekers zien dat obinutuzumab dit kanaal snel uitschakelt: binnen enkele minuten na behandeling produceert een middel dat normaal TRPML-kanalen opent geen calciumburst meer. Genetische benaderingen die TRPML2-niveaus verlagen, of kleine-molecuulremmers die TRPML-activiteit blokkeren, maken lymfomacellen gevoeliger voor obinutuzumab, wat leidt tot meer lysosomale lekken en hogere percentages directe celdood.
Hoe membraanfetten het evenwicht kantelen
De studie vraagt vervolgens wat de opname van het antilichaam verbindt met het uitschakelen van het kanaal. De aandacht gaat uit naar sfingomyeline, een lipide (vet) die overvloedig aanwezig is in celmembranen en waarvan bekend is dat het TRPML-kanalen verstoort. Met een fluorescerende sfingomyeline-bindende probe vinden de auteurs dat vesikels die obinutuzumab bevatten rijk zijn aan sfingomyeline zodra ze zure compartimenten bereiken, veel meer dan vesikels met rituximab. Wanneer cellen behandeld worden met sfingomyelinase, een enzym dat sfingomyeline afbreekt, wordt de calciumafgifteactiviteit van TRPML2 hersteld, zelfs in aanwezigheid van obinutuzumab. Onder deze omstandigheden zijn lysosomen minder geneigd te lekken en sterven minder cellen, wat er sterk op wijst dat opgehoopte sfingomyeline TRPML2 uitschakelt en lysosomen vatbaar maakt voor ruptuur.
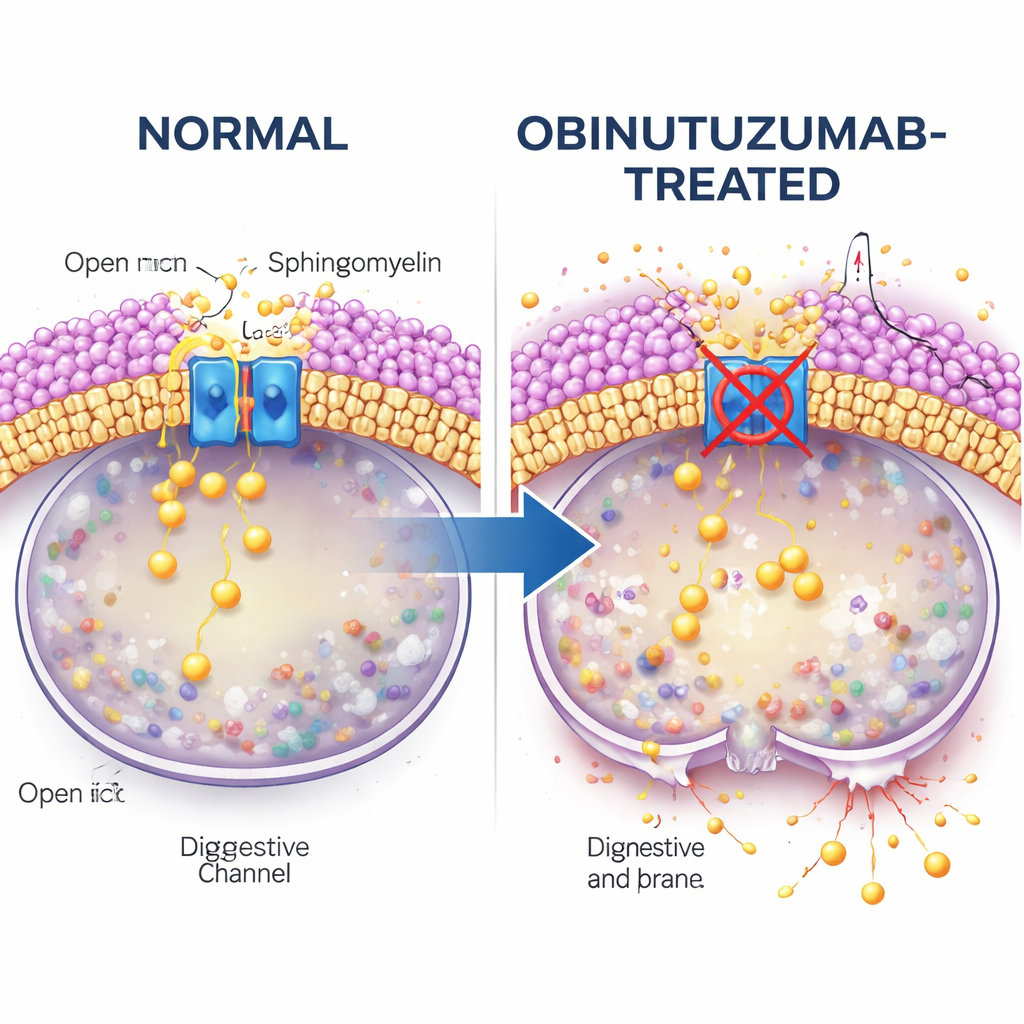
Verkeersroutes en cholesterol-checkpoints
Het pad dat obinutuzumab in de cel volgt, blijkt ook van belang. Elektronenmicroscopie en pH‑gevoelige antilichaamlabels tonen aan dat obinutuzumab het celoppervlak verlaat en sneller intracellulaire vesikels binnengaat dan rituximab. Wanneer de onderzoekers specifieke opnameroutes verstoren, vinden ze dat het blokkeren van een cholesterolafhankelijke vorm van endocytose (met een stof genaamd filipine) voorkomt dat obinutuzumab TRPML2 uitschakelt en gedeeltelijk lysosomale schade en celdood vermindert. Andere endocytose-remmers geven dit beschermende effect niet. Dit wijst op een gespecialiseerde, cholesterol- en sfingomyeline-rijke route die obinutuzumab naar lysosomen brengt op een manier die leidt tot TRPML2-remming en daaropvolgende membraandestabilisatie.
Wat dit betekent voor toekomstige kankerbehandelingen
Simpel gezegd laat dit werk zien dat obinutuzumab B-cellymfomen zo efficiënt doodt omdat het hun lysosomen in een fragiele staat dwingt. Door antilichaam–CD20-complexen naar sfingomyeline-rijke compartimenten te sturen, schakelt het middel indirect een beschermend calciumkanaal, TRPML2, uit. Zodra die beveiliging wegvalt, barsten lysosomen onder stress gemakkelijker, waarbij corrosieve enzymen vrijkomen die de kankercel van binnenuit afbreken. Het begrijpen van deze lipide–ionkanaal-as verklaart niet alleen waarom obinutuzumab beter presteert dan rituximab; het suggereert ook nieuwe strategieën om antilichaamtherapieën te versterken — bijvoorbeeld door ze te combineren met middelen die sphingolipiden veranderen of TRPML2-activiteit verhogen om te sturen hoe en wanneer lysosomen van tumorcellen zelfvernietigen.
Bronvermelding: Oh, J., Jin, N., Kwon, S. et al. Obinutuzumab induces lysosomal destabilization via sphingomyelin-dependent inhibition of TRPML2. Sci Rep 16, 7079 (2026). https://doi.org/10.1038/s41598-026-38087-5
Trefwoorden: obinutuzumab, B-cellymfoom, lysosoom, sfingomyeline, TRPML2