Clear Sky Science · nl
Functionele eigenschappen van extracellulaire blaasjes afkomstig van skeletmyotubes op basis van microRNA-profielen: een vergelijkende analyse met extracellulaire blaasjes van mesenchymale stamcellen
Spierberichten in kleine pakketjes
Onze spieren doen veel meer dan ons voortbewegen — ze sturen voortdurend moleculaire "tekstberichtjes" door het hele lichaam. Deze studie onderzoekt hoe kleine deeltjes die door spiercellen worden vrijgegeven zich verhouden tot vergelijkbare deeltjes van veelgebruikte stamcellen voor toekomstige therapieën. Door de genetische signalen die deze deeltjes dragen te ontcijferen, stellen de auteurs een praktische vraag: bij welke soorten ziekten zouden spier-afgeleide deeltjes beter kunnen zijn dan die afkomstig van stamcellen?
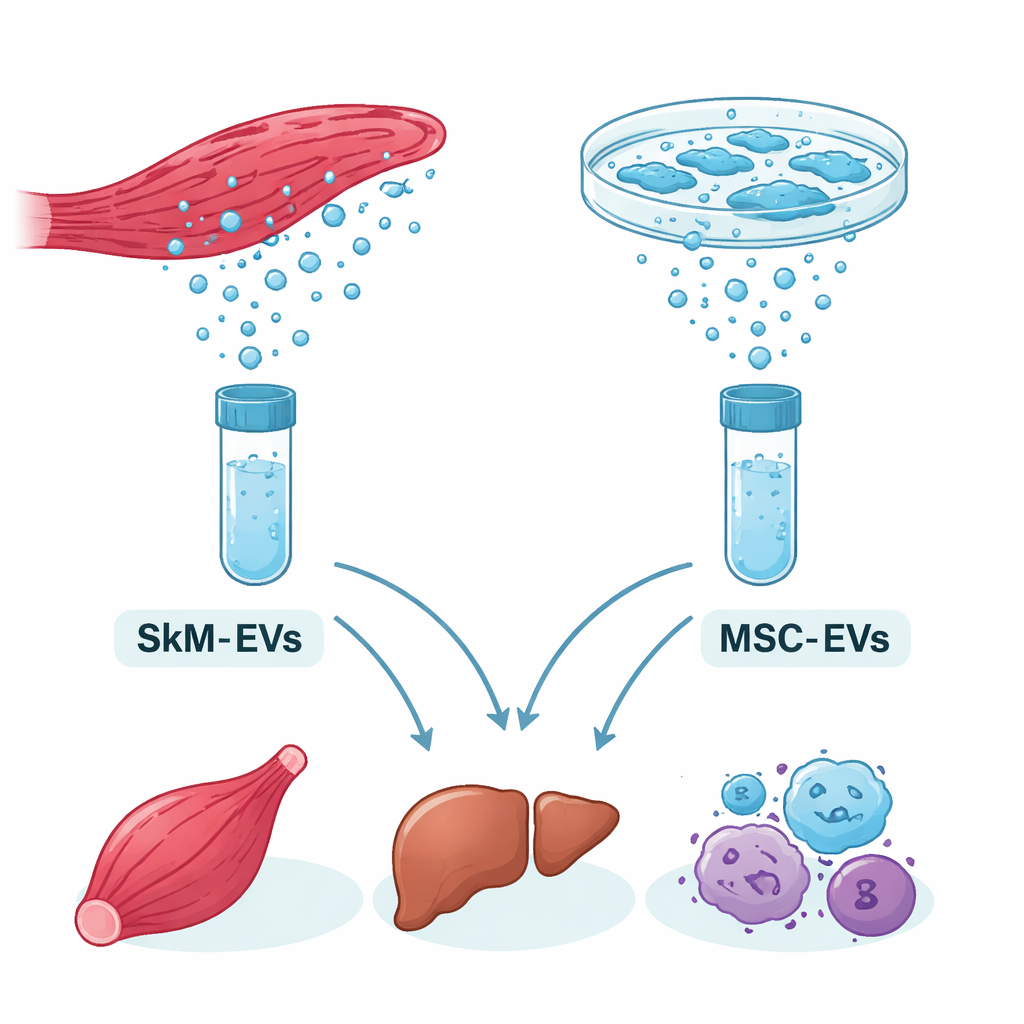
Kleine koeriers door het lichaam
Alle cellen geven microscopische belletjes vrij die extracellulaire blaasjes (EV's) worden genoemd. Dit zijn nanoschaal pakketjes omhuld met vet en geladen met moleculair vrachtgoed. Een belangrijk type lading zijn microRNA's — korte RNA-fragmenten die helpen genen omhoog of omlaag te regelen en zo het gedrag van cellen vormen. Skeletspier, het weefsel dat beweging aandrijft, blijkt het grootste secretieorgaan van het lichaam te zijn en kan grote hoeveelheden EV's afgeven, vooral wanneer het op niet-invasieve manieren wordt gestimuleerd, zoals met echografie. Mesenchymale stamcellen daarentegen zijn al een werkpaard in klinische onderzoeken, waarbij hun EV's getest worden voor weefselherstel en het temperen van ontsteking.
De genetische code van de lading lezen
In plaats van EV's direct in dieren of mensen te testen, heranalyseerden de onderzoekers bestaande sequencingdatasets die bijhouden welke microRNA's aanwezig zijn in EV's van muis-skeletmyotubes (in het laboratorium gekweekte spiervezels) en van uit beenmerg afkomstige mesenchymale stamcellen. Spier-EV's hadden een paar dominante microRNA's, zoals miR-206-3p en miR-378a-3p, die meer dan 60 procent van hun lading uitmaakten, terwijl stamcel-EV's een meer gelijkmatige mix droegen, waaronder de breed werkende let-7-familie. Omdat elk microRNA veel doelgenen kan beïnvloeden, en veel microRNA's kunnen samenlopen op dezelfde route, bouwde het team computationele methoden om te begrijpen hoe volledige profielen — niet losse moleculen — cellulair programma's kunnen herschikken.
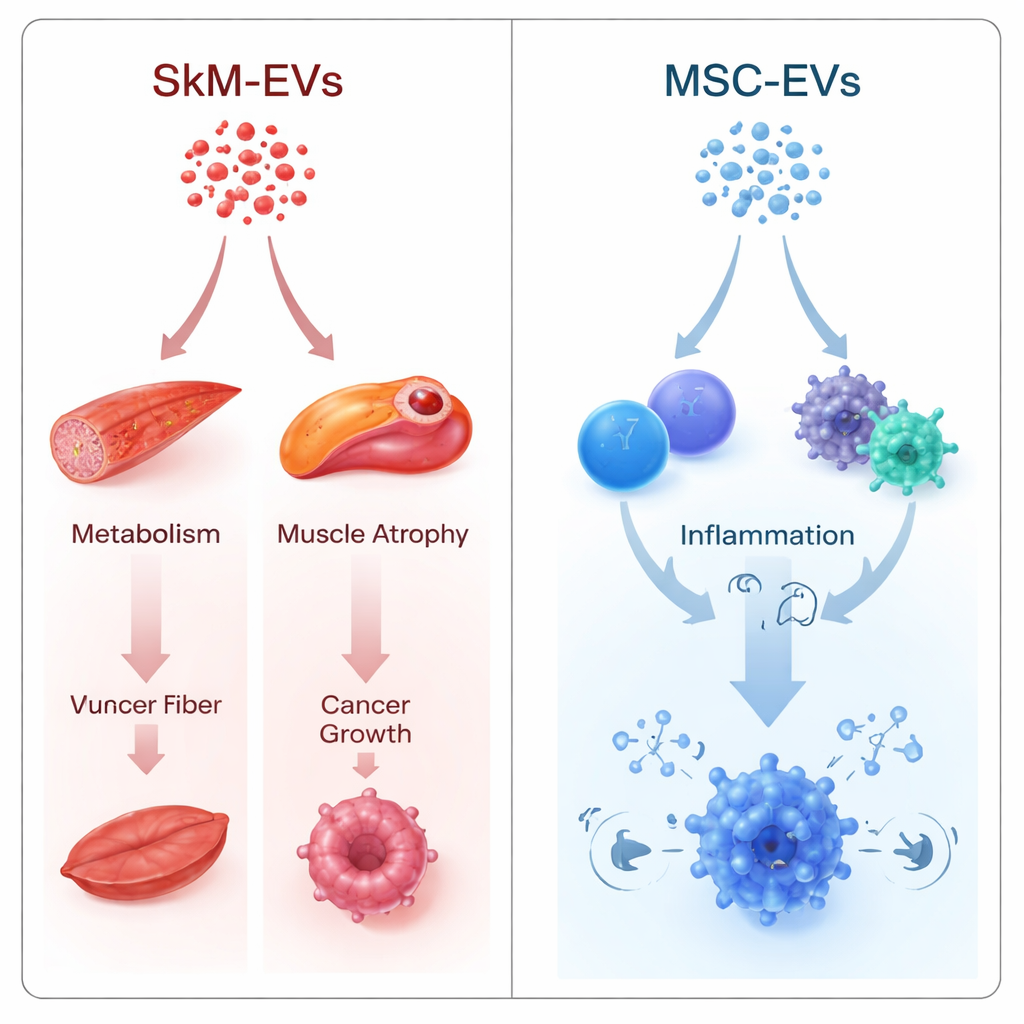
Routes gekoppeld aan spier, stofwisseling en kanker
De auteurs gebruikten twee complementaire strategieën. De ene vergeleek spier- en stamcel-EV's rechtstreeks met elkaar en onderzocht waar hun microRNA's verschilden. De andere behandelde elk EV-type afzonderlijk en zette het microRNA-profiel om in een gen-niveau "impactscore" die schat hoe sterk de lading bepaalde routes zou kunnen dempen. Ondanks verschillende wiskunde wezen beide benaderingen in dezelfde richting. Spier-afgeleide EV's toonden een voorspelde neiging om routes te onderdrukken die samenhangen met spierverlies (FoxO- en TGF-β-signaleringsroutes), bloedsuikerregeling en energiebalans (FoxO, mTOR, AMPK) en routes die tumorgroei bevorderen (ErbB-signaleringsroute en een groep aangeduid als "microRNA's in kanker"). Veel van de meest invloedrijke doelen waren centrale regelaars van gluconeogenese in de lever, belangrijke aanjagers van spieratrofie en kerngenen die kanker bevorderen.
Stamcelblaasjes en het immuunsysteem
Stamcel-EV's vertellen een ander verhaal. Hun microRNA-lading werd voorspeld sterker te werken op immuungerelateerde routes: NF-κB-signaleringsroute, cytokine–receptorinteracties, B- en T-celreceptorsignalering en Th17-celdifferentiatie. Deze zijn centraal voor hoe het lichaam infecties waarneemt, ontsteking aan- en uitzet en de identiteit van immuuncellen vormt. Deze bias komt overeen met groeiend experimenteel bewijs dat stamcel-EV's immuunreacties breed kunnen moduleren en worden getest bij aandoeningen waarbij het temperen van ontsteking cruciaal is, zoals auto-immuun- en ontstekingsziekten.
Van computer-voorspellingen naar toekomstige behandelingen
Samengevat suggereert het werk dat spier-afgeleide EV's van nature geschikt kunnen zijn voor aandoeningen die gepaard gaan met spierverlies, verstoorde stofwisseling of ongecontroleerde celgroei, terwijl stamcel-EV's beter aansluiten bij ziekten die worden aangedreven door ontregelde immuunresponsen. De resultaten zijn volledig gebaseerd op computationele analyse van bestaande gegevens en bewijzen nog geen voordeel bij patiënten, en ze houden geen rekening met andere EV-lading zoals eiwitten of lipiden. Toch biedt deze studie, door complexe microRNA-profielen om te zetten in route-niveau "vingerafdrukken", een routekaart voor het koppelen van EV-bronnen aan ziektecategorieën en helpt ze prioriteren welke combinaties het meest veelbelovend zijn om in het laboratorium en uiteindelijk in de kliniek te testen.
Bronvermelding: Kawamoto, Y., Yamaguchi, A., Ma, X. et al. Functional properties of skeletal myotube-derived extracellular vesicles based on microRNA profiles: a comparative analysis with mesenchymal stem cell-derived extracellular vesicles. Sci Rep 16, 7436 (2026). https://doi.org/10.1038/s41598-026-38076-8
Trefwoorden: extracellulaire blaasjes, skeletspier, microRNA, mesenchymale stamcellen, celsignaalroutes