Clear Sky Science · nl
Engineering polyethylenimine–metal functionalized cryogels for superior catalase binding, activity, and long-term durability
Waarom het vasthouden van enzymen ertoe doet
Waterstofperoxide is een veelvoorkomend chemisch bijproduct in alles van voedselverwerking tot medische behandelingen, en levende cellen vertrouwen op het enzym catalase om het af te breken tot onschadelijk water en zuurstof. In de industrie wordt catalase echter meestal in vrije, opgeloste vorm gebruikt; die verliest snel activiteit, is niet makkelijk terug te winnen en moet vaak worden vervangen. Deze studie onderzoekt een manier om catalase in een sponsachtig materiaal te "parkeren" zodat het langer actief blijft, herhaaldelijk kan worden hergebruikt en efficiënter werkt — allemaal factoren die de kosten kunnen verlagen en enzymgebaseerde processen schoner en duurzamer kunnen maken.

Een slimme spons bouwen
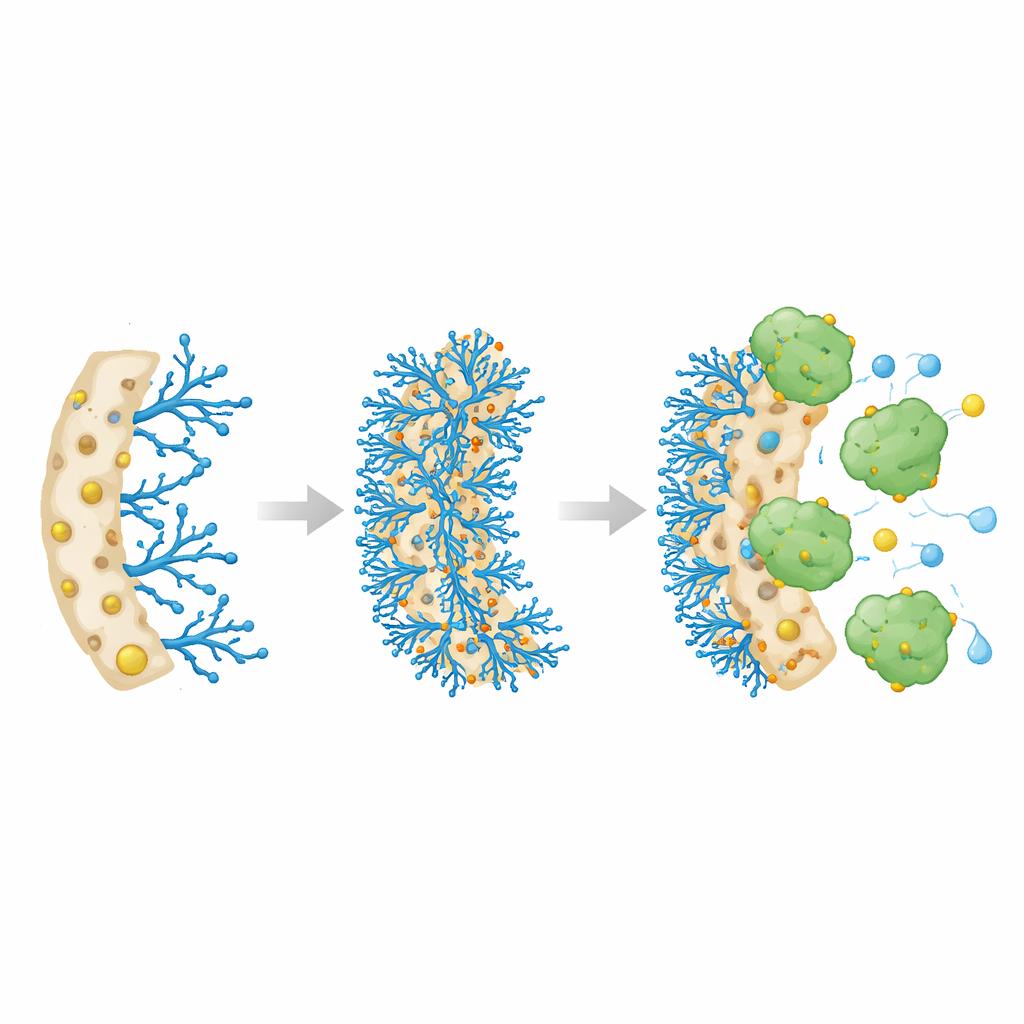
De onderzoekers ontwierpen een speciaal polymeersponsje, een zogenoemde cryogel, gevormd door een vloeibaar mengsel in te vriezen en weer te ontdooien zodat ijskristallen grote, onderling verbonden poriën uitkerven. Deze poriën laten vloeistoffen vrij doorstromen, zoals water door een loofah, terwijl het vaste raamwerk taai en elastisch blijft. Het team gebruikte een basismateriaal genaamd Poly(HEMA-co-GMA), waarop ze chemisch een vertakt molecuul rijk aan stikstofgroepen graftten: polyethyleenimine (PEI). Tenslotte koppelden ze metaalionen — koper, nikkel of kobalt — aan deze stikstofplaatsen. Het idee was dat de metaalionen zouden fungeren als aanlegplaatsen die catalasemoleculen stevig aantrekken en vasthouden, zonder de doorstroming van vloeistof door de spons te blokkeren.
Het materiaal afstemmen voor optimale prestaties
Om te begrijpen hoe elke stap in dit ontwerp het materiaal veranderde, gebruikte het team verschillende laboratoriumtechnieken om de structuur, chemie en stabiliteit te onderzoeken. Ze lieten zien dat het toevoegen van PEI en daarna metalen het poreuze netwerk niet deed instorten, maar juist het vermogen van de spons om water vast te houden vergrootte, wat gunstig is om enzymen een comfortabele, actieve omgeving te bieden. Van de drie metalen creëerde koper de meest gehydrateerde en goed georganiseerde omgeving. Microscopische beelden toonden aan dat het oorspronkelijke materiaal op gepakte korrels leek, terwijl de met PEI en metalen behandelde versies openden naar een schoner, meer continu netwerk van grote poriën. Metingen van het metaalgehalte bevestigden dat koper sterker en in hogere hoeveelheden gebonden was dan nikkel of kobalt, wat suggereert dat het de meest effectieve aanlegplaatsen voor catalase zou bieden.
Catalase op zijn plaats vergrendelen
Toen catalase aan de verschillende metaalgedragen sponzen werd toegevoegd, namen alle drie het enzym snel op, maar de koperversie stak er met kop en schouders bovenuit. Deze laadde de grootste hoeveelheid catalase — ongeveer 392 milligram per gram droge spons — en bereikte binnen ongeveer acht uur een evenwichtsniveau. De onderzoekers onderzochten vervolgens hoe goed het geïnmmobiliseerde enzym werkte vergeleken met vrije catalase in oplossing. Hoewel de maximale reactiesnelheid per gram enzym enigszins daalde, toonde de geïnmmobiliseerde catalase een veel sterkere schijnbare aantrekking tot zijn substraat, waterstofperoxide. In praktische termen betekent dit dat het gebonden enzym zijn werk efficiënter deed bij lagere substraatconcentraties, waarschijnlijk omdat de poreuze, watergevulde koperspons het substraat nabij het enzym concentreerde en hielp de actieve vouwing te behouden.
Een enzym dat het uithoudt
Een van de grootste voordelen van het immobiliseren van enzymen is de belofte van herbruikbaarheid en een lange houdbaarheid. Hier bleek catalase dat aan de kopergebaseerde cryogel was gebonden veel duurzamer dan zijn vrije tegenhanger. Na 15 herhaalde gebruikscycli behield het geïmmobiliseerde enzym nog ongeveer een derde van zijn initiële activiteit, terwijl vrije catalase doorgaans na één gebruik wordt weggegooid. In opslagtests bij koelkasttemperatuur over 70 dagen behield de geïmmobiliseerde catalase meer dan 60% van zijn activiteit, ruwweg het dubbele van het vrije enzym. De spons maakte het ook mogelijk het enzym met een eenvoudige zoutoplossing los te maken en opnieuw te laden, wat aantoont dat het materiaal zelf meerdere keren kan worden hergebruikt zonder noemenswaardig verlies van capaciteit.
Wat dit betekent voor gebruik in de praktijk
Voor niet-specialisten is de belangrijkste conclusie dat de onderzoekers een soort herbruikbare "enzymspons" hebben gebouwd die catalase stevig maar zacht vasthoudt, waardoor het beter functioneert bij lagere chemische concentraties en veel langer meegaat tijdens gebruik en opslag. Door een zeer poreuze cryogel te combineren met PEI en koperionen hebben ze een platform gecreëerd dat hoge enzymbelading, verbeterde efficiëntie en sterke langetermijnstabiliteit verenigt. Dergelijke materialen zouden kunnen worden geïntegreerd in industriële of milieusystemen om waterstofperoxide en aanverwante stoffen betrouwbaarder en met minder afval af te breken, een praktische stap richting groenere, enzymgestuurde technologieën.
Bronvermelding: Erol, K., Alkan, M.H. & Alacabey, İ. Engineering polyethylenimine–metal functionalized cryogels for superior catalase binding, activity, and long-term durability. Sci Rep 16, 7880 (2026). https://doi.org/10.1038/s41598-026-38040-6
Trefwoorden: enzyme immobilization, catalase, cryogel, copper-functionalized polymers, biocatalysis