Clear Sky Science · nl
Een hulpmiddel om pH- en temperatuureffecten op varkens- en menselijke pepsineactiviteit tijdens in vitro maagvertering te voorspellen
Waarom maagenzymen van belang zijn voor alledaags eten
Telkens wanneer we eten, beginnen krachtige enzymen in onze maag eiwitten uit voedsel af te breken tot kleinere stukken die ons lichaam kan gebruiken. Een van de belangrijkste van deze enzymen is pepsine. Voedselwetenschappers gebruiken in laboratoriumtests vaak een varkensversie van pepsine als vervanger voor de menselijke vorm, in de veronderstelling dat ze zich min of meer hetzelfde gedragen. Deze studie stelt een eenvoudige maar cruciale vraag: onder de veranderende omstandigheden in een echte maag—waar zowel de zuurgraad (pH) als de temperatuur schommelen—gedragen menselijke en varkenspepsine zich dan echt gelijk, en hoe kunnen we voorspellen wat ze zullen doen?
Hoe de veranderende omstandigheden in de maag de vertering vormen
In de maag zijn pH en temperatuur allesbehalve constant. Een koud drankje kan de maag tijdelijk met meer dan 10 graden afkoelen, en een grote of alkalische maaltijd kan de maag-pH met meerdere eenheden verhogen voordat deze langzaam terugkeert naar een zuurdere toestand. Omdat de capaciteit van pepsine om eiwitten te knippen sterk afhangt van zowel zuurgraad als warmte, kunnen deze schommelingen de vertering versnellen of vertragen. Direct volgen van dit proces bij mensen is lastig, dus onderzoekers vertrouwen op in vitro-modellen—zorgvuldig gecontroleerde glasopstellingen van vertering. Die modellen gebruiken meestal porcine (varkens) pepsine als plaatsvervanger voor menselijke pepsine, maar tot nu toe ontbrak een duidelijke kaart van hoe beide enzymen reageren wanneer pH en temperatuur samen verschuiven, zoals na een maaltijd.
Pepsineprestaties meten over veel omstandigheden
De auteurs testten menselijke pepsine uit maagvocht en commerciële porcine pepsine in 37 combinaties van pH (van zeer zuur tot bijna neutraal) en temperatuur (van koelkast-koud tot behoorlijk heet). Ze gebruikten deze metingen om wiskundige modellen te bouwen die kunnen voorspellen hoe actief elk enzym zal zijn onder elke maagachtige combinatie van zuurgraad en warmte. Beide enzymen werkten het beste rond pH 2 en lichaamstemperatuur, maar de menselijke versie bleef werkzaam over een breder bereik. Bij pH 3 en 4 behield menselijke pepsine nog aanzienlijke activiteit, terwijl de activiteit van varkenspepsine sterk terugliep. Interessant genoeg was porcine pepsine, hoewel krachtiger op zijn piek, veel gevoeliger voor pH-veranderingen, wat betekent dat zijn prestatie sneller kan afnemen naarmate de omstandigheden minder ideaal worden.
Wat het nieuwe voorspellingsinstrument ons kan vertellen
Door deze metingen om te zetten in gebruiksvriendelijke vergelijkingen ingebed in spreadsheettools, creëerden de onderzoekers een manier voor anderen om de pepsineactiviteit tijdens laboratoriumverteringsexperimenten te schatten. Ze voerden verschillende casestudies uit om te laten zien wat het instrument kan doen. In een semi-dynamisch model van melksvertering toonden gesimuleerde menselijke en porcine pepsine vergelijkbare algemene patronen, maar menselijke pepsine behield nuttige activiteit langer naarmate de pH verschoof, wat leidde tot een grotere totale “oppervlakte onder de curve” voor activiteit in de tijd. Het hulpmiddel vergeleek ook traditionele statische verteringsopstellingen—waarbij pH constant wordt gehouden—met semi-dynamische opstellingen die geleidelijk verzuren, en simuleerde hoe pepsineactiviteit zou kunnen verschillen bij jongere versus oudere volwassenen, die doorgaans minder pepsine afscheiden. Deze voorbeelden benadrukken hoe dezelfde maaltijd en protocollen verschillende niveaus van eiwitafbraak kunnen opleveren, afhankelijk van welk enzymtype en verteringsmodel wordt gebruikt.
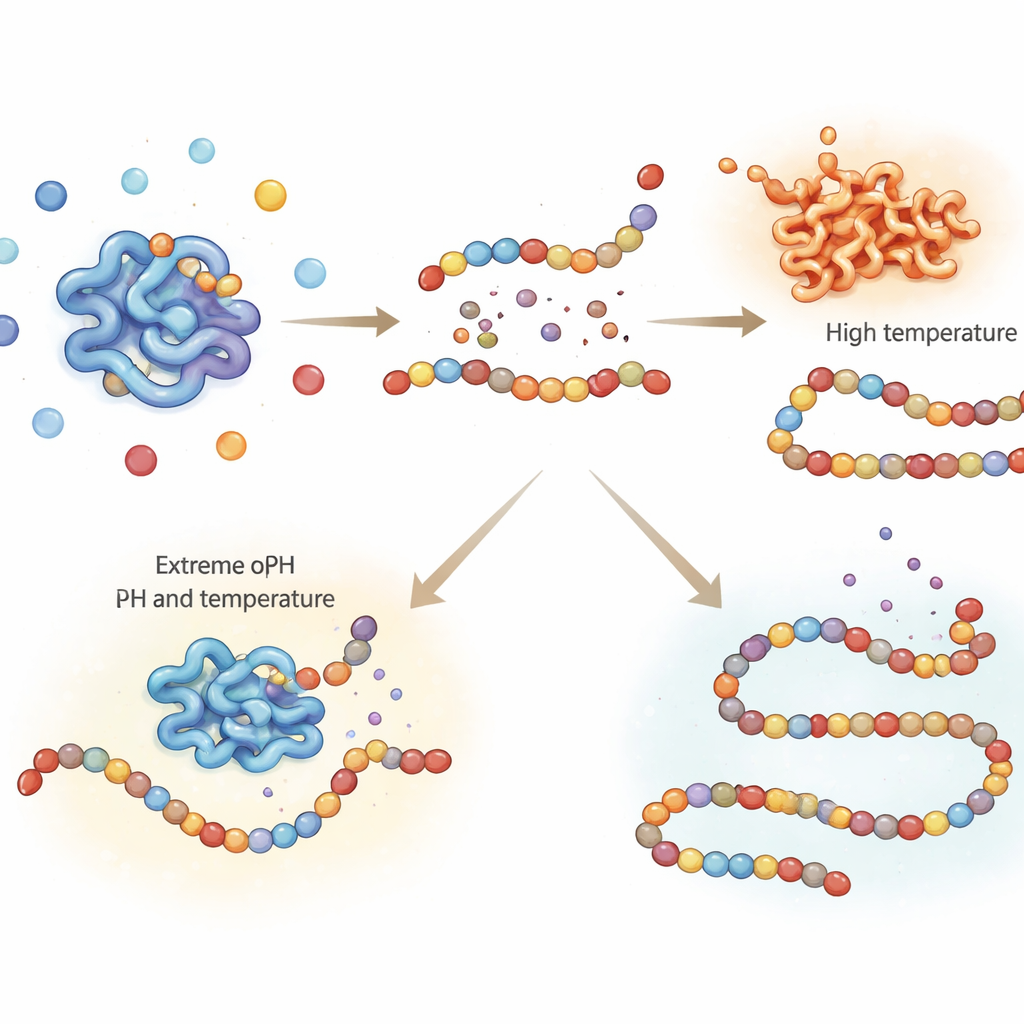
Het bepalen van het milde punt waarop hitte pepsine uitschakelt
In verteringsexperimenten is het essentieel om pepsine op specifieke tijdstippen te stoppen zodat latere metingen weerspiegelen wat in de “maag” gebeurde en niet de voortgezette afbraak in buisjes. Een gebruikelijke manier om enzymen uit te schakelen is verwarming, maar te veel hitte kan andere voedingscomponenten beschadigen en de resultaten vertekenen. Deze studie testte zorgvuldig hoe lang en hoe heet porcine pepsine verhit moet worden om permanent geïnactiveerd te raken. Verwarming op 65 °C gedurende tot 15 minuten verminderde de activiteit slechts gedeeltelijk, wat betekent dat het enzym daarna nog steeds kon doorwerken. Daarentegen schakelde verwarming op 75 °C of hoger gedurende slechts 5 minuten pepsine volledig en onomkeerbaar uit. Infraroodspectroscopie van de structuur van het enzym toonde aan dat deze hogere temperaturen blijvende ontvouwing en aggregatie van het eiwit veroorzaakten, wat overeenkomt met het verlies van activiteit.
Wat dit betekent voor voedingsonderzoek en gezondheid
Voor niet-specialisten is de kernboodschap dat de varkenspepsine die vaak in laboratoriummodellen wordt gebruikt zich niet precies hetzelfde gedraagt als menselijke pepsine wanneer realistische maagomstandigheden—schommelende zuurgraad en temperatuur—in aanmerking worden genomen. Het nieuwe voorspellingsinstrument helpt onderzoekers in te schatten hoeveel eiwitknipkracht op elk moment van een verteringsexperiment aanwezig is en te beoordelen of hun opzet echt weerspiegelt wat in een menselijke maag zou kunnen gebeuren, inclusief die van oudere volwassenen. Tegelijkertijd wijst het werk op een milde maar betrouwbare warmtebehandeling—vijf minuten bij 75 °C—om pepsine uit te schakelen zonder onnodige schade aan andere voedingscomponenten. Samen zouden deze verbeteringen laboratoriumgebaseerde verteringsstudies nauwkeuriger en beter vergelijkbaar moeten maken, wat ons begrip verbetert van hoe verschillende voedingsmiddelen en verwerkingsmethoden eiwitvertering in het dagelijks leven beïnvloeden.
Bronvermelding: C. J., F., D., F., I., C. et al. A tool for predicting pH and temperature effects on porcine and human pepsin activity during in vitro gastric digestion. Sci Rep 16, 9176 (2026). https://doi.org/10.1038/s41598-026-38033-5
Trefwoorden: pepsine, maagvertering, pH en temperatuur, in vitro modellen, proteïnevertering