Clear Sky Science · nl
Chronische NH4Cl-lading verbetert glucosetolerantie zonder insulinegevoeligheid te veranderen bij muizen
Waarom zuur-basebalans belangrijk is voor de bloedsuiker
Mensen met chronische nierziekte ontwikkelen vaak een toestand die metabole acidose wordt genoemd, waarbij het bloed iets zuurder is dan normaal. Artsen beschouwen dit doorgaans als schadelijk, deels omdat korte periodes van acidose bekendstaan om de bloedsuikerregeling te verslechteren. Deze studie keert dat idee om: bij muizen verbeterde een langdurige, milde acidose juist de manier waarop het lichaam met suiker omgaat, zonder dat het hormoon insuline beter of slechter ging werken. Het begrijpen van deze verrassende bevinding kan uiteindelijk helpen behandelingen voor zowel nierziekte als type 2 diabetes te verfijnen.
Een langdurige zure uitdaging bij muizen
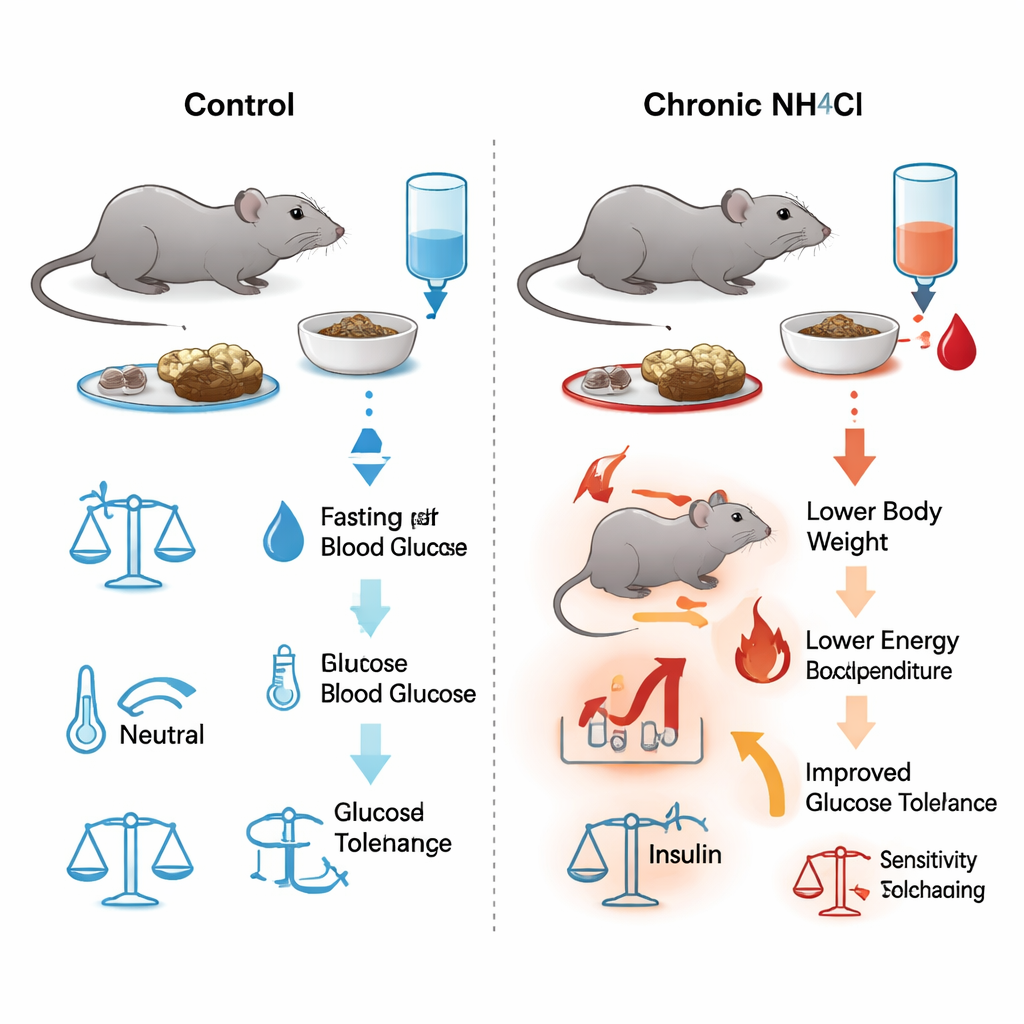
De onderzoekers gaven mannelijke muizen drinkwater met ammoniumchloride, een zout dat het bloed zachtjes verzacht (zuurder maakt), gedurende maximaal zes maanden. Deze behandeling bootst de chronische zure belasting na die bij nierziekte voorkomt. Bloedtests bevestigden een aanhoudende, milde metabole acidose: lagere pH en bicarbonaat, hogere chloride en verder stabiele niergerelateerde maten zoals ureum en hematocriet. Ondanks dat ze evenveel of meer aten en dronken dan onbehandelde muizen, stopten de zuurbelaste dieren na ongeveer twee maanden met gewichtstoename. Gedetailleerde metingen in metabolische kooien toonden dat deze muizen in het algemeen meer energie verbrandden, minder vetvrije (spierrijke) massa hadden en relatief meer vet meedroegen, wat wijst op een hogere metabole kost van bestaan onder chronische acidose.
Betere bloedsuikercontrole zonder extra insulinehulp
Het team testte herhaaldelijk hoe snel de muizen suiker uit hun bloed verwijderden door glucose te injecteren en de bloedspiegels in de tijd te volgen. Al binnen een week na het starten van het verzurende drankje verlaagden de behandelde muizen hun bloedsuiker sneller dan de controles, en dit voordeel bleef aanwezig op veel tijdstippen tot 180 dagen. Nuchtere bloedsuiker was consequent lager in de zure groep. Toch waren de insulinespiegels in het bloed tijdens deze tests gelijk in beide groepen. Losse tests waarin muizen rechtstreeks insuline kregen toegediend toonden ook dat hun algehele insulinegevoeligheid ongewijzigd was. Met andere woorden: chronische acidose verbeterde de glucosetolerantie zonder de alvleesklier te dwingen meer insuline te produceren of de weefsels sterker te laten reageren.
Verplaatsing waar en hoe suiker wordt gemaakt en verloren
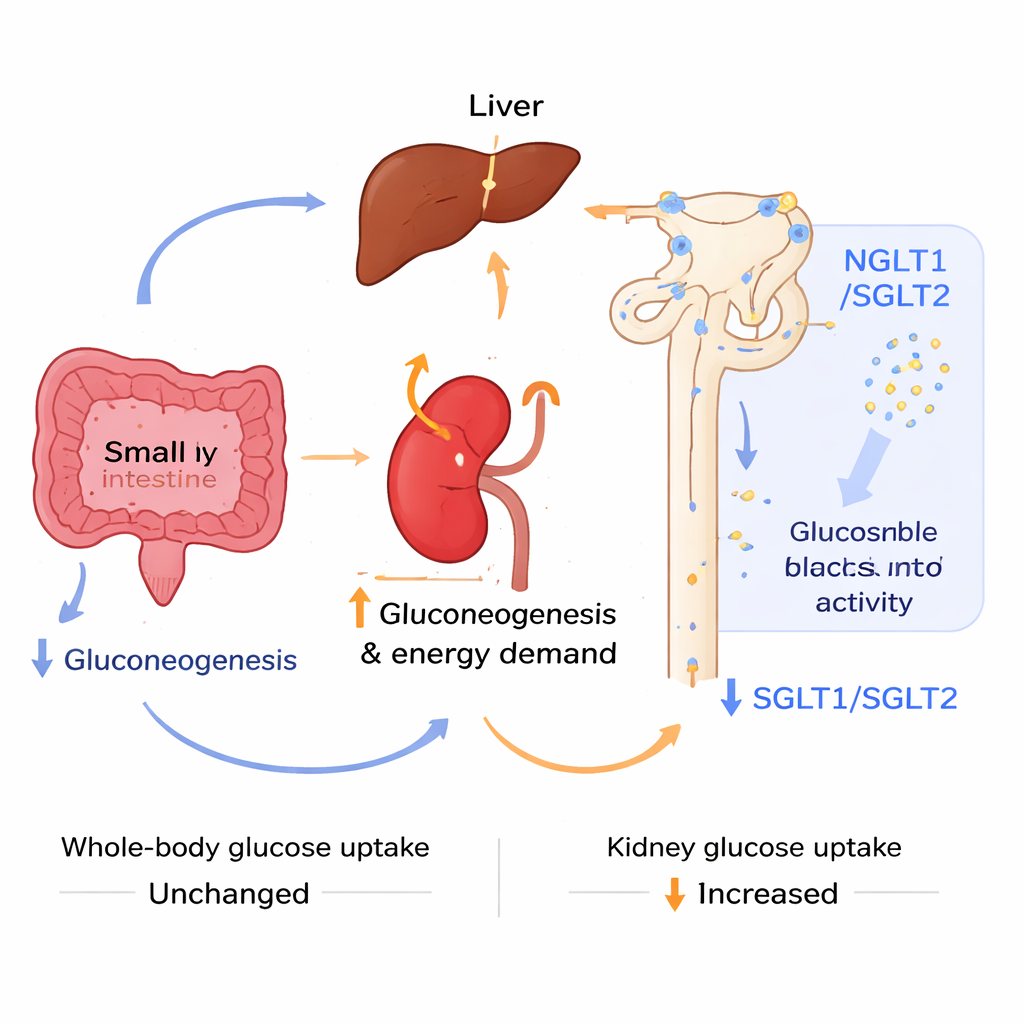
Om te achterhalen waar de extra suikercontrole vandaan kwam, onderzochten de onderzoekers hoe verschillende organen glucose produceerden. Ze gebruikten specifieke stoffen — pyruvaat, alanine en glutamine — die in suikermakende routes in lever, nier en darm terechtkomen. In de loop van de tijd werden de lever en delen van de darm van de zure muizen minder actief in het maken van nieuwe glucose, vooral uit alanine en glutamine. Daarentegen liet de nier tekenen van verhoogde activiteit zien: sleutelgenen die betrokken zijn bij glucoseproductie en energievoorziening waren omhooggeregeld, en beeldvorming met een radioactieve glucosemimic toonde een hogere suikeropname in de nieren en blaas, ondanks dat de totale lichaamsopname ongewijzigd was. Tegelijkertijd ging er na een suikerbelasting meer glucose verloren in de urine, omdat de hoofd natrium–glucosetransporters van de nier, die normaal gefilterde suiker terugwinnen, op zowel RNA- als proteïneniveau naar beneden waren bijgesteld. Deze combinatie — minder suiker geproduceerd door lever en darm, meer suiker verbrand en uitgescheiden door de nier — hielp de bloedspiegels onder controle te houden.
Diepe veranderingen binnen niercellen
Snapshots van genactiviteit in de nieren gedurende de eerste twee maanden van behandeling toonden brede herprogrammering van cellulaire mechanismen. Routes die betrokken zijn bij het verplaatsen van geladen deeltjes (anionen), het terugwinnen van bicarbonaat en het laten draaien van mitochondriën en oxidatieve fosforylering — de belangrijkste energiegeneratoren van de cel — waren versterkt. Genen die verband houden met glucose- en vetmetabolisme verschoof ook omhoog, terwijl sommige immuun- en detoxificatiepaden, inclusief delen van het complementstelsel en de cytochroom P450-familie, werden gedempt. Deze patronen komen overeen met een nier die harder werkt om zuur uit te scheiden, meer brandstof verbruikt en tegelijkertijd herprogrammeert hoe het met suiker en lipiden omgaat om aan de extra energievraag te voldoen.
Wat dit betekent voor mensen met nier- en suikerproblemen
Samengevat: langdurige, milde metabole acidose bij muizen schaadde de bloedsuikercontrole niet — het verbeterde die juist — door de suikerproductie in lever en darm te verminderen, de suikerterugresorptie in de nier te verlagen en het eigen energiegebruik van de nier te verhogen. Insuline zelf speelde geen grotere rol dan normaal. Dit betekent niet dat acidose goed is of dat patiënten zuur moeten blijven; acidose heeft nog steeds veel schadelijke effecten. Maar de bevindingen laten zien dat het lichaam op onverwachte manieren kan aanpassen en benadrukken de nier als een krachtige regulator van de bloedsuiker. Toekomstig werk zou mogelijk enkele van deze nier-gebaseerde mechanismen — zoals verhoogd urineverlies van glucose en gewijzigde glucoseproductie — kunnen benutten zonder patiënten bloot te stellen aan de risico’s van chronische acidose.
Bronvermelding: Zaibi, N., Montaigne, J., Baraka-Vidot, J. et al. Chronic NH4Cl loading improves glucose tolerance without modifying insulin sensitivity in mice. Sci Rep 16, 7048 (2026). https://doi.org/10.1038/s41598-026-38007-7
Trefwoorden: metabole acidose, glucosetolerantie, nierfunctie, gluconeogenese, type 2 diabetes risico