Clear Sky Science · nl
Computationele identificatie en mechanistische karakterisering van natuurlijke productbinders gericht op de PDE6D-prenylbindings-tunnel
De favoriete schakel van kanker tegen zichzelf keren
Veel van de dodelijkste vormen van kanker — van alvleesklier- tot colorectale- en longtumoren — zijn afhankelijk van één moleculaire "aan"-schakel genaamd RAS. Wanneer deze schakel vastzit in de AAN-stand, groeien cellen ongecontroleerd. Decennialang hebben geneesmiddelenontwikkelaars moeite gehad om RAS rechtstreeks uit te schakelen. Deze studie onderzoekt een andere tactiek: zoeken naar natuurlijke verbindingen die stilletjes het hulp-eiwit kunnen blokkeren dat RAS nodig heeft om op zijn werkplek te komen, waardoor het signaal mogelijk wordt gedimd zonder RAS zelf direct aan te pakken. 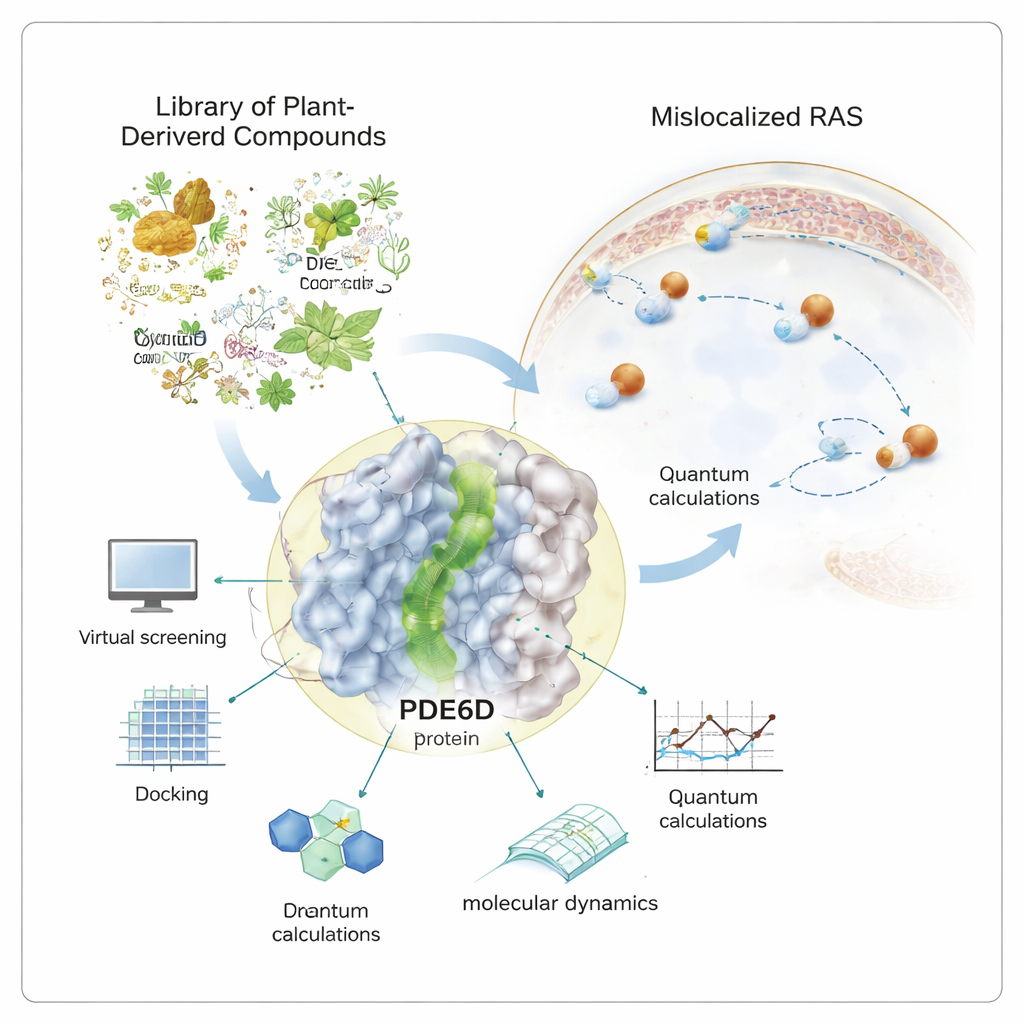
Een verborgen helper in kankercellen
RAS-eiwitten moeten aan de binnenkant van het celmembraan zitten om groeisignalen te geven. Om daar te komen dragen ze een vette staart die ze in het membraan verankert. Een chaperonne-eiwit genaamd PDE6D fungeert als een taxi en beschermt die staart terwijl RAS door het waterige binnenste van de cel reist. PDE6D heeft een smalle, met olie beklede tunnel die de RAS-staart vastgrijpt. Als die tunnel wordt geblokkeerd, komt RAS eerder op de verkeerde plaats terecht, waardoor zijn vermogen om kanker aan te jagen afneemt. Omdat veel bestaande RAS-medicijnen slechts werken voor een kleine subset van mutaties, zijn onderzoekers geïnteresseerd in PDE6D als een indirect maar breder relevant doelwit.
Computers gebruiken om de chemische bibliotheek van de natuur te winnen
In plaats van uitsluitend op synthetische chemicaliën te vertrouwen, wendde de auteur zich tot een gecureerde bibliotheek van meer dan duizend koopbare natuurlijke producten — moleculen oorspronkelijk afgeleid van planten, microben en andere levende bronnen. Krachtige computertools werden gebruikt om deze bibliotheek te screenen tegen de 3D-structuur van PDE6D. In deze virtuele test werd elk molecuul in de tunnel "gedokt" om te zien hoe nauw en gunstig het mogelijk zou binden. De best scorende kandidaten werden vervolgens nauwkeuriger onderzocht met kwantumniveau-berekeningen, die nagaan hoe elektronen in elk molecuul zijn gerangschikt en hoe gemakkelijk ze kunnen deelnemen aan stabiliserende interacties in de eiwitpocket.
Veelbelovende kandidaten op de proef stellen in beweging
Eiwitten en kleine moleculen blijven niet stil zitten in cellen, dus de studie ging verder dan statische momentopnames. Met lange moleculaire dynamica-simulaties die atomaire bewegingen over een halve microseconde volgden, observeerde de onderzoeker hoe elk veelbelovend natuurlijk verbindingsmiddel zich in de loop van de tijd in de PDE6D-tunnel gedroeg. Twee kandidaten, gelabeld MolPort-039-052-621 en MolPort-002-507-186, bleven in de tunnel verankerd met stabiele contactnetwerken, terwijl een derde molecule naar de tunneluitgang dreven en zwakker gebonden raakte. Aanvullende analyses brachten in kaart welke delen van de PDE6D-structuur flexibeler werden of juist tot rust kwamen bij binding, en hoe het complex zijn "energielandschap" verkende — in wezen welke vormen het meest comfortabel en langdurig waren. 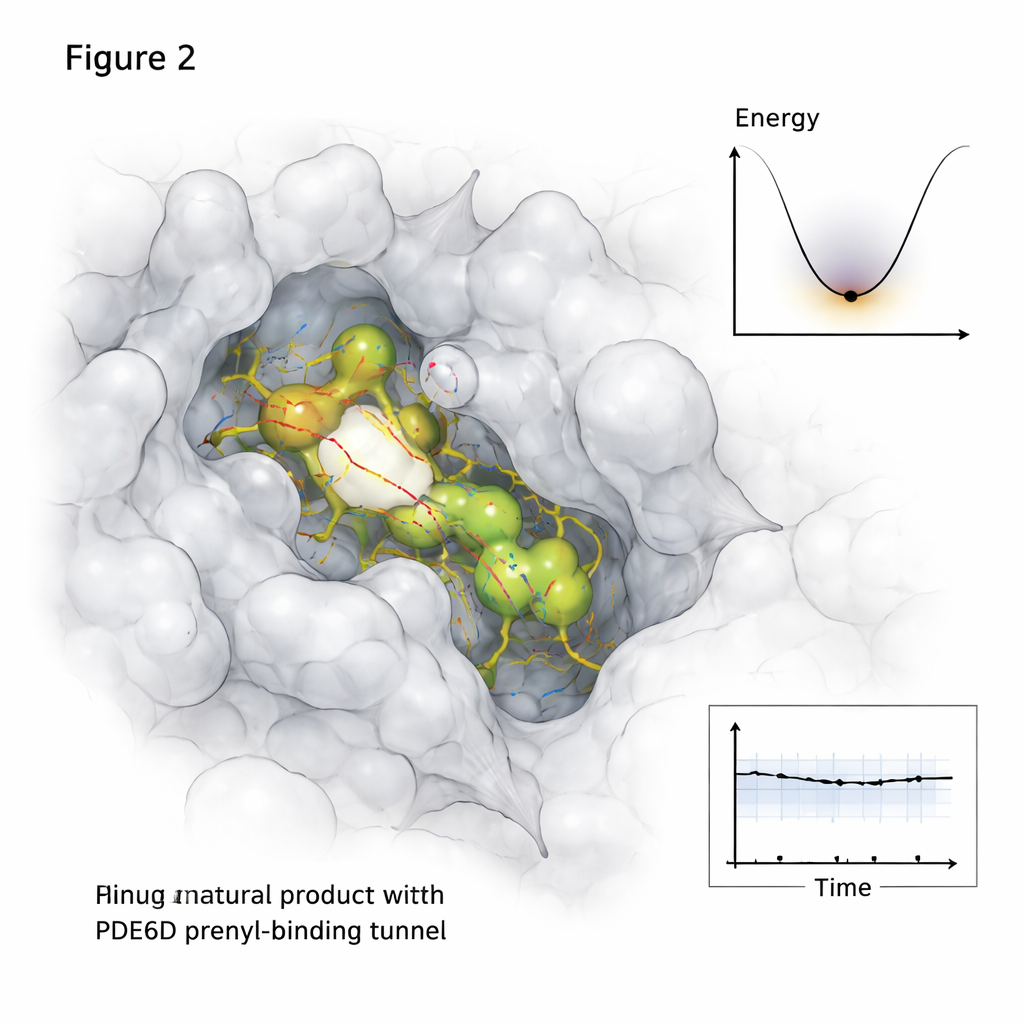
Balanceren van bindingssterkte en geneesmiddellijkenmerken
De studie gebruikte ook online voorspellingshulpmiddelen om te beoordelen of deze natuurlijke verbindingen realistische startpunten voor medicijnen lijken. Alle drie de topkandidaten hadden chemische kenmerken die consistent zijn met basale "drug-likeness", maar elk droeg ook waarschuwingstekens. Sommige werden voorspeld slecht opneembaar of slecht oplosbaar te zijn; andere toonden aanwijzingen voor mogelijke toxiciteit, zoals invloed op het hartritme of op DNA. Deze problemen betekenen dat de moleculen, in hun huidige vorm, waarschijnlijk geen kant-en-klare geneesmiddelen zijn. In plaats daarvan zijn ze het best te zien als structurele sjablonen die chemici kunnen modificeren, waarbij de tunnel-passende kenmerken behouden blijven en probleemgebieden worden afgekapt.
Wat dit betekent voor toekomstige kankerbehandelingen
In eenvoudige termen levert dit werk geen nieuw kanker medicijn op, maar het schetst wel een veelbelovende route. Door verschillende lagen van berekening te combineren — van snelle docking tot gedetailleerde simulaties en kwantumberekeningen — beperkt de studie een enorme verzameling natuurlijke moleculen tot een kleine groep die geschikt lijkt om de PDE6D-tunnel te verstoppen. Als toekomstige laboratoriumexperimenten bevestigen dat deze verbindingen RAS in cellen daadwerkelijk verkeerd localiseren en de groei van RAS-gedreven tumoren vertragen, zouden ze een nieuwe klasse behandelingen kunnen inspireren die de "logistiek" van kanker richten in plaats van de primaire trigger direct aan te pakken.
Bronvermelding: Alshahrani, M.M. Computational identification and mechanistic characterization of natural product binders targeting the PDE6D prenyl binding tunnel. Sci Rep 16, 6571 (2026). https://doi.org/10.1038/s41598-026-37939-4
Trefwoorden: RAS-signaaltransductie, PDE6D-remmers, natuurlijke producten, computationele geneesmiddelenontdekking, kankertherapie