Clear Sky Science · nl
Habitatgebaseerde MRI-radiomics voor verbeterde diagnose van de ziekte van Parkinson
Waarom dit belangrijk is voor patiënten en gezinnen
De ziekte van Parkinson sluipt vaak langzaam binnen, met subtiele tremoren of stijfheid die moeilijk vast te stellen kunnen zijn. Artsen vertrouwen momenteel nog sterk op symptomen en op gespecialiseerde, dure scans om een diagnose te stellen, en vroege gevallen worden gemakkelijk gemist. Deze studie toont aan dat dezelfde alledaagse MRI-scans die veel ziekenhuizen al gebruiken, kunnen worden doorzocht op verborgen patronen, en zo een snellere, minder ingrijpende en opmerkelijk nauwkeurige manier bieden om de ziekte van Parkinson te detecteren.
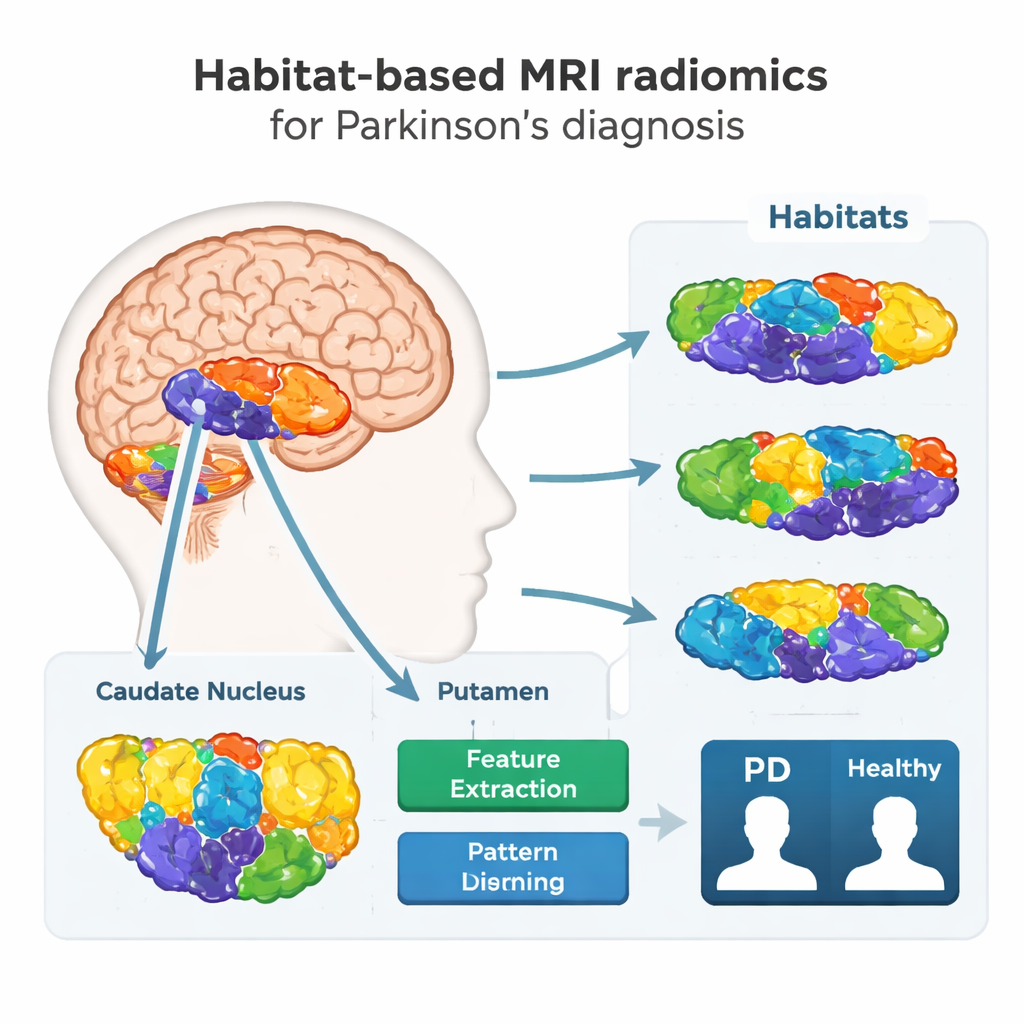
Op een nieuwe manier in de hersenen kijken
De onderzoekers richtten zich op twee diepe hersenstructuren, de nucleus caudatus en de putamen, die centraal staan in bewegingscontrole en sterk aangetast zijn bij de ziekte van Parkinson. In plaats van elke structuur als één massief weefselblok te behandelen, stelden ze een gedetailleerdere vraag: gedragen verschillende stukjes binnen deze regio’s zich anders op MRI, en kunnen die verschillen ziekte onthullen? Om dit te onderzoeken verzamelden ze routine-MRI-scans van 308 mensen—173 met Parkinson en 135 gezonde vrijwilligers—aan twee ziekenhuizen met verschillende scanners, wat de variatie weerspiegelt die in de praktijk voorkomt.
Van hersen-„buurten” naar digitale vingerafdrukken
Met een techniek genaamd habitatgebaseerde radiomics verdeelde het team elke doelregio in kleinere "buurten" of habitats, op basis van subtiele verschillen in helderheid en textuur in de MRI-beelden. Een computeralgoritme groepeerde voxels (kleine 3D-pixels) met vergelijkbare beeldkenmerken in deze habitats en extraheerde vervolgens honderden numerieke kenmerken uit elk van hen. Deze kenmerken vormen een soort digitale vingerafdruk van weefselgezondheid, en vangen kleine onregelmatigheden die met het blote oog onzichtbaar zijn maar mogelijk duiden op verlies van zenuwcellen, littekenvorming of ijzerophoping die geassocieerd worden met Parkinson.
Een diagnostisch model trainen met routine-scans
Met deze vingerafdrukken trainden de wetenschappers een machine-learningmodel, bekend als een support vector machine, om patiënten met Parkinson te onderscheiden van gezonde controles. Ze testten verschillende manieren om de hersenregio’s in habitats te verdelen, van één groot gebied tot tien kleinere. Zowel de hoofd-trainingsset als een onafhankelijke validatieset werden gebruikt om de prestaties te beoordelen. Wanneer de regio’s in vijf habitats werden verdeeld, presteerde het model het beste: op nieuwe, niet-geziene data identificeerde het bijna 9 op de 10 personen met Parkinson correct en bereikte het een totale diagnostische nauwkeurigheid van meer dan 94% in de volledige studie. Dit overtrof eerdere benaderingen die elke hersenregio als één eenheid behandelden en vaak rond de 80–85% nauwkeurigheid bleven steken.
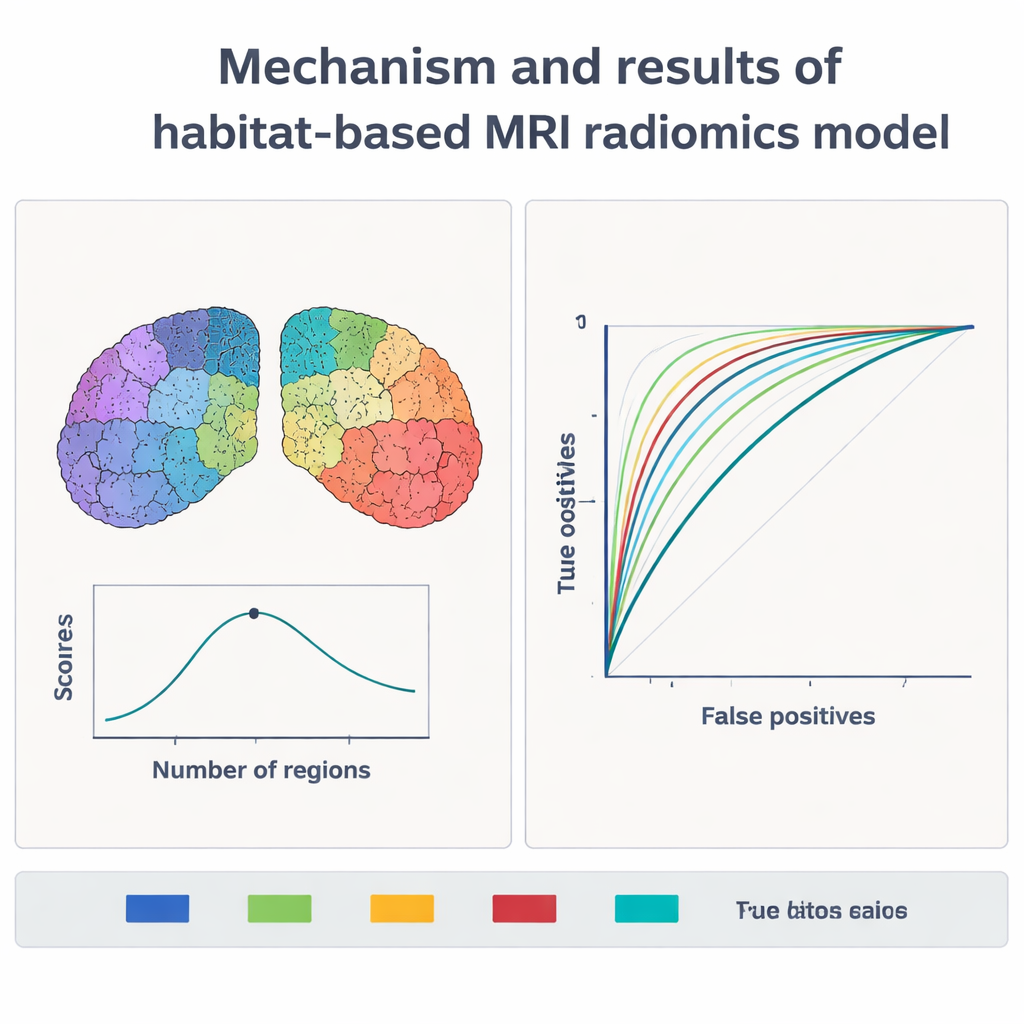
Wat het model eigenlijk ziet
Om te voorkomen dat er een "black box" werd opgebouwd, gebruikte het team een verklaringsmethode genaamd SHAP om te zien welke beeldkenmerken de beslissingen van het model beïnvloedden. De belangrijkste signalen kwamen uit T2-gewogen MRI, een veelgebruikte klinische sequentie. Bij mensen met Parkinson vertoonden de relevante habitats grotere variatie in intensiteit, meer extreme lichte en donkere plekken en scheve intensiteitsverdelingen vergeleken met gezonde vrijwilligers. Deze patronen weerspiegelen waarschijnlijk bekende ziekteprocessen in de basale ganglia, zoals verlies van dopamine-producerende neuronen, lokale littekenvorming en abnormale ijzerafzettingen. Belangrijk is dat dezelfde kenmerken steeds terugkeerden wanneer de data op verschillende manieren werden verdeeld en opnieuw geanalyseerd, en dat ze stabiel bleven over scanners heen, wat suggereert dat de methode robuust is en geen toevallig effect van één enkele machine.
Van onderzoekstool naar kliniek
Decision-curve-analyses, die de voordelen van het opsporen van echte gevallen afwegen tegen de nadelen van valse alarmen, gaven aan dat het model artsen kan helpen beslissen wie echt verdere tests nodig heeft, zoals een DaTscan, en wie veilig extra kostbare procedures kan vermijden. Omdat de methode alleen vertrouwt op standaard MRI-scans en software, kan zij bijzonder waardevol zijn in omgevingen waar geavanceerde nucleaire beeldvorming niet beschikbaar of te duur is. De auteurs stellen dat habitatgebaseerde radiomics bekende MRI-beelden omzet in rijke datakaarten, en zo een krachtig, niet-invasief hulpmiddel biedt voor eerdere en nauwkeurigere diagnose van Parkinson en de basis legt voor toekomstige instrumenten die mogelijk ook ziekteprogressie volgen en behandeling kunnen sturen.
Bronvermelding: Li, YZ., Wang, Y., Cai, C. et al. Habitat-based MRI radiomics for enhanced parkinson’s diagnosis. Sci Rep 16, 4755 (2026). https://doi.org/10.1038/s41598-026-37923-y
Trefwoorden: Ziekte van Parkinson, MRI, radiomics, machine learning, vroegtijdige diagnose