Clear Sky Science · nl
Uiterlijke expressie van CD63 en HLA-DR op circulerende eosinofielen correleert met verbeterde klinische controle na optimalisatie van de behandeling bij astma
Waarom piepkleine bloedcellen belangrijk zijn bij astma
Voor veel mensen met ernstig astma laten krachtige inhalatoren en andere medicijnen hen toch kortademig achter en kwetsbaar voor aanvallen. Artsen volgen de ziekte meestal met eenvoudige bloedtelling, uitgeademde gasmetingen en allergietests, maar die komen niet altijd overeen met hoe patiënten zich voelen. Deze studie vraagt of nader kijken naar een specifiek type witte bloedcel in het bloed — de eosinofiel — artsen een beter venster kan geven op hoe goed de astmabehandeling werkelijk werkt.
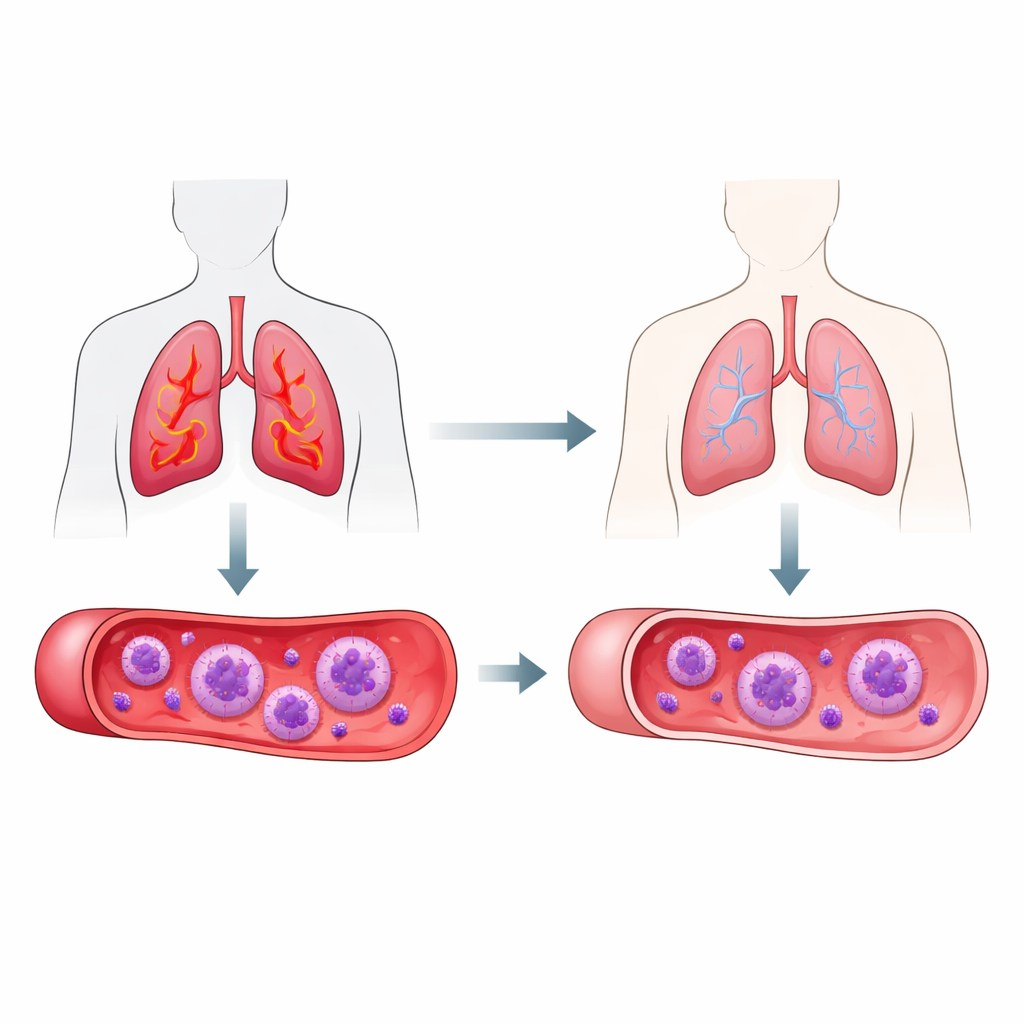
Voorbij de gebruikelijke astmacontroles kijken
Astma wordt aangedreven door chronische ontsteking in de luchtwegen, en eosinofielen behoren tot de belangrijkste betrokken cellen, vooral bij een veelvoorkomende vorm die type 2–hoog astma wordt genoemd. Standaardtests tellen vooral hoeveel eosinofielen aanwezig zijn, maar niet hoe actief ze zijn. De onderzoekers richtten zich op twee moleculen die op het oppervlak van eosinofielen kunnen verschijnen, genaamd CD63 en HLA-DR. Wanneer deze moleculen aanwezig zijn of verhoogd, signaleren ze dat de cellen meer "ingeschakeld" zijn en betrokken bij de immuunreactie. Het idee was dat, zelfs als het aantal eosinofielen hetzelfde blijft, veranderingen in deze oppervlakte-eigenschappen kunnen weerspiegelen of iemands astma beter onder controle komt.
Hoe de studie patiënten volgde tijdens behandelingstuning
Het team bestudeerde volwassenen met ernstig astma die werden geëvalueerd voor geavanceerde injecties gericht op eosinofielen. Voordat ze met deze biologische geneesmiddelen begonnen, doorliepen de patiënten een run-in periode van drie maanden in een gespecialiseerde polikliniek, waarin hun gebruikelijke behandeling zorgvuldig werd verfijnd volgens internationale richtlijnen. Dit hield in dat de inhalatietechniek werd gecontroleerd en dat medicatie werd opgehoogd indien nodig, zoals inhalatiecorticosteroïden, langwerkende bronchodilatoren, leukotrieenremmers en tiotropium. Aan het begin en het einde van deze periode maten de onderzoekers symptomen met de Asthma Control Test, registreerden aanvallen, controleerden longfunctie en namen bloed af om eosinofielen te analyseren met een hoogdetailtechniek genaamd flowcytometrie.
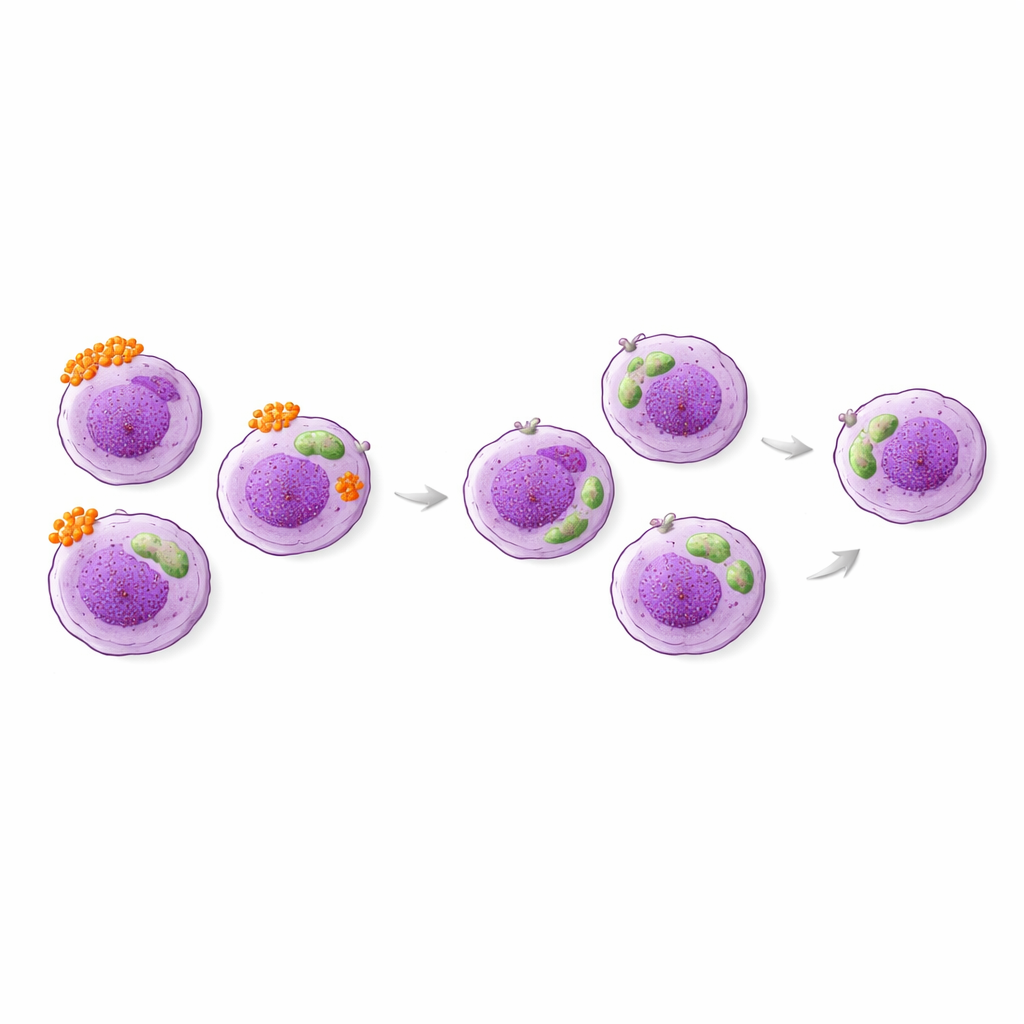
Wat in het bloed veranderde en wat niet
Na drie maanden geoptimaliseerde therapie voelden patiënten zich gemiddeld beter: hun scores op de controletest stegen, en het aandeel mensen met slecht gecontroleerd astma daalde van ongeveer de helft naar ongeveer één op de zes. Het gebruik van orale steroïdentabletten nam af, en astma-aanvallen werden minder frequent. Verrassend genoeg veranderden de eenvoudige tellingen van eosinofielen in het bloed weinig, en gebruikelijke markers zoals uitgeademd stikstofoxide en totaal IgE waren niet sterk gekoppeld aan de veranderingen in symptomen. Daarentegen daalde één van de oppervlakte-eigenschappen van eosinofielen — HLA-DR — duidelijk tijdens deze periode, zowel in hoeveel cellen het droegen als in de sterkte van de expressie. CD63, de andere activatiemarker, veranderde gemiddeld niet, maar neigde hoger te blijven bij patiënten van wie het astma slecht gecontroleerd bleef.
Het koppelen van celgedrag aan hoe patiënten zich voelen
Toen de wetenschappers nader keken, ontdekten ze dat patiënten die na behandelingstuning nog steeds hoge niveaus van HLA-DR en CD63 op hun eosinofielen hadden, meer kans hadden op aanhoudende symptomen. Statistische modellen suggereerden dat verschuivingen in HLA-DR, in het bijzonder, bescheiden samenhingen met verbeteringen in symptoomscores, ook al veranderde het totale aantal eosinofielen niet. Geen van beide markers kwam netjes overeen met de gebruikelijke bloedtellingen, uitgeademde gasniveaus of allergiemetingen, wat impliceert dat deze oppervlaktekenmerken een andere, meer kwalitatieve kant van de ziekte vastleggen. De auteurs benadrukken dat deze markers nog niet gebruikt moeten worden om te voorspellen wie op een bepaald geneesmiddel zal reageren, maar dat ze kunnen dienen als "associatieve" aanwijzingen dat de onderliggende ontsteking kalmeert — of actief blijft — ondanks standaardtherapie.
Wat dit kan betekenen voor mensen met moeilijk behandelbaar astma
De studie suggereert dat kijken naar hoe eosinofielen zich gedragen, in plaats van alleen hoeveel er zijn, kan helpen bij het personaliseren van astmazorg. Een daling van HLA-DR tijdens routinematige behandelingaanpassing kan aangeven dat conventionele inhalatiemedicatie de immuunactiviteit succesvol dempt, zelfs voordat grote veranderingen in symptomen optreden. Aan de andere kant kunnen eosinofielen die hoge niveaus van HLA-DR of CD63 blijven vertonen, patiënten signaleren van wie de ziekte blijft smeulen en die mogelijk baat hebben bij opschaling naar biologische therapieën of het kiezen van geneesmiddelen die andere routes targeten. Hoewel verder onderzoek nodig is voordat deze tests deel uitmaken van de dagelijkse kliniek, voegt het onderzoeken van de "persoonlijkheid" van eosinofielen een veelbelovende nieuwe laag toe aan het begrijpen en behandelen van ernstig astma.
Bronvermelding: Scarlata, S., Mazzuca, C., Vitiello, L. et al. Surface expression of CD63 and HLA-DR in circulating eosinophils correlates with improved clinical control after treatment optimization in asthma. Sci Rep 16, 8289 (2026). https://doi.org/10.1038/s41598-026-37906-z
Trefwoorden: ernstig astma, eosinofielen, biomarkers, gepersonaliseerde geneeskunde, flowcytometrie