Clear Sky Science · nl
Whole-cellmodellering voorspelt alternatieve strategieën voor proteoomallocatie in de archaeon Methanococcus maripaludis
Waarom kleine methaanmakers ertoe doen
Methanococcus maripaludis is een microscopische archaeon die eenvoudige chemicaliën zoals kooldioxide en formiaat omzet in methaan, een belangrijk bestanddeel van aardgas. Begrijpen hoe deze microbe haar interne middelen—vooral eiwitten—verdeelt, kan algemene levensregels onthullen voor omstandigheden met beperkte energie en kan richting geven aan pogingen om ze te benutten als biologische methaanfabriek of als platform voor groene chemie.
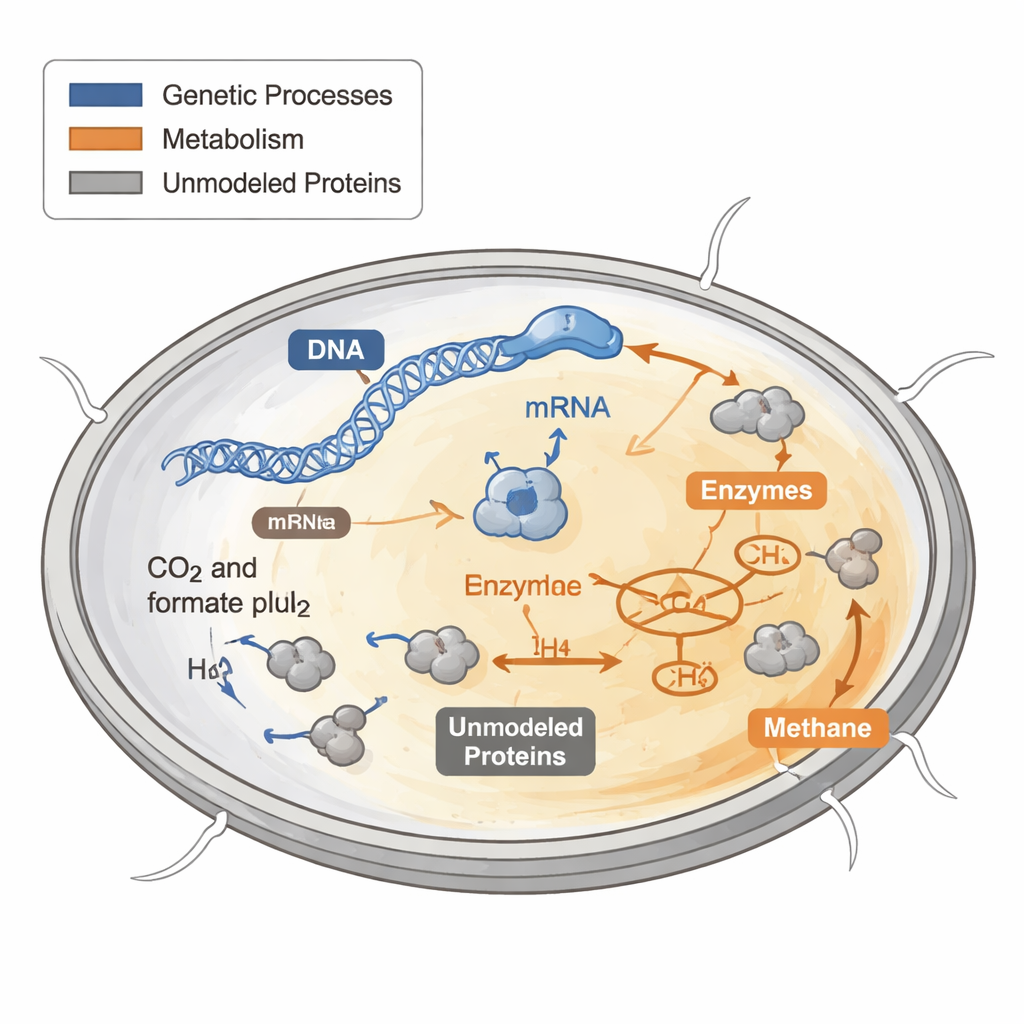
Hoe cellen hun eiwitbudget besteden
Elke cel moet beslissen hoe ze haar beperkte eiwit "budget" besteedt. Sommige eiwitten bouwen nieuwe celonderdelen, sommige winnen energie en andere vervullen onderhoudstaken. Eerdere computermodellen van metabolisme behandelden deze eiwitten alsof ze vrij en onbeperkt zijn, wat slecht werkt bij het voorspellen van groei onder zware of voedingsarme omstandigheden. Bij bacteriën en gist hebben experimenten aangetoond dat snelgroeiende cellen een groter aandeel van hun eiwitbudget aan ribosomen toewijzen—de moleculaire machines die nieuwe eiwitten maken—terwijl langzaam groeiende cellen middelen elders onderbrengen.
Een archaeon die de regels doorbreekt
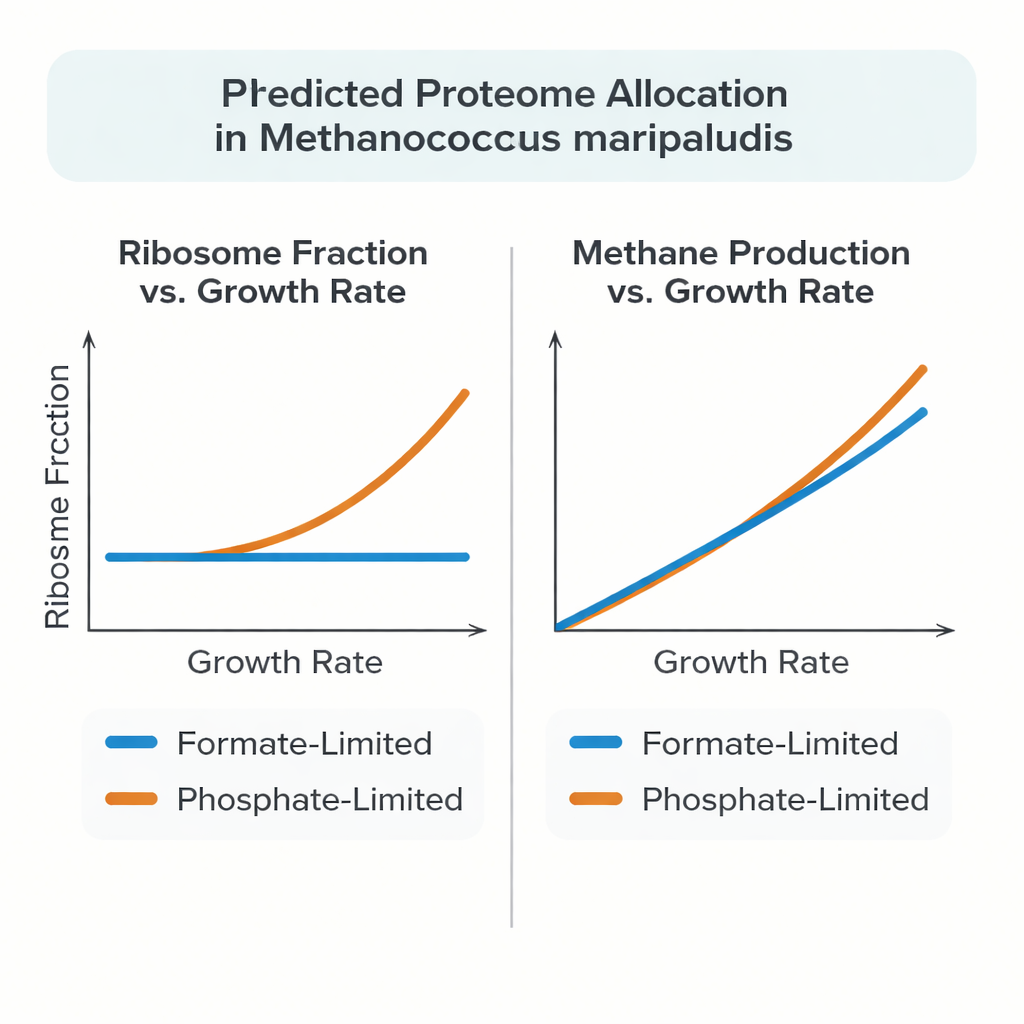
Recente experimenten toonden aan dat M. maripaludis niet altijd dit patroon volgt. Wanneer het groeit op formiaat als zowel voedings- als energiebron, blijft het aandeel van het eiwitbudget dat in ribosomen wordt geïnvesteerd bijna constant als de groei vertraagt. Onder fosfaatbeperking gedraagt de archaeon zich echter conventioneel: de ribosomale fractie stijgt met de groeisnelheid, vergelijkbaar met Escherichia coli en gist. Om dit ongebruikelijke gedrag te verklaren bouwden de auteurs een gedetailleerd whole-cell-achtig model dat metabolisme koppelt aan het kostbare proces van het maken en assembleren van eiwitten en RNA, in plaats van eiwitten te behandelen als abstracte reactietarieven.
Het opbouwen van een whole-cell-achtig model
De onderzoekers begonnen met een bestaande metabole kaart van M. maripaludis en voegden duizenden aanvullende reacties toe die genexpressie beschrijven: het kopiëren van DNA naar RNA, het laden van transfer-RNA's, het assembleren van ribosomen en enzymcomplexen, en het verdunnen van deze componenten tijdens celdeling. Ze verzamelden enzymsnelheidslimieten uit biochemische databases en literatuur, en schatten welk deel van de eiwitmassa bestaat uit "niet-gemodelleerde" eiwitten die niet rechtstreeks aan de reacties in de kaart gekoppeld zijn. Vervolgens legden ze globale beperkingen op die de totale massa van eiwit en RNA limiteren, reactietarieven koppelen aan de hoeveelheid beschikbaar enzym en de eiwitproductie binden aan ribosomale capaciteit. Met deze beperkingen moet het model kiezen hoe het een vast eiwitbudget verdeelt om groei te ondersteunen.
Wat de simulaties onthulden
Getest tegen hoogwaardige chemostaatexperimenten reproduceerde het model nauwkeurig gemeten eiwit- en RNA-massa's, methaanproductiesnelheden en groeiritmes over een reeks langzame groeisnelheden. Bij formiaatbeperking koos de gesimuleerde cel vanzelf voor een vrijwel constante fractie ribosomaal eiwit terwijl de groei varieerde, wat de experimentele gegevens weerspiegelde. Onder fosfaatbeperking kwam het model overeen met de waargenomen toename in ribosoomfractie alleen wanneer ribosomen bij lage groeisnelheden sneller mochten werken, consistent met metingen die aantonen dat meer ribosomen actief bij de eiwitsynthese betrokken zijn. Het model suggereerde ook dat een substantieel aandeel van de eiwitten in M. maripaludis niet strikt vereist is voor minimale groei, en dat overtollig koolstof en energie kunnen worden opgeslagen of omgeleid naar andere grote moleculen zoals glycogeen of vrije aminozuren, afhankelijk van welk nutriënt de beperkende factor is.
Mutanten en groeigrenzen onderzoeken
Omdat het model expliciet rekening houdt met de eiwitkosten van elk pad, kan het niet alleen voorspellen of genetische mutanten groeien, maar ook hoe goed ze groeien ten opzichte van het wildtype. De auteurs simuleerden stammen die verschillende waterstofverwerkende enzymen misten en vergeleken de voorspelde fitheid met laboratoriummetingen onder meerdere groeicondities, inclusief de aanwezigheid of afwezigheid van waterstof en koolmonoxide. In veel gevallen voorspelde het model of mutanten konden groeien en gaf het redelijke schattingen van hun relatieve groeisnelheden, een verbetering ten opzichte van eerdere modellen die alleen ja-of-nee-antwoorden konden geven. Hetzelfde kader werd gebruikt om maximale mogelijke groeisnelheden onder batchcondities voor verschillende substraatcombinaties te schatten.
Wat dit betekent voor wetenschap en technologie
In gewone taal laat deze studie zien dat M. maripaludis een alternatieve strategie gebruikt om haar eiwitpersoneel te budgetteren, waarbij ze haar eiwitfabrieken onder sommige omstandigheden op een constant aandeel van het budget laat draaien in plaats van ze terug te schroeven wanneer de groei vertraagt. Door dat gedrag in een gedetailleerd, data-gedreven model te verankeren, biedt het werk een testomgeving om te onderzoeken hoe energiebeperkte microben groei, onderhoud en opslag in evenwicht brengen. Voor toegepast onderzoek biedt het model een routekaart om deze archaeon te ontwerpen om meer methaan of andere producten te maken door te identificeren welke enzymen en paden het meest kostbaar zijn qua eiwitinvestering. Breder gezien breidt het krachtige whole-cell-achtige modellering uit voorbij bacteriën en gist naar het archaeale domein, en helpt het de kloof te overbruggen tussen de moleculaire details en het grootschalige gedrag van microbiële gemeenschappen die betrokken zijn bij klimaat, energie en industriële biotechnologie.
Bronvermelding: Kasem, G.S., Soliman, T.H.A., Mousa, M.A.A. et al. Whole-cell modeling predicts alternative proteome allocation strategies in the archaeon Methanococcus maripaludis. Sci Rep 16, 7386 (2026). https://doi.org/10.1038/s41598-026-37887-z
Trefwoorden: Methanococcus maripaludis, proteoomallocatie, whole-cellmodellering, methanogenese, archaea metabolisme