Clear Sky Science · nl
SARS-CoV-2-nucleocapside-eiwit vormt complexen met oplosbare complementregulerende eiwitten die aan het virion kunnen binden
Waarom deze verborgen virale truc ertoe doet
De meesten van ons hebben gehoord van het coronavirus‑“spike”‑eiwit, omdat dat het belangrijkste doelwit van vaccins is. Maar binnenin het virus zit een ander eiwit, het nucleocapside‑ of N‑eiwit, dat veel meer blijkt te zijn dan louter structurele verpakking. Deze studie laat zien dat het N‑eiwit zich kan vasthechten aan belangrijke menselijke immuunregulatoren in het bloed en die naar het virusoppervlak kan vervoeren. Daarmee kan SARS‑CoV‑2 één van onze vroegste verdedigingssystemen—het complementsysteem—gedeeltelijk uitschakelen, het virus laten overleven en mogelijk bijdragen aan ernstige COVID‑19.
Een nadere blik op het binnenste eiwit van het virus
Het N‑eiwit is de ‘wikkel’ van het virale genoom en helpt het RNA te verpakken en te stabiliseren. Artsen hebben hoge niveaus van N‑eiwit in het bloed gevonden bij patiënten met COVID‑19, vooral bij ernstige gevallen, en eerder onderzoek suggereert dat het ontstekingssignalen kan opwekken. De auteurs vroegen zich af of N ook het complement zou kunnen beïnvloeden, een netwerk van bloedproteïnen dat indringers markeert voor vernietiging en gaten in microben kan slaan. Veel virussen hebben sluwe methoden ontwikkeld om de complementregulatoren van het lichaam te lenen of na te bootsen om aanval te vermijden. Het team stelde drie vragen: bindt N aan het spike‑eiwit en aan het virus zelf, bindt het aan menselijke complementregulerende eiwitten in bloed, en kan het deze regulatoren naar het virusoppervlak transporteren?
Hoe N en spike elkaar op het virus ontmoeten
Met verschillende eiwitbindtests toonden de onderzoekers aan dat het N‑eiwit rechtstreeks aan het spike‑eiwit kan kleven, zowel wanneer spike in het lab is gemaakt als wanneer het op echte SARS‑CoV‑2‑deeltjes voorkomt. Ze bevestigden deze interactie in diverse experimentele opstellingen en maten de bindingssterkte, en vonden een affiniteit vergelijkbaar met die van veel antilichamen. Door het spike‑eiwit in fragmenten te knippen en te identificeren welke stukken aan N bleven zitten, brachten ze waarschijnlijke contactzones in kaart, grotendeels in het N‑terminaal domein van spike, een regio die al bekendstaat als een hotspot voor antilichaambinding en voor het aangrijpen van bepaalde gastheermoleculen. Dit suggereert dat N een sterke, biologisch relevante brug naar spike op werkelijke virions kan vormen.
Het kapen van de eigen veiligheidsremmen van het lichaam
Het complementsysteem wordt strak gecontroleerd door oplosbare “remmen” die complementregulerende eiwitten heten en onze eigen cellen beschermen tegen vriendelijke vuur. Het team richtte zich op vier van deze — C1‑inhibitor, C4‑bindingsproteïne, factor H en vitronectine — omdat zij op verschillende stadia van de complementcascade werken. In op serum‑gebaseerde tests en zuivere‑eiwitassays bond het N‑eiwit aan alle vier de regulatoren, terwijl spike onder dezelfde voorwaarden niet aan hen bond. Dit betekent dat N–CRP‑complexen in plasma kunnen ontstaan. Cruciaal was dat wanneer N vooraf met menselijk serum werd gemengd en daarna aan virusdeeltjes werd blootgesteld, de onderzoekers deze regulerende eiwitten aan de virions detecteerden—maar alleen wanneer N aanwezig was. Hoe meer N ze gebruikten, hoe meer complementregulatoren op het virus verschenen, wat wijst op een dosisafhankelijke rekruteringsmechaniek. 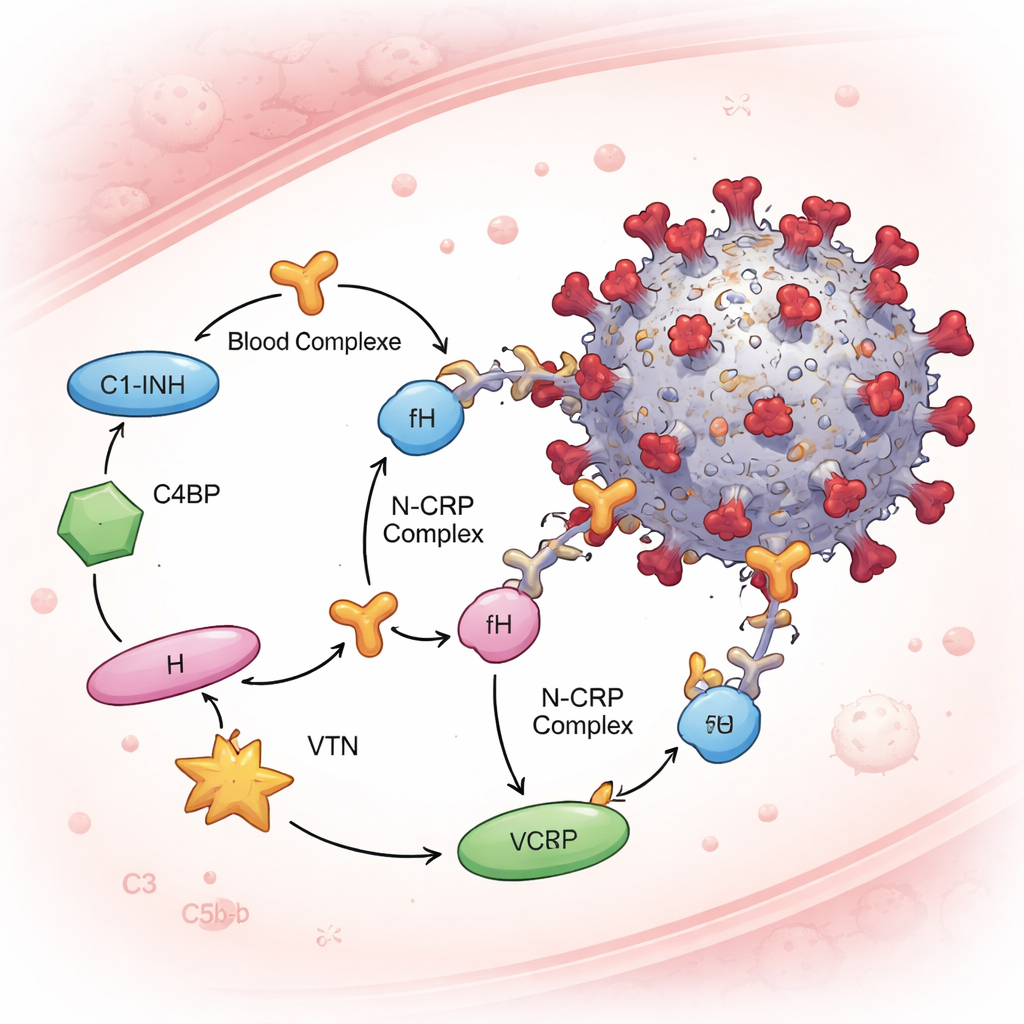
Het dempen van de laatste aanvalsstap
Het ultieme wapen van het complementsysteem is het membraan‑aanvalcomplex (MAC), een ringachtige structuur die poriën vormt in cel‑ of virusomhulsels. De auteurs onderzochten of N de MAC‑vorming op SARS‑CoV‑2 kon beïnvloeden. Ze incubeerden gezuiverd virus met menselijk serum, met of zonder toegevoegd N‑eiwit, en maten vervolgens hoeveel van het MAC‑component C5b‑9 op de virions belandde. Zonder N stapelde het virus C5b‑9 op, wat wijst op actieve complementaanval. Wanneer N aanwezig was, daalde de MAC‑depositie op concentratieafhankelijke wijze: meer N betekende minder C5b‑9 op het virus. Dit past bij het idee dat N, door het virion te decoreren met complementregulatoren, het beschermt tegen het inslaan van poriën. 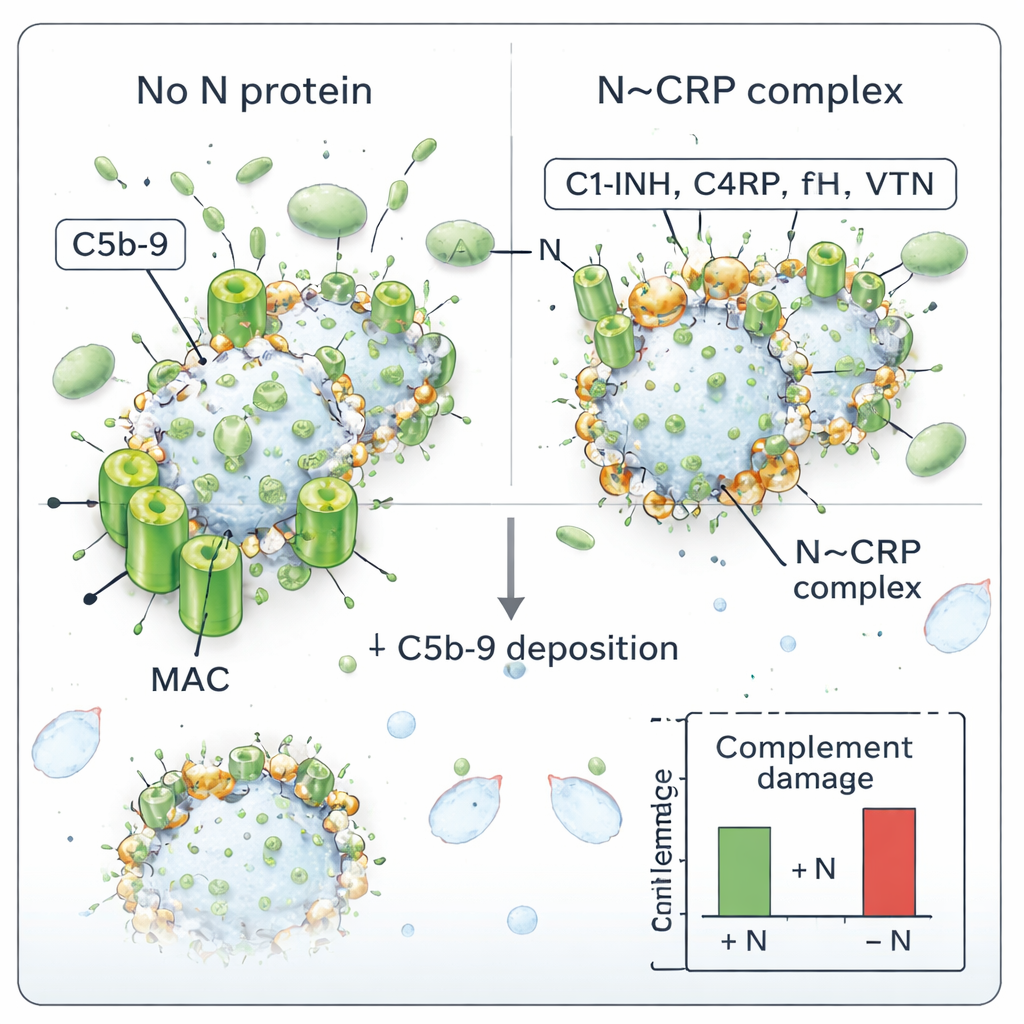
Wat dit betekent voor patiënten en toekomstige therapieën
Voor niet‑specialisten is de kernboodschap dat SARS‑CoV‑2 niet alleen op zijn beroemde spike vertrouwt om het immuunsysteem te slim af te zijn. Zijn interne N‑eiwit kan in de bloedbaan terechtkomen, de complement‑“remmen” van het lichaam grijpen en die terugbrengen naar het virusoppervlak. Daar kunnen ze het virus helpen verbergen voor een krachtige tak van de aangeboren immuniteit en directe complementgemedieerde schade verminderen. Dit kan zowel bijdragen aan persisterende infectie als aan de verwarde complementafwijkingen die bij ernstige COVID‑19 worden gezien. Hoewel deze experimenten in gecontroleerde laboratoriumomstandigheden zijn uitgevoerd, benadrukken ze N–complementinteracties als een potentieel nieuw doelwit: therapieën die verhinderen dat N aan deze regulatoren bindt, of die de complementactiviteit weer in balans brengen, zouden op den duur kunnen helpen het gevecht in het voordeel van het immuunsysteem te beslechten.
Bronvermelding: Víglaský, J., Bhide, K., Talpasova, L. et al. SARS-CoV-2 nucleocapsid protein forms complexes with soluble complement regulatory proteins that can bind to the virion. Sci Rep 16, 6599 (2026). https://doi.org/10.1038/s41598-026-37866-4
Trefwoorden: SARS-CoV-2 nucleocapside, complementsysteem, immuunontwijking, complementregulerende eiwitten, ernst van COVID-19