Clear Sky Science · nl
Het mTOR-signaleringspad reguleert sleutelstappen van de ontwikkeling van mammaklierorganoïden op een tijdgebonden manier
Waarom kleine borstmodellen ertoe doen
Onze borsten behoren tot de weinige organen die zichzelf herhaaldelijk herbouwen: ze groeien tijdens de puberteit en zwangerschap, produceren melk en krimpen daarna weer terug na het geven van borstvoeding. Begrijpen hoe deze complexe herstructurering wordt gestuurd is cruciaal voor de gezondheid van vrouwen, van succes bij borstvoeding tot het risico op kanker. Deze studie gebruikt miniatuurlijke driedimensionale "mini-borstjes", organoïden genoemd, gekweekt uit muizencellen om te laten zien hoe een hoofdschakelaar voor groei in cellen, bekend als het mTOR-pad, het timen en vormen van de ontwikkeling van mammair weefsel bepaalt.
Een cellulaire verkeerslicht voor groei
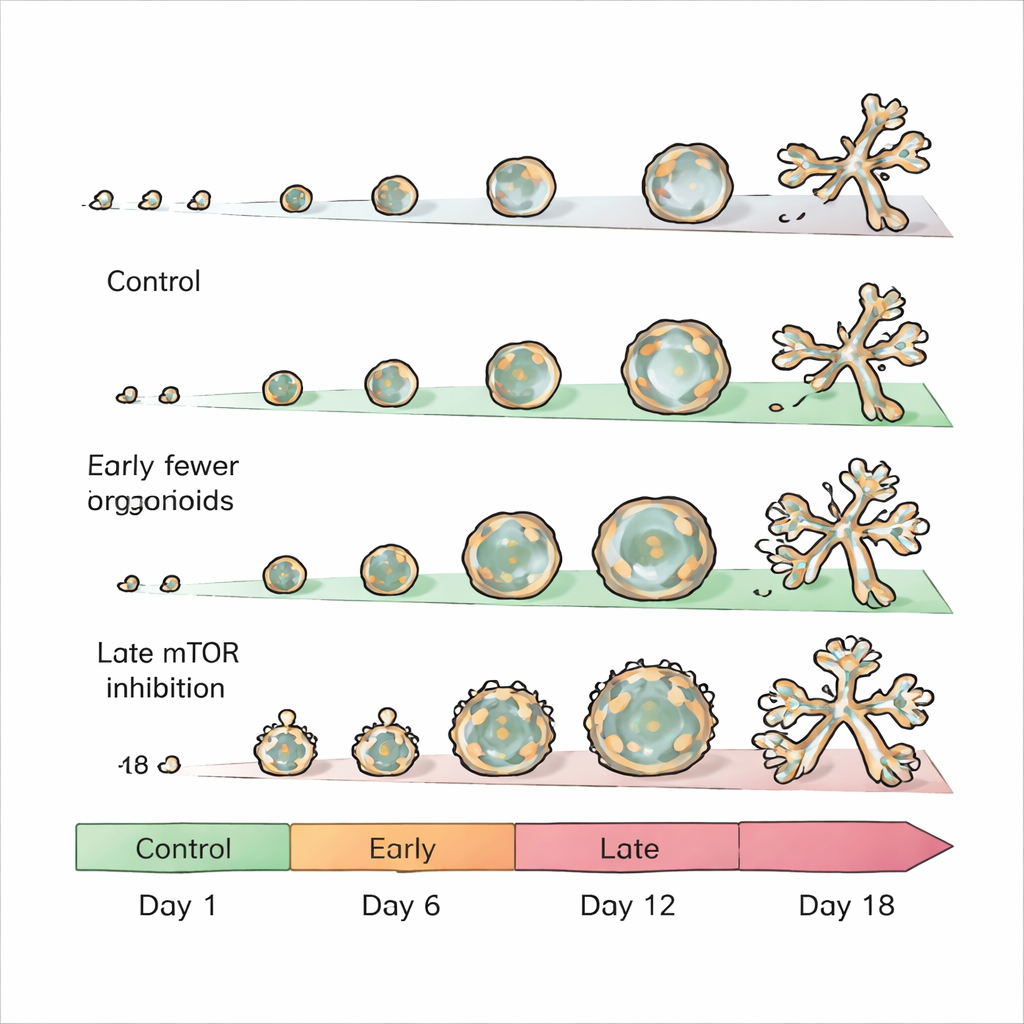
mTOR is een centraal regelmechanisme dat cellen helpt beslissen wanneer ze moeten groeien, delen en hun stofwisseling moeten aanpassen. De onderzoekers wilden weten hoe het uitschakelen van deze schakelaar op verschillende momenten de ontwikkeling van organoïden zou beïnvloeden. Ze lieten muis mammacellulaire epitheelcellen groeien in een gel die hen in staat stelt zichzelf te organiseren tot structuren die lijken op kleine melkgangetjes met een holle kern en soms vertakte, "druifachtige" clusters. Vervolgens gaven ze bekende mTOR-remmers, rapamycine en torin 1, ofwel zeer vroeg, halverwege de groei of later, wanneer vertakking gewoonlijk begint.
Vroege ingreep: mini-organen die nooit echt gevormd worden
Wanneer mTOR vanaf de allereerste dag werd geblokkeerd, groeiden de organoïden vrijwel niet. Hun diameter werd met ongeveer twee derde of meer gereduceerd, wat aangeeft dat actief mTOR essentieel is voor de vroege expansie van mammair weefsel. Dit sluit aan bij mTOR’s reputatie als aanjager van celgroei en eiwitsynthese. Omdat deze organoïden zo klein en onderontwikkeld bleven, richtte het team zich op latere behandelingsvensters, waar de effecten genuanceerder waren en inzicht gaven in hoe de interne architectuur van het weefsel wordt gecontroleerd.
Wijziging halverwege: holle sferen en verloren flexibiliteit
Het blokkeren van mTOR vanaf ongeveer dag 6—nadat de beginstructuren waren gevormd maar vóór vertakking—leverde onverwacht grote, grotendeels holle organoïden op. Deze werden gedomineerd door luminale cellen, de binnenste cellen die normaal de melkafscheidende kanalen bekleden, terwijl de buitenste basale cellaag vrijwel volledig verdween. In gezonde ontwikkeling kunnen individuele luminale of basale cellen elk organoïden voortbrengen die beide celtypen bevatten; deze eigenschap staat bekend als lineageplasticiteit. mTOR-remming in dit middenstadium bevroren deze flexibiliteit in wezen, waarbij cellen werden gedwongen een luminale identiteit aan te nemen en de gebruikelijke balans van lagen werd verhinderd. Moleculaire analyses toonden wijdverspreide veranderingen in gen- en eiwitniveaus, in het bijzonder verlagingen in onderdelen van de cellulaire metabole machinerie en in eiwitten die helpen bij het herschikken van de omringende ondersteunende matrix—veranderingen die het gewijzigde vorm- en celbestand helpen verklaren.
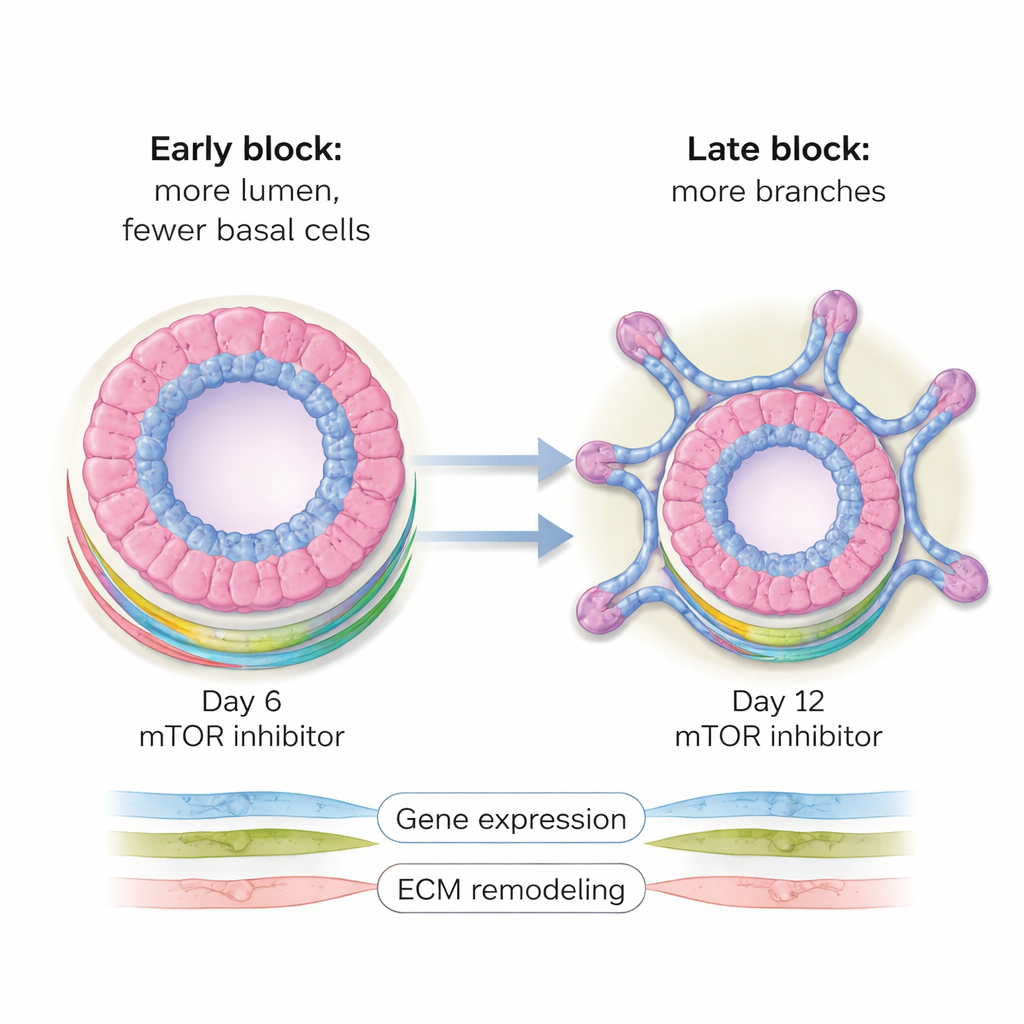
Late onderbreking: meer vertakkingen, andere bedrading
Wanneer dezelfde middelen later werden toegevoegd, rond dag 12, precies wanneer vertakking typisch begint, keerde het resultaat om. In plaats van vergrote holle sferen vormden de organoïden nu meer—en complexere—vertakte knopachtige structuren die leken op de kleine zakjes waar melk wordt geproduceerd. In deze situatie bleef de balans tussen luminale en basale cellen grotendeels behouden, maar nam het aantal vertakkingen en knopjes aanzienlijk toe in vergelijking met niet-behandelde controles. Patronen in genactiviteit weerspiegelden deze verschuiving: veel genen die gekoppeld zijn aan weefselvorming en vertakking waren hoger afgesteld, terwijl veel genen die betrokken zijn bij metabolisme juist lager werden afgesteld. Metingen op eiwitniveau echoën deze bevindingen en benadrukken veranderingen in componenten van de extracellulaire matrix en in metabole routes, met name aminozuur- en energiegebruik.
Wat dit betekent voor echte borsten
Samengevat laat het werk zien dat mTOR geen simpele aan-uitgroeiknop is, maar een tijdgevoelige coördinator van zowel celidentiteit als weefselarchitectuur in de mammaklier. In een vroeg stadium is actief mTOR nodig zodat cellen kunnen groeien en de flexibiliteit behouden om zowel luminale als basale cellen te worden. Later herschikt verandering in mTOR-activiteit hoe cellen met hun omgeving omgaan om ofwel de vorming van vertakte melkproducerende structuren af te zwakken ofwel te versterken. Voor leken is de kernboodschap dat hetzelfde moleculaire pad heel verschillende taken kan hebben afhankelijk van het tijdstip waarop het actief is—eerst helpt het de juiste soorten cellen te vormen, daarna helpt het die cellen in de juiste driedimensionale vorm te boetseren. Dit genuanceerde beeld is belangrijk voor het begrijpen van normale borstvoedingontwikkeling, de impact van geneesmiddelen die mTOR-targeten en mogelijk hoe vroege veranderingen in dit pad kunnen bijdragen aan borstziekten.
Bronvermelding: Lacouture, A., Sylla, M.S., Germain, L. et al. The mTOR signaling pathway regulates key steps of mammary gland organoid genesis in a temporal manner. Sci Rep 16, 6751 (2026). https://doi.org/10.1038/s41598-026-37825-z
Trefwoorden: ontwikkeling van de mammaklier, mTOR-signaleringspad, organoïden, vertakkingsmorfogenese, borstbiologie