Clear Sky Science · nl
COL8A1 bevordert de progressie van prostaatkanker door tumorimmuuninfiltratie te moduleren en het FAK/PI3K/AKT-pad te activeren via regulatie van ADAMTS2
Waarom dit onderzoek ertoe doet
Prostaatkanker is een van de meest voorkomende vormen van kanker bij mannen, maar artsen hebben nog steeds moeite te voorspellen wie een agressieve ziekte zal ontwikkelen en hoe die het beste kan worden tegengegaan. Deze studie onthult hoe een weinig bekend structureel eiwit, COL8A1, prostaattumoren helpt groeien, uitzaaien en in wisselwerking treden met het immuunsysteem van het lichaam. Inzicht in deze verborgen drijver kan de deur openen naar nauwkeurigere tests en nieuwe gerichte behandelingen.
Een structureel eiwit met een donkere kant
COL8A1 maakt deel uit van collageen, het geraamte dat onze weefsels bijeenhoudt. Normaal bevindt het zich in bloedvat- en ondersteunende cellen en onderhoudt het stilletjes de structuur. De onderzoekers gebruikten grote openbare kankerdatabases en monsters van mannen die een prostaatoperatie ondergingen om een simpele vraag te stellen: is COL8A1 veranderd bij prostaatkanker? Ze ontdekten dat COL8A1-niveaus veel hoger waren in tumweefsel dan in nabijgelegen gezond prostaatweefsel, en dat patiënten met de hoogste niveaus vaak een gevorderdere ziekte, hogere Gleason-scores en kortere periodes hadden voordat hun kanker verslechterde. Dit patroon bleef bestaan zelfs bij mannen met lage PSA-waarden, wat suggereert dat COL8A1 gevaarlijke tumoren kan aanwijzen die huidige bloedtests missen.
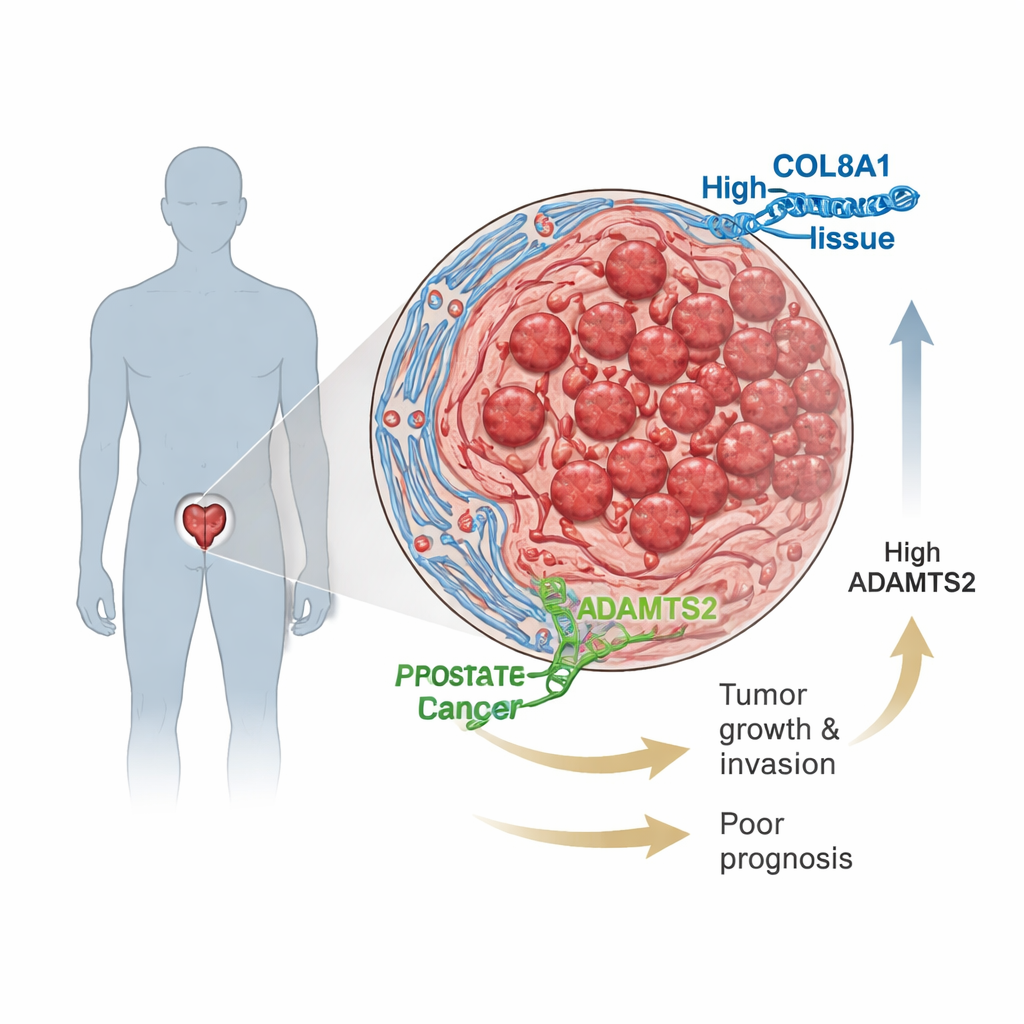
Van petrischaal naar levende muizen
Om te zien wat COL8A1 daadwerkelijk doet, manipuleerde het team de niveaus ervan in in het lab gekweekte prostaatkankercellen. Wanneer ze de cellen dwongen meer COL8A1 te produceren, deelden de cellen sneller, bewogen makkelijker, drongen ze door kunstmatige barrières en ondergingen ze minder vaak geprogrammeerde celdood. Het verlagen van COL8A1 had het tegenovergestelde effect: de groei vertraagde, invasie nam af en meer cellen stierven. Dit zijn allemaal kenmerken van respectievelijk agressievere of minder agressieve kankercellen. De wetenschappers implanteerden vervolgens prostaatkankercellen met of zonder COL8A1 in muizen. Tumoren zonder COL8A1 groeiden veel langzamer en waren kleiner, wat bevestigt dat dit eiwit tumorgroei in levende organismen bevordert.
Een moleculair partner in misdaad
Dieper gravend, zochten de onderzoekers naar andere genen die sterk met COL8A1 samenhang vertonen in prostaattumoren. Eén gen, ADAMTS2, viel op. ADAMTS2 is een enzym dat de weefselomgeving rond cellen herstructureert. Zowel in patiëntendatasets als in ziekenhuismonsters was ADAMTS2 verhoogd in prostaattumoren en geassocieerd met slechtere klinische kenmerken en uitkomsten. In kankercellen verhoogde het stimuleren van COL8A1 het ADAMTS2-eiwit, terwijl het verlagen van COL8A1 dit eiwit deed dalen, ook al bleef het genetische bericht (mRNA) van ADAMTS2 gelijk. Dit suggereert dat COL8A1 het ADAMTS2-eiwit beschermt of stabiliseert. Experimenten bevestigden dat de twee eiwitten fysiek aan elkaar binden. Wanneer het team ADAMTS2 onderdrukte, verzwakten veel van de agressieve eigenschappen die door COL8A1 werden getriggerd, wat aantoont dat ADAMTS2 een belangrijke tussenpersoon is in deze schadelijke route.
Een krachtig groeicircuit inschakelen
De studie laat ook zien hoe dit COL8A1–ADAMTS2-duo communiceert met de kern van de groeimachinerie in de cel. Met behulp van computeranalyses en eiwitmetingen toonden de auteurs aan dat hoge COL8A1 samenhangt met activatie van een bekend signaalpad binnen cellen, het FAK/PI3K/AKT-pathway. Dit pad geeft kankercellen instructies om te overleven, te delen, te bewegen en weerstand tegen celdood te bieden. Extra COL8A1 verhoogde het "aan"-signaal (gefosforyleerde vormen) van FAK, PI3K en AKT, terwijl het verwijderen van COL8A1 dit signaal dempte. Belangrijk is dat het verstoren van ADAMTS2 dit signaal gedeeltelijk afzwakte, zowel in gekweekte cellen als in muizen tumoren. Gezamenlijk schetsen de data een duidelijke route: COL8A1 bindt en stabiliseert ADAMTS2, dat op zijn beurt helpt het FAK/PI3K/AKT-schakelaartje om te zetten dat de progressie van prostaatkanker aanjaagt.
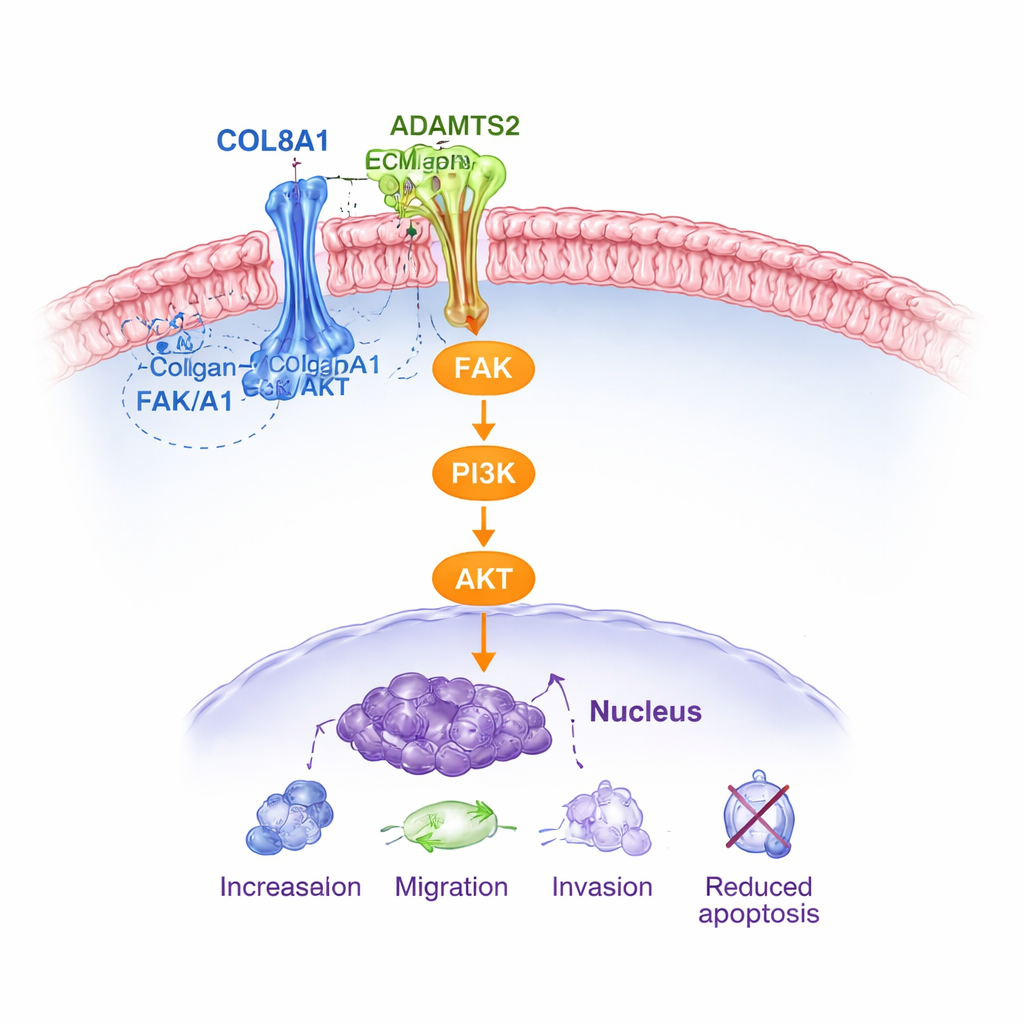
De immuunomgeving hervormen
Voorbij de kankercellen zelf keek het team naar het omliggende immuunlandschap. Door tumoren met hoge versus lage COL8A1 te vergelijken in een grote patiëntengroep, vonden ze dat hoge COL8A1 gepaard ging met sterkere infiltratie door verschillende immuunceltypen, waaronder macrofagen en bepaalde T-cellen die in verband zijn gebracht met slechtere uitkomsten bij prostaatkanker. Hoewel de studie nog niet bewijst dat COL8A1 deze cellen direct aantrekt of herprogrammeert, suggereert het dat dit eiwit helpt een immuunomgeving te vormen die uiteindelijk de tumor in de kaart speelt.
Wat dit betekent voor patiënten
In toegankelijke termen laat dit onderzoek zien dat COL8A1 meer is dan een passief bouwblok: bij prostaatkanker gedraagt het zich als een medeplichtige die het lokale weefsel verstijft, een schadelijk enzym stabiliseert en groeisignalen in tumcellen inschakelt, terwijl het ook geassocieerd is met een vijandigere immuunomgeving. Omdat hoge COL8A1 en ADAMTS2 betrouwbaar wijzen op agressievere ziekte, zouden ze kunnen dienen als nieuwe biomarkers om risicovoorspelling verder te verfijnen naast alleen PSA. Nog veelbelovender zijn medicijnen die de COL8A1–ADAMTS2‑verbinding verbreken of het downstream FAK/PI3K/AKT‑pad blokkeren; die zouden op termijn de tumorgroei en -uitzaaiing kunnen vertragen en mannen met hoogrisico- of behandelingsresistente prostaatkanker nieuwe opties kunnen bieden die zijn geworteld in de biologie van hun ziekte.
Bronvermelding: Wang, J., Ning, J., Xu, L. et al. COL8A1 promotes prostate cancer progression via modulating tumor immune infiltration and activating the FAK/PI3K/AKT pathway through ADAMTS2 regulation. Sci Rep 16, 6744 (2026). https://doi.org/10.1038/s41598-026-37799-y
Trefwoorden: prostaatkanker, COL8A1, ADAMTS2, tumormicro-omgeving, PI3K AKT-signaalgeving