Clear Sky Science · nl
Computationele strategieën om inzichten uit bekende remmers te ontsluiten voor verdere leidoptimalisatie: Een casestudy van celecoxib-analogen
Waarom kleine wijzigingen in pijnstillers ertoe doen
Moderne pijnstillers dempen niet alleen pijn; ze verfijnen de chemie van het lichaam op zeer precieze manieren. Celecoxib, een veelgebruikt ontstekingsremmend middel, richt zich op een enzym dat betrokken is bij pijn en zwelling, terwijl een verwant enzym dat de maag beschermt grotendeels ongemoeid wordt gelaten. Toch gedragen tientallen nauwe chemische familieleden van celecoxib zich in het lichaam heel anders. Deze studie gebruikt computermodellen om een schijnbaar eenvoudige vraag met grote implicaties voor veiligere geneesmiddelen te stellen: hoeveel betekent een enkele kleine wijziging in een molecuul?
Het enzym dat pijn activeert
Wanneer weefsel beschadigd of ontstoken is, geeft het lichaam een vetmolecuul genaamd arachidonzuur vrij. Een enzym genaamd COX-2 zet dit molecuul om in prostaglandinen, die pijn, koorts en zwelling veroorzaken. Een verwant enzym, COX-1, helpt de maagwand en bloedplaatjes te beschermen. Oudere pijnstillers zoals ibuprofen pakken beide enzymen aan, waardoor pijn afneemt maar de maag vaak geïrriteerd raakt. Celecoxib is ontworpen om in een iets grotere holte te glijden die vooral in COX-2 voorkomt, waardoor pijnsignalen worden geblokkeerd terwijl het beschermende werk van COX-1 grotendeels blijft. Het begrijpen van de gedetailleerde vorm van deze holte en hoe geneesmiddelmoleculen daarin liggen, is cruciaal voor het ontwerpen van nieuwe middelen die zowel krachtig als veilig zijn.
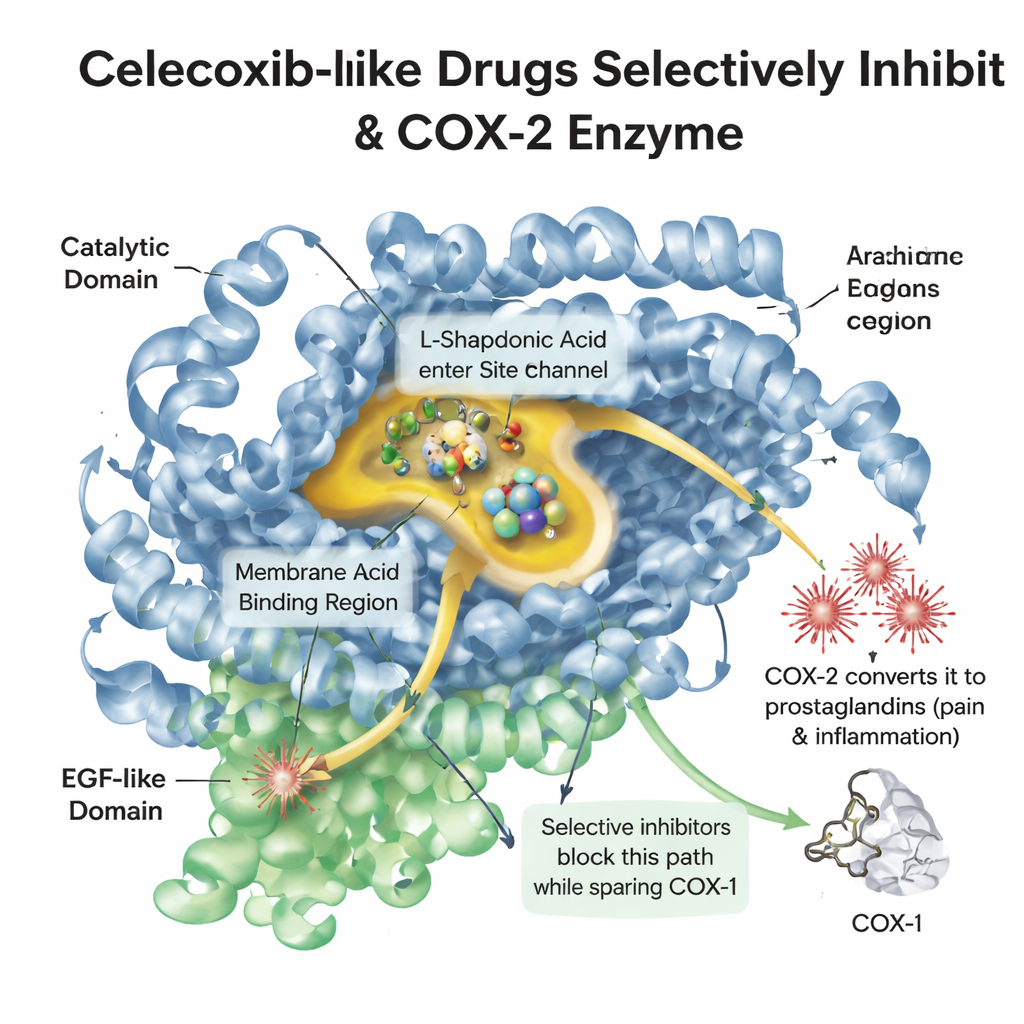
Een digitale bibliotheek van gelijkaardige middelen
De onderzoekers stelden een set samen van 375 moleculen die allemaal het basale dreringenraamwerk van celecoxib delen maar op kleine punten verschillen, bijvoorbeeld door één atoom of zijgroep te verwisselen. Ze haalden deze structuren en hun gemeten COX-2-remmende sterktes uit een openbare geneesmiddeldatabase. Met chemiesoftware maakten ze 3D-modellen van elk molecuul, berekenden bijna 2.000 numerieke descriptoren van hun vormen en eigenschappen, en plaatsten ze vervolgens in dockingprocedures in een hoge-resolutie structuur van het COX-2-enzym. Bij docking duwt een computer een molecuul op veel manieren in de holte van het enzym en waardeert hoe nauw elk pose past.
Wat echt sterkte en selectiviteit bepaalt
Het team zoomde in op drie sleutelregio’s van celecoxib. "Site-1" is een ring die in een vetachtige plek van de holte zit; "Site-2" is een ring met een fluorhoudende staart; en "Site-3" is een ring met een sulfonamidegroep die sterke waterstofbruggen vormt. Hun analyse toonde aan dat Site-1 de voorkeur geeft aan kleine, niet-polaire groepen die hydrofobe contacten behouden; deze regio meer wateraantrekkend maken, bijvoorbeeld door een –OH- of zuurgroep toe te voegen, verzwakte het geneesmiddel doorgaans. Bij Site-2 scherpten kleine elektronegatieve groepen zoals fluor vaak de potentie aan door interacties in een strakke holte te verbeteren, terwijl grotere of meer polaire staarten de activiteit juist schaden. Bij Site-3 was de stikstof van de sulfonamide, die een waterstofbrug kan doneren, cruciaal; vervanging door een niet-bindende versie verminderde de binding merkbaar.
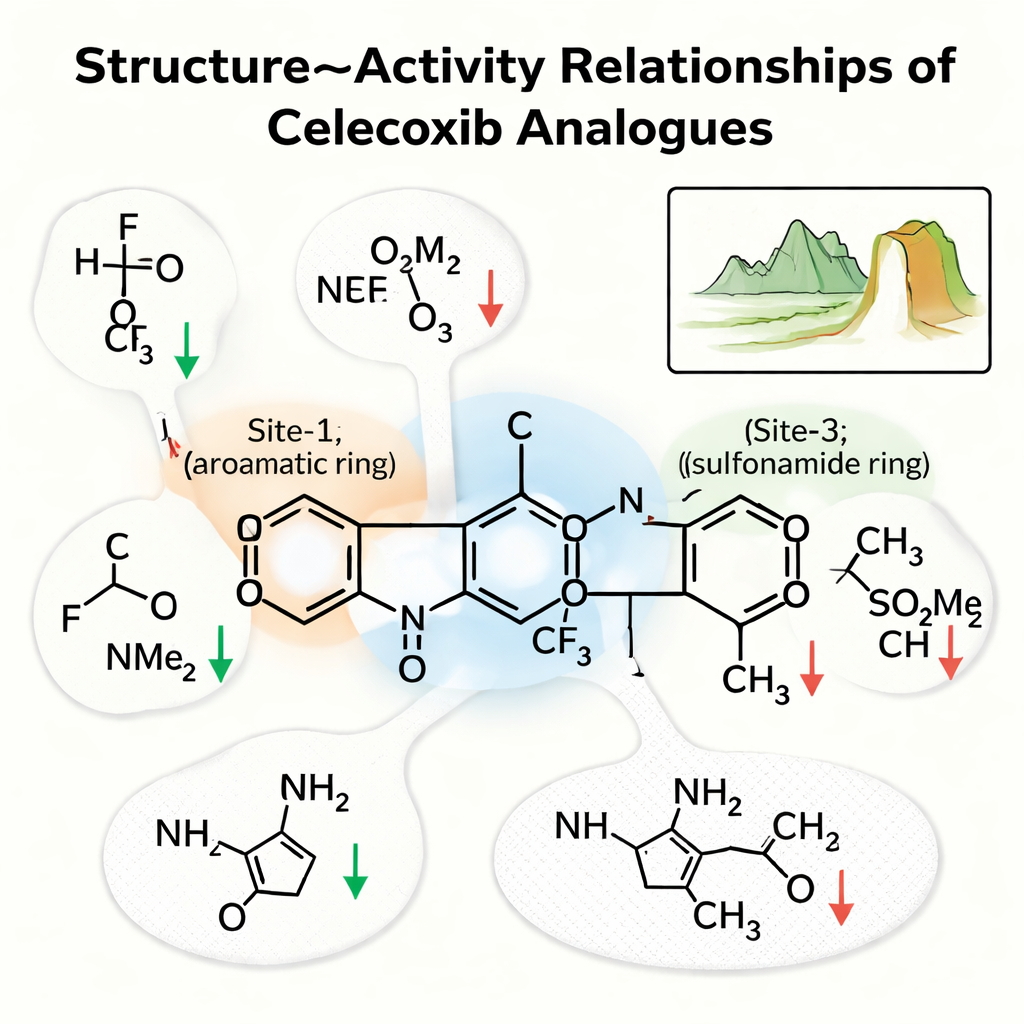
Kliffen in het chemische landschap
Om verder te gaan dan eenvoudige trends bouwden de auteurs een "structuur–activiteitslandschap", dat onderzoekt hoeveel de sterkte van een middel verandert wanneer de structuur maar een beetje wijzigt. In dit beeld liggen de meeste celecoxib-achtige verbindingen op zachte heuvels: ze subtiel aanpassen — bijvoorbeeld door een halogeen te verplaatsen of een kleine flexibele groep toe te voegen — verplaatst de potentie voorspelbaar omhoog of omlaag. Maar enkele paren vormen scherpe "activiteitskliffen", waar een kleine wijziging, zoals het vervangen van een methylgroep door een trifluormethylgroep of het toevoegen van één fluoratoom, een dramatisch verlies of winst aan activiteit veroorzaakt. De studie voerde ook volledige moleculaire dynamicasimulaties uit — virtuele films van geneesmiddel–enzymcomplexen in beweging — die bevestigden dat de beste analogen stabiel in de holte blijven zitten over honderden nanoseconden.
De volgende generatie veiligere pijnstillers sturen
Voor niet‑specialisten is de kernboodschap dat in medicijnontwerp kleine details enorm belangrijk zijn. Twee verbindingen die op papier bijna identiek lijken, kunnen duizendvoudig verschillen in hoe sterk ze COX-2 blokkeren, simpelweg omdat één extra atoom de passing in een microscopische holte verbetert of een cruciaal contact verstoort. Door systematisch in kaart te brengen welke wijzigingen per celecoxib‑site helpen of schaden, en door de gevaarlijke "kliffen" te benadrukken waar kleine aanpassingen buitensporige effecten hebben, biedt dit computationele werk een routekaart voor chemici. Het wijst de weg naar nieuwe ontstekingsremmers die de pijnstillende kracht van celecoxib behouden en tegelijkertijd veiligheid en selectiviteit verder verbeteren.
Bronvermelding: Grewal, S., Ghosh, B., Narayan, U. et al. Computational strategies for unraveling insights from known inhibitors for further lead optimization: A case study on Celecoxib analogues. Sci Rep 16, 6720 (2026). https://doi.org/10.1038/s41598-026-37798-z
Trefwoorden: COX-2-remmers, celecoxib-analogen, ontstekingsremmende geneesmiddelen, computationeel medicijnontwerp, structuur-activiteitrelaties