Clear Sky Science · nl
Exosomaal miR-25-3p afkomstig van humane amnionepitheelcellen verhoogt mucine-expressie in conjunctivale gobletcellen via downregulatie van BCL2L11
Waarom een gladder oogoppervlak ertoe doet
Ieder die heeft geworsteld met droge, krassende ogen weet hoe belangrijk een gezonde traanfilm is voor helder en comfortabel zicht. Een essentieel onderdeel van deze beschermende laag is het slijm dat wordt geproduceerd door kleine fabrieken, gobletcellen genoemd, die het oogwit en de binnenkant van de oogleden bekleden. Wanneer deze cellen beschadigd raken of verloren gaan, zoals bij droge-oogziekte of ernstige ontstekingsaandoeningen, wordt het oogoppervlak kwetsbaar. Deze studie onderzoekt een opkomende ‘celvrije’ therapie die microscopische pakketjes gebruikt, afkomstig van gedoneerd placentaweefsel, om gobletcellen te helpen overleven en meer van het slijm te produceren dat onze ogen vochtig en beschermd houdt.
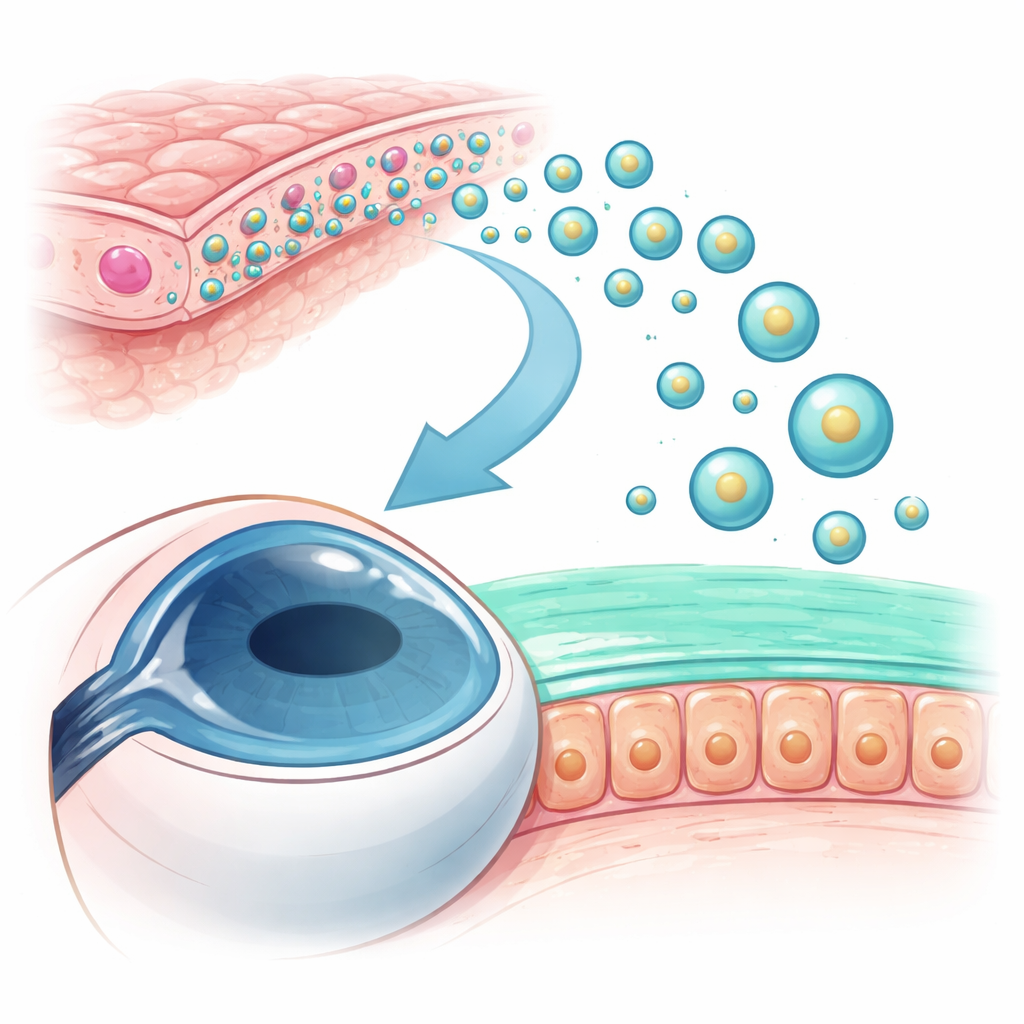
Kleine afleverpakketjes uit zwangerschapsweefsel
De onderzoekers richtten zich op humane amnionepitheelcellen, afkomstig van het dunne vlies rond een baby tijdens de zwangerschap, die al bekendstaan om hun wondgenezende en ontstekingsremmende eigenschappen. Deze cellen geven nanoschaal belletjes af, exosomen genoemd, die eiwitten en genetische regulatoren van de ene cel naar de andere vervoeren. Het team isoleerde deze vesicles uit amnioncelculturen, bevestigde hun typische kelkvormige verschijning en maatbereik onder een elektronenmicroscoop, en verifieerde de aanwezigheid van bekende exosoommerkeiwitten. Deze karakterisatiestap toonde aan dat ze een zuivere bereiding van de kleine pakketjes hadden verkregen die ze wilden testen.
Een microscopische boodschap naar cellen op het oogoppervlak
De volgende vraag was of deze exosomen de conjunctivale gobletcellen — de slijmproducerende cellen die zo belangrijk zijn voor ooggemak — konden bereiken en beïnvloeden. De wetenschappers labelden de exosomen met een fluorescent kleurstof en voegden ze toe aan humane gobletcellen gekweekt in schaaltjes. Onder de microscoop zagen ze felle signalen binnenin de cellen, vooral bij hogere exosoomdoses, wat bevestigde dat gobletcellen deze pakketjes gemakkelijk opnemen. In de exosomen vonden ze een specifiek klein RNA-molecuul, miR-25-3p, veilig opgeborgen tegen afbrekende enzymen, en ze lieten zien dat het blokkeren van exosoomproductie in de broncellen de afgifte van dit molecuul sterk verminderde. Gezamenlijk toonden deze testen aan dat miR-25-3p voornamelijk wordt uitgestuurd binnen exosomen en rechtstreeks in gobletcellen kan worden afgeleverd.
Gobletcellen beter laten functioneren en overleven
Zodra ze deze afleverroute hadden vastgesteld, onderzochten de auteurs wat er gebeurt met gobletcellen nadat ze amnion-afgeleide exosomen ontvangen. Cellen die met exosomen werden behandeld, produceerden meer MUC5AC, een belangrijk slijmcomponent dat de glibberige, beschermende laag op het oogoppervlak vormt. Metingen van zowel het eiwit binnenin de cellen als de hoeveelheid die werd uitgescheiden in de omringende vloeistof toonden een duidelijke, dosisafhankelijke toename. Tegelijkertijd vertoonden minder gobletcellen kenmerken van geprogrammeerde celdood, wat betekent dat de behandeling hun overleving bevorderde. Wanneer de onderzoekers miR-25-3p direct versterkten, werden deze gunstige effecten nog sterker, wat wijst op dit kleine RNA als een sleutelbestanddeel in de exosomen.
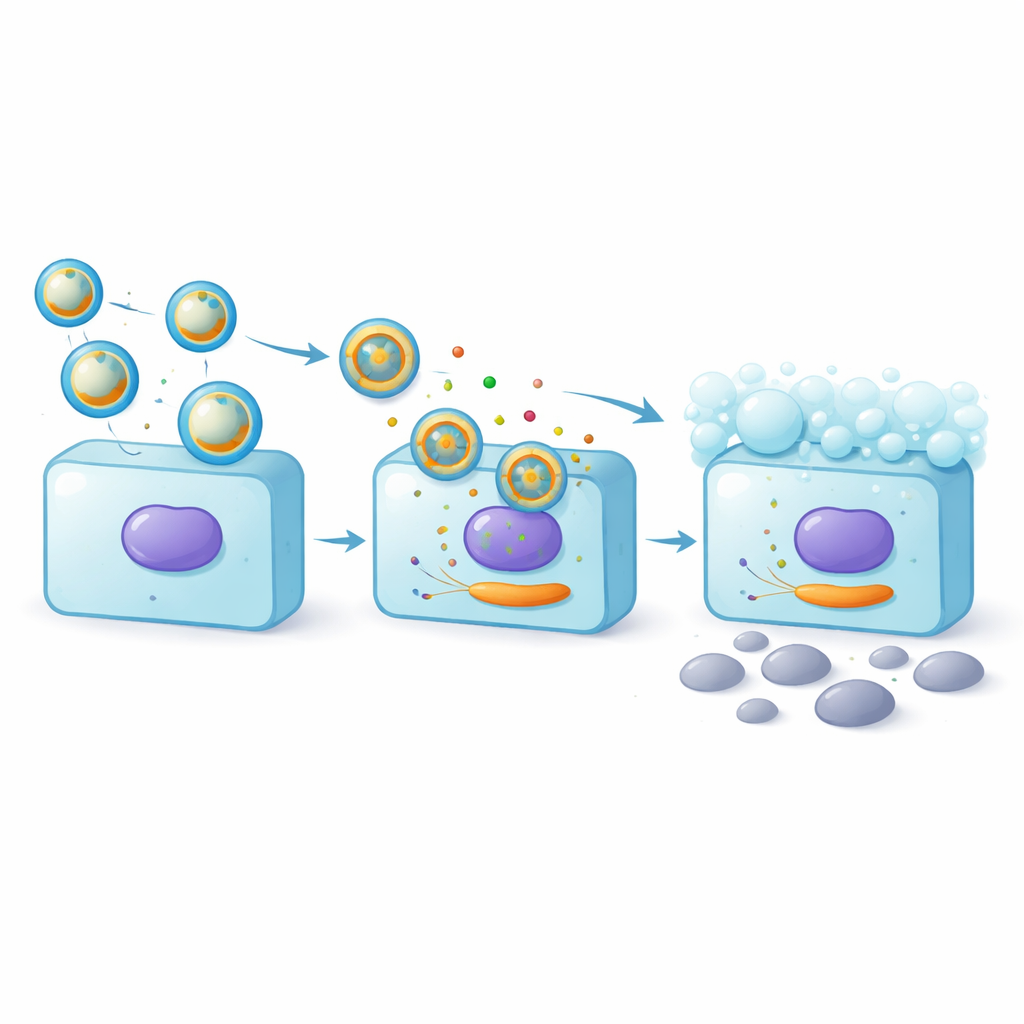
Het uitschakelen van een celdoodtrigger
Om te begrijpen hoe miR-25-3p gobletcellen beschermt, zocht het team naar het moleculaire doelwit en richtte zich op BCL2L11, een gen dat celdood bevordert. Met een reportersysteem bevestigden ze dat miR-25-3p kan binden aan het boodschapper-RNA van BCL2L11 in de cel en de activiteit ervan dempt. Gobletcellen die werden blootgesteld aan amnionexosomen toonden lagere niveaus van BCL2L11, vooral wanneer de exosomen verrijkt waren met miR-25-3p. Toen de onderzoekers kunstmatig BCL2L11 verhoogden, ging een deel van de beschermende effecten van miR-25-3p verloren: celdood nam weer toe en slijmproductie daalde. Dit touwtrekken toonde aan dat een belangrijk deel van het voordeel van de exosomen voortkomt uit miR-25-3p dat BCL2L11 onderdrukt en zo zowel het overleven van gobletcellen als de slijmproductie ondersteunt.
Wat dit zou kunnen betekenen voor mensen met droge ogen
Simpel gezegd laat deze studie zien dat microscopische pakketjes, afkomstig van gedoneerd geboorteweefsel, een beschermende genetische boodschap kunnen afleveren aan de slijmproducerende cellen van het oog. Die boodschap, gedragen door miR-25-3p, helpt een ingebouwde zelfvernietigingsschakel uit te schakelen en moedigt gobletcellen aan meer van het slijm te produceren dat het oogoppervlak glad en beschermd houdt. Hoewel deze experimenten in laboratoriumschalen zijn uitgevoerd en meer werk in diermodellen en bij patiënten nodig is, schetsen de bevindingen een veelbelovende celvrije strategie: het gebruik van gezuiverde exosomen in plaats van volledige cellen om een gezonde traanfilm te herstellen en mogelijk aandoeningen te verlichten waarbij het oogoppervlak droog, ontstoken en kwetsbaar raakt.
Bronvermelding: Zhang, Y., Wu, W., Meng, T. et al. Human amnion epithelial cell-derived exosomal miR-25-3p enhances mucin expression in conjunctival goblet cells via downregulating BCL2L11. Sci Rep 16, 7958 (2026). https://doi.org/10.1038/s41598-026-37794-3
Trefwoorden: droge-oogziekte, traanfilmmucus, exosomen, therapie voor het oculair oppervlak, gobletcellen