Clear Sky Science · nl
Voorlopige beoordeling van biodistributie en targeting van de fluorescerende moleculaire probe Cy7-SYL3C in een EpCAM-positief muismodel voor colorectale kanker
Waarom dit belangrijk is voor kankerdetectie
Colorectale kanker is een van de grootste veroorzakers van sterfte door kanker wereldwijd, deels omdat veel tumoren laat worden ontdekt. De huidige belangrijkste screeningsmethode, colonoscopie, is effectief maar ingrijpend en onaangenaam, waardoor veel mensen het vermijden. Deze studie onderzoekt een nieuw soort oplichtende “slimme tracer” die artsen in de toekomst zou kunnen helpen darmptumoren eerder en duidelijker te zien, met licht in plaats van een scalpel of een lange buis.
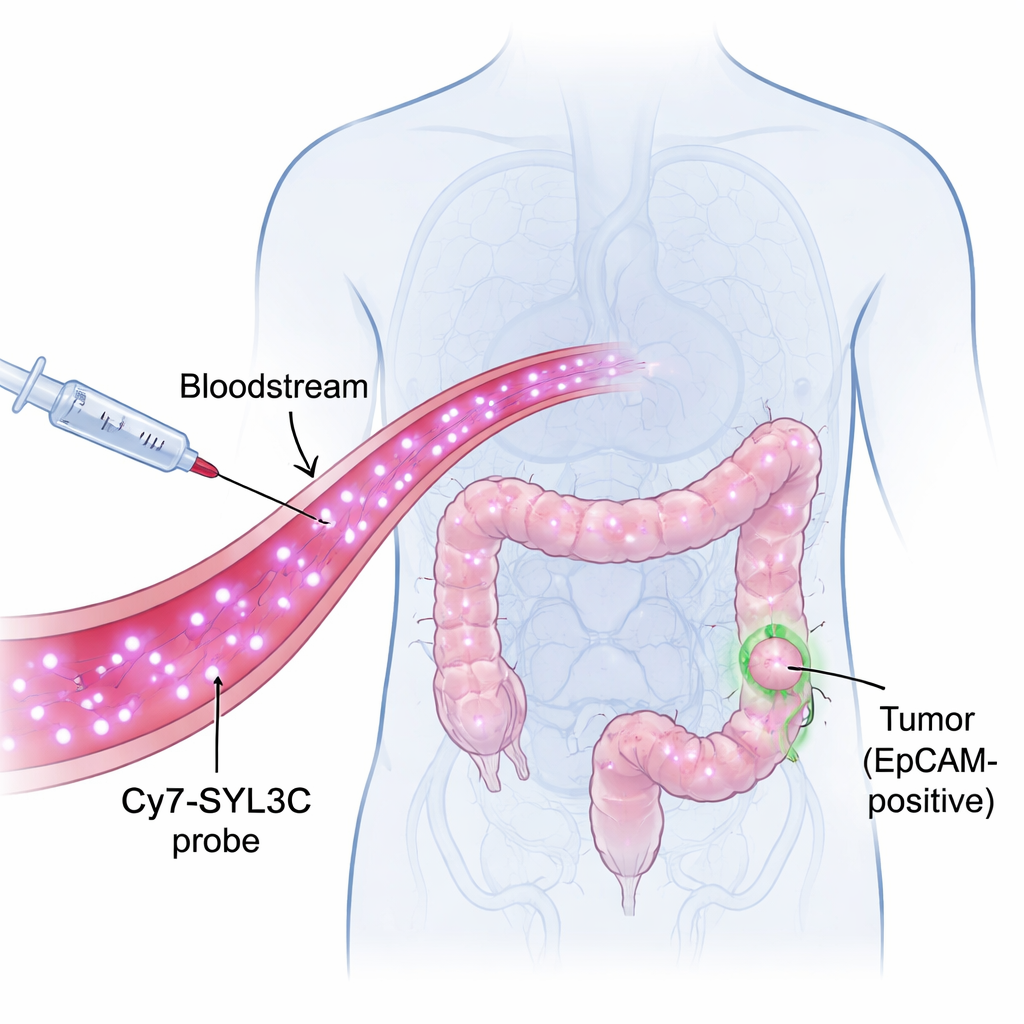
Een oplichtend label dat tumorcellen herkent
De onderzoekers richtten zich op een molecuul genaamd EpCAM, dat op het oppervlak van veel colorectale kankercellen voorkomt maar schaars is in gezond weefsel. Ze bouwden een probe genaamd Cy7-SYL3C door een nabij-infrarode kleurstof (Cy7) te koppelen aan een korte streng DNA, een aptameer (SYL3C), die EpCAM kan herkennen zoals een sleutel in een slot past. Nabij-infrarood licht is onzichtbaar voor het oog maar kan enkele millimeters in weefsel doordringen, waardoor camera’s signalen van binnen het lichaam met hoge contrastwaarden kunnen vastleggen. Het idee is simpel: injecteer Cy7-SYL3C in de bloedbaan, laat het EpCAM-rijke tumorcellen opzoeken en gebruik vervolgens een speciale camera om die cellen te laten oplichten tegen een donkerder achtergrond.
Veiligheid en stabiliteit testen in het laboratorium
Voordat ze de probe in levende dieren probeerden, controleerde het team of deze stabiel en veilig was. Ze mengden Cy7-SYL3C met bloedserum van muizen en runderen en vonden dat het grootste deel van de probe minstens acht uur intact bleef, lang genoeg voor beeldvorming tijdens een medische ingreep. Vervolgens brachten ze menselijke colorectale kankercellen en normale darmcellen bloot aan verschillende concentraties van de probe. Celgroei bleef in wezen ongewijzigd, en toen de probe met rode bloedcellen werd gemengd, veroorzaakte deze geen hemolyse. Deze tests suggereren dat Cy7-SYL3C zowel chemisch stabiel als vriendelijk voor cellen is — belangrijke vereisten voor elke beeldvormende stof die bij patiënten gebruikt zou kunnen worden.
Waar de probe zich in het lichaam bevindt
De wetenschappers volgden vervolgens het pad van Cy7-SYL3C in gezonde muizen met behulp van een klein-dier imaging-systeem. Kort na injectie verscheen het sterkste signaal in de lever en nieren, organen die stoffen uit het bloed filteren en verwijderen. Het leversignaal piekte rond één uur en vervaagde daarna, terwijl de nieren langer oplichtten, wat wijst op urine als belangrijkste uitscheidingsroute voor de probe. Na twee dagen bleef slechts een klein deel van het oorspronkelijke signaal over, en microscopisch onderzoek van belangrijke organen toonde geen duidelijke weefselschade. Dit betekent dat de probe redelijk snel wordt uitgescheiden en in deze kortdurende studie geen zichtbare schade aan vitale organen veroorzaakt.
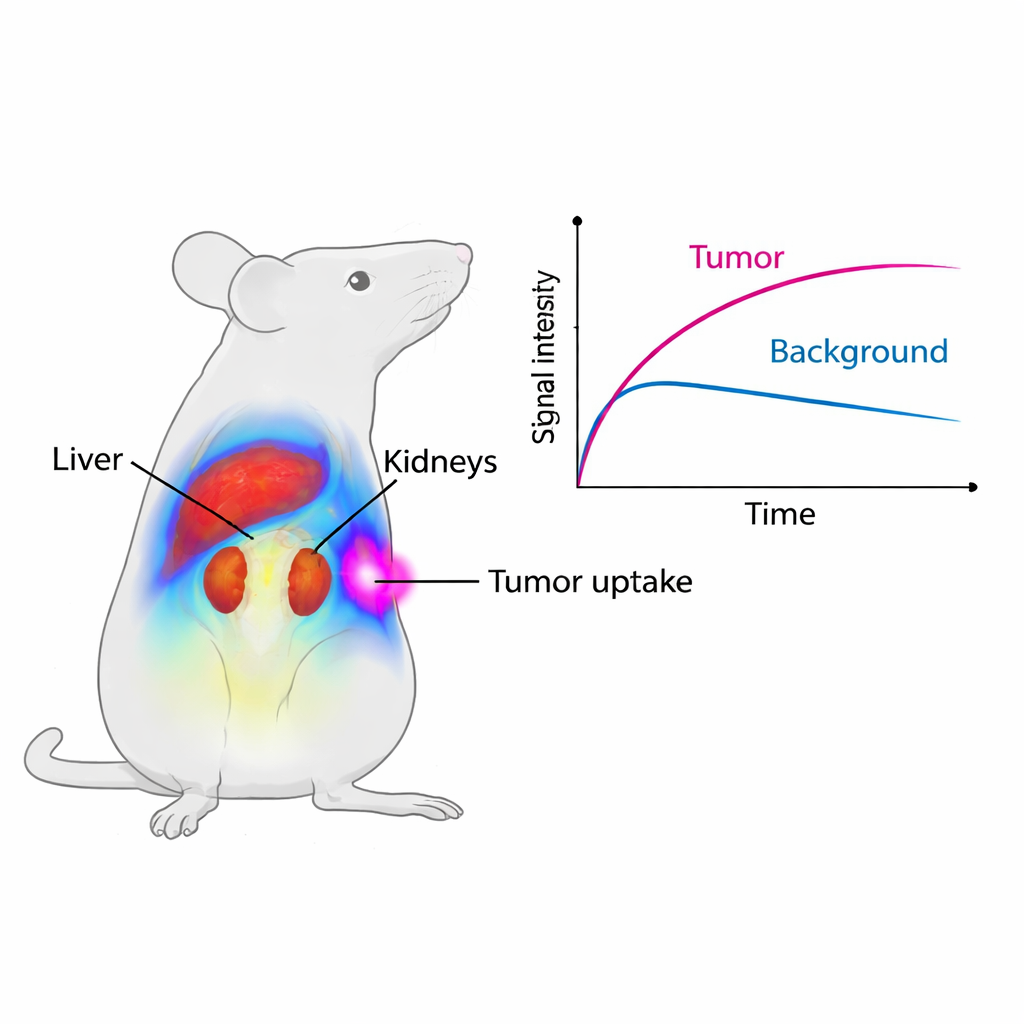
Inzoomen op colorectale tumoren
Om te onderzoeken of Cy7-SYL3C daadwerkelijk naar kanker toe gaat, gebruikte het team muizen met geïmplanteerde humane colorectale tumoren die EpCAM produceren. Binnen slechts vijf minuten na injectie begonnen de tumoren te gloeien op het beeldvormingssysteem. Gedurende de eerste vier uur was het gemiddelde signaal in tumoren bijna twee keer zo sterk als bij muizen waarbij de tumoren vooraf waren “geblokkeerd” met een overschot aan niet-gedifferentieerde SYL3C, die tijdelijk EpCAM-sites bezette en verhinderde dat de gelabelde probe zich hechtte. De verhouding van tumorsignaal tot nabijgelegen spier werd groter dan één en piekte rond acht uur, wat betekent dat tumoren duidelijk helderder waren dan hun omgeving gedurende een bruikbare beeldvormingsperiode. Gedetailleerde microscopische studies bevestigden dat de fluorescerende probe samenviel met EpCAM-kleuring op tumorcellen, terwijl normale organen weinig of geen EpCAM toonden.
Hoe dit toekomstige chirurgie en diagnose zou kunnen begeleiden
Voor niet‑specialisten is de belangrijkste boodschap dat Cy7-SYL3C zich gedraagt als een slimme kleurstof die colorectale kankercellen opzoekt en vervolgens grotendeels via de nieren wordt uitgescheiden. Het lijkt stabiel, celvriendelijk en in staat tumoren snel en gedurende enkele uren te laten oplichten, wat chirurgen kan helpen tumorranden in real time duidelijker te zien of radiologen verdachte gebieden tijdens minimaal invasieve procedures op te sporen. Hoewel deze resultaten uit vroege muisexperimenten komen en er meer werk nodig is voordat toepassing bij mensen mogelijk is, legt de studie belangrijke basis voor een nieuwe klasse van lichtgebaseerde tracers die detectie en chirurgie van colorectale kanker preciezer en minder ingrijpend zouden kunnen maken.
Bronvermelding: Li, Y., Li, M., Li, P. et al. Preliminary assessment of biodistribution and targeting of the fluorescent molecular probe Cy7-SYL3C in an EpCAM-positive colorectal cancer mouse model. Sci Rep 16, 6589 (2026). https://doi.org/10.1038/s41598-026-37787-2
Trefwoorden: beeldvorming van colorectale kanker, nabij-infrarode fluorescentie, EpCAM-targeting, aptameerprobe, geleiding bij tumorchirurgie