Clear Sky Science · nl
Kankerclassificatie met radiomics in gecontroleerde preklinische modellen
Kanker aflezen uit scans en bloed
Moderne kankerzorg vertrouwt steeds meer op computers die medische beelden en laboratoriumtests doorzoeken op patronen die mensen niet gemakkelijk zien. Deze studie stelt een eenvoudige maar belangrijke vraag: als we willen bepalen welk type kanker een patiënt heeft, is het dan beter om verborgen informatie uit hun scans te lezen of uit hun bloed? Met zorgvuldig gecontroleerde experimenten bij muizen vergeleken de onderzoekers deze twee benaderingen direct om te zien welke betrouwbaardere antwoorden geeft.
Wat het betekent om een “virtuele biopsie” te nemen
Radiomics is een snelgroeiende techniek die elke medische scan behandelt als een rijke gegevensbron in plaats van slechts een afbeelding. Speciale software doorzoekt driedimensionale CT‑beelden van een tumor en zet ze om in honderden numerieke kenmerken die de vorm, helderheid en fijnmazige textuur beschrijven. In principe kunnen deze patronen de biologie van de tumor weerspiegelen op een manier die lijkt op een biopsie, maar zonder naalden of operatie — een zogenaamde “virtuele biopsie.” Voorstanders hopen dat radiomics kan helpen bij het classificeren van kankers, het inschatten van agressiviteit en het sturen van behandelingskeuzes. Maar er zijn zorgen: resultaten zijn soms moeilijk te reproduceren, vatbaar voor technische vertekeningen en lastig voor artsen om te interpreteren.
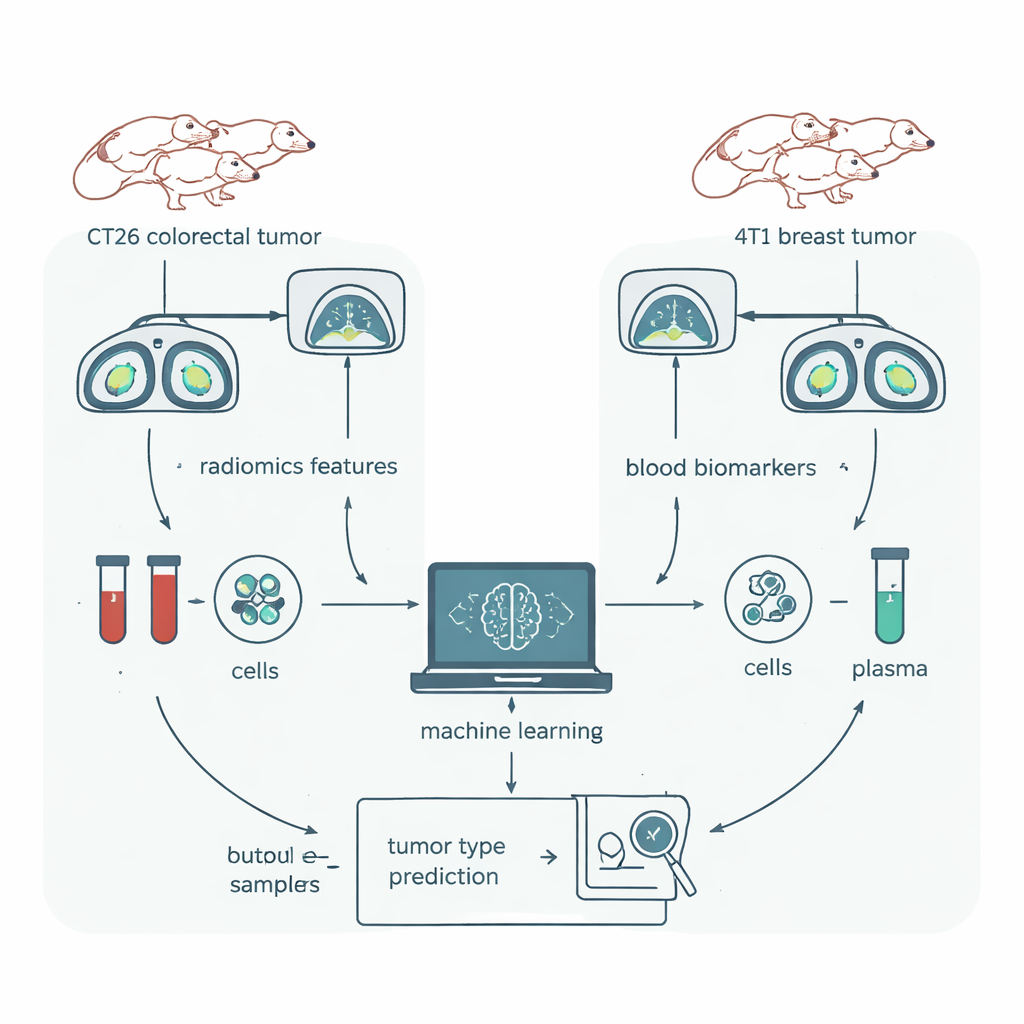
Een eerlijke onderlinge vergelijking in muizen
Om radiomics rigoureus te testen richtte het team zich op een muismodel waarbij bijna alles gecontroleerd kon worden. Groepen genetisch identieke muizen kregen ingrijvingen met een van twee tumortypes: CT26, een model voor colorectale kanker, en 4T1, een model voor borstkanker. Alle dieren waren van hetzelfde ras, geslacht en vergelijkbare leeftijd, gehouden in dezelfde omgeving en gescand op dezelfde CT‑scanner. Tumoren werden zorgvuldig driedimensionaal omlijnd in software, en een populair radiomics‑pakket extraheerde 1.409 numerieke kenmerken uit elke scan. Tegelijkertijd trokken de onderzoekers bloed van dezelfde dieren en maten ze immuunceltypen en tientallen eiwitten — biomarkers die in hun eerdere werk al hadden aangetoond dat ze deze kankermodellen vrijwel perfect konden onderscheiden.
Duizenden beelddetails comprimeren tot een bruikbaar signaal
De meeste ruwe beeldkenmerken bleken weinig behulpzaam: sommige varieerden nauwelijks tussen muizen en veel waren bijna duplicaten van elkaar. Na meerdere rondes van statistische filteringen bleven slechts 18 niet‑redundante radiomische kenmerken over, die vooral subtiele textuurpatronen beschreven in plaats van eenvoudige grootte of vorm. Het team gebruikte vervolgens een standaard machine‑learningmethode, Random Forest, om te zien hoe goed deze verfijnde beeldkenmerken de twee tumortypes van elkaar konden onderscheiden. Ze pasten ook visualisatietools toe om te onderzoeken of de gegevens zonder voorafgaande labels vanzelf afzonderlijke clusters voor elk kankertype vormden.
Bloedsignalen verslaan beeldsignalen
Het contrast tussen bloed en beeldvorming was opvallend. Toen de onderzoekers de bloedcel‑ en plasma‑proteïnegegevens tot twee dimensies reduceerden, vormden de twee tumortypes duidelijk gescheiden clusters, wat bevestigde dat het bloed sterke, tumorspecifieke signalen vastlegde. In de radiomicsgegevens verschenen daarentegen drie gemengde clusters, elk met een mengeling van beide kankers, wat suggereert dat andere, onbekende factoren de beelden beïnvloedden. In gesuperviseerde tests classificeerde radiomics alleen het tumortype met een nauwkeurigheid van ongeveer 87 procent — goed, maar merkbaar slechter dan de 96 procent nauwkeurigheid van immuunceltaantallen en de 99 procent nauwkeurigheid van plasma‑eiwitten. Het toevoegen van radiomics aan de bloedmarkers verbeterde de prestatie niet; in sommige combinaties verminderde het de nauwkeurigheid licht. Een verdere proef toonde aan dat het gebruik van slechts een kleine bolvormige regio binnenin de tumor, in plaats van de hele massa te omlijnen, de radiomicsprestaties nog verder verslechterde, wat benadrukt hoe gevoelig deze kenmerken zijn voor hoe de tumor in de scan wordt getekend.
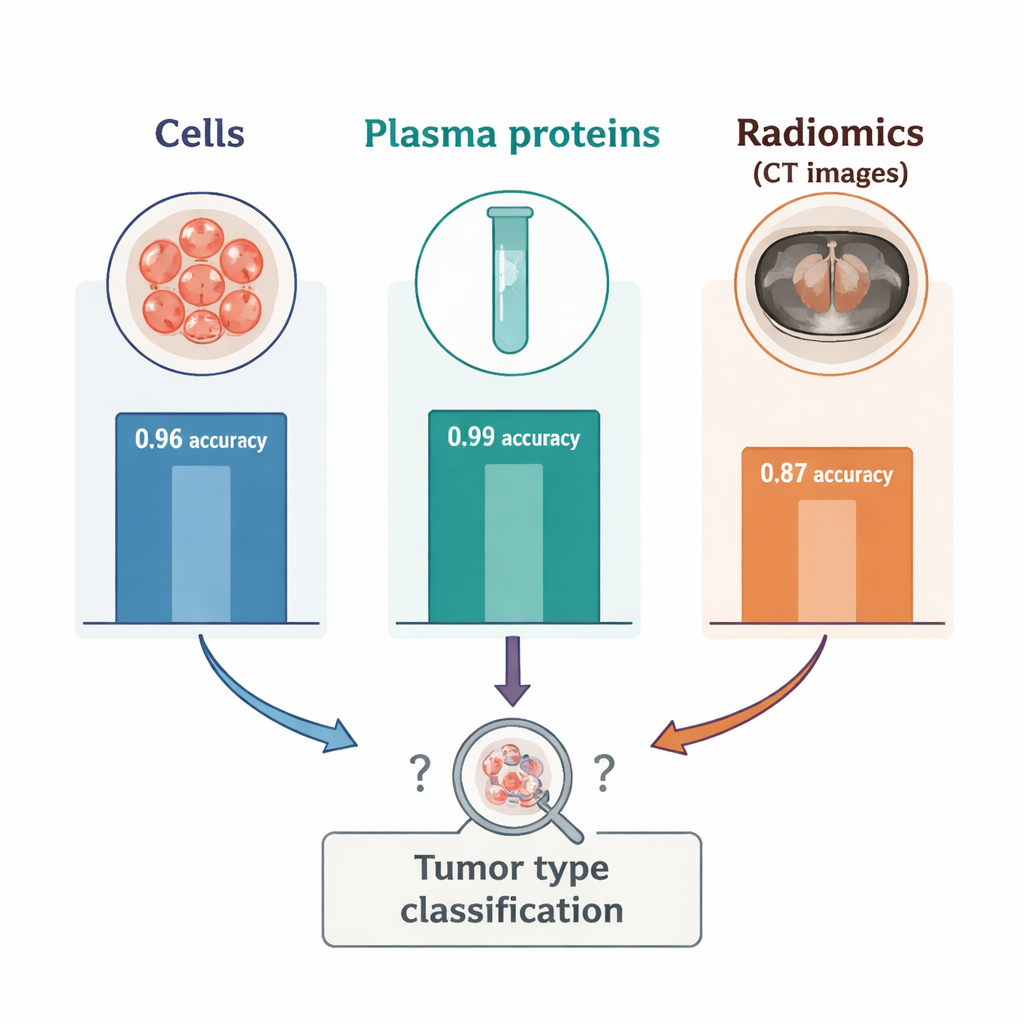
Wat dit betekent voor toekomstige kankertests
De conclusie voor een algemeen publiek is duidelijk: hoewel geavanceerde beeldanalyse enkele nuttige aanwijzingen kan geven, werd het in deze studie overtroffen door relatief eenvoudige bloedtesten als het ging om het onderscheiden van twee kankertypes. Zelfs in een streng gecontroleerde laboratoriumomgeving met identieke muizen en gestandaardiseerde beeldvorming leken kleine technische verschillen en de complexiteit van beeldverwerking het radiomische signaal te vervagen. De auteurs concluderen dat radiomics nog niet klaar is om als zelfstandige, hoogst betrouwbare kankerclassifier te fungeren. In plaats daarvan pleiten zij voor sterkere standaardisatie van beeldvorming, betere contoureringstools en duidelijkere verbanden tussen beeldpatronen en onderliggende biologie voordat virtuele biopsies betrouwbaar klinische beslissingen kunnen begeleiden naast, of in plaats van, goed gevestigde bloedbiomarkers.
Bronvermelding: Drover, K., Davis, D.A.S., Gosling, K. et al. Cancer classification with radiomics in controlled preclinical models. Sci Rep 16, 6647 (2026). https://doi.org/10.1038/s41598-026-37757-8
Trefwoorden: radiomics, kankerbiomarkers, medische beeldvorming, machine learning in oncologie, bloedtesten voor kanker