Clear Sky Science · nl
Synergetische gerichtheid op de ARID2–MYC‑as door pomalidomide en panobinostat overwint intrinsieke IMiD‑resistentie bij multipel myeloom
Waarom dit onderzoek belangrijk is voor patiënten
Multipel myeloom is een kanker van antistofproducerende cellen in het beenmerg die beter behandelbaar is geworden maar zelden geneest. Veel patiënten verliezen na verloop van tijd de respons op standaardmedicatie, waardoor artsen minder opties overhouden. Deze studie onderzoekt waarom de combinatie van twee bestaande medicijnklassen — zogenaamde IMiD’s zoals pomalidomide en geneesmiddelen die de DNA‑opvouwing beïnvloeden, de histon‑deacetylaseremmers (HDAC‑remmers) zoals panobinostat — gezamenlijk myeloomcellen kan doden, zelfs wanneer de kanker al resistent is tegen IMiD’s alleen. Inzicht in deze samenwerking op moleculair niveau kan leiden tot betere combinatietherapieën en meer patiënten laten profiteren van geneesmiddelen die we al hebben.
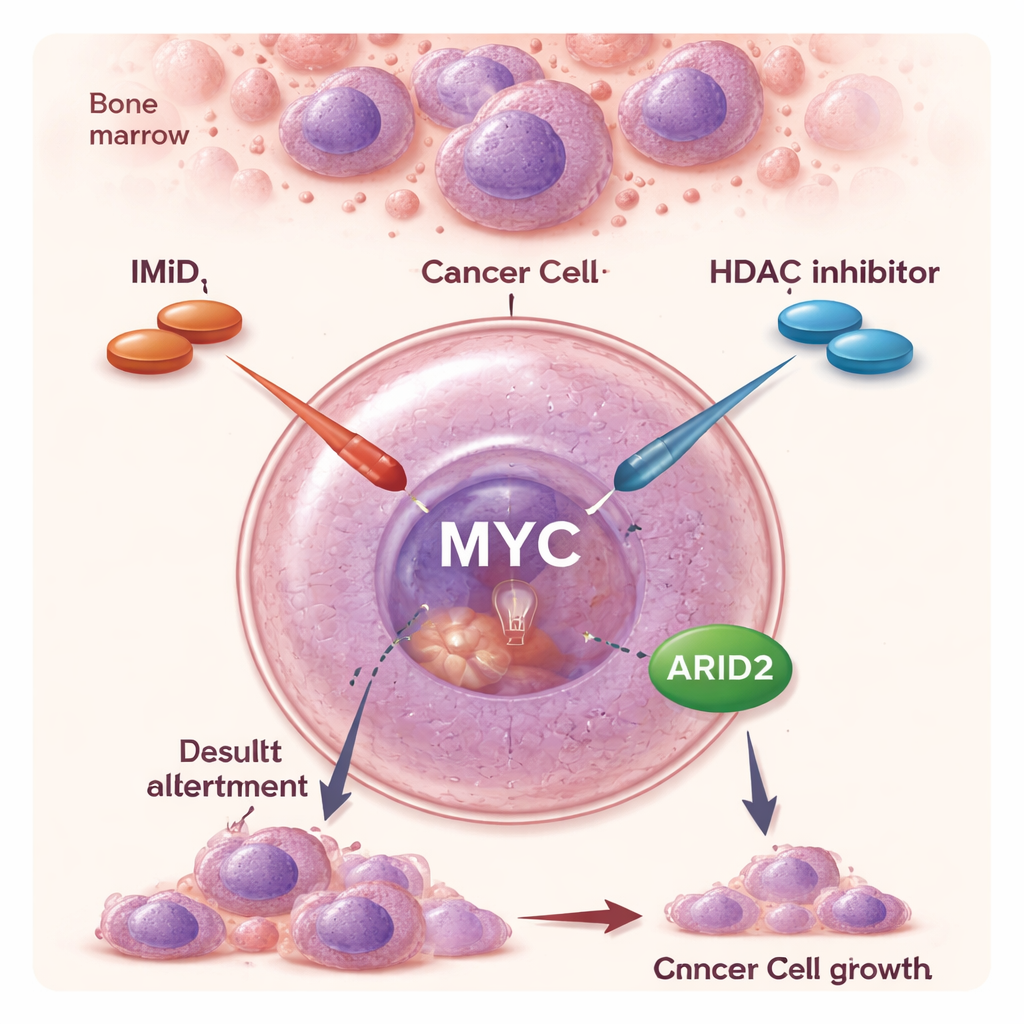
Twee oudere medicijnklassen, één nieuwe samenwerking
In de afgelopen twee decennia hebben IMiD’s en andere gerichte middelen de overleving bij multipel myeloom sterk verlengd. IMiD’s werken op een ongebruikelijke manier: in plaats van een eiwit eenvoudigweg te blokkeren, veroorzaken ze dat bepaalde eiwitten worden gelabeld voor afbraak, waardoor die uit de cel verdwijnen. Daardoor verzwakken ze cruciale overlevingssignalen waarop myeloomcellen vertrouwen. HDAC‑remmers zoals panobinostat werken anders: ze versoepelen de strakke verpakking van DNA en veranderen daardoor in brede zin welke genen aan of uit staan. Als afzonderlijke middelen hebben HDAC‑remmers bescheiden effecten en kunnen bijwerkingen veroorzaken, maar klinische studies wezen erop dat combinatie met IMiD’s een veel sterkere antikankerreactie kan geven, ook bij patiënten wiens ziekte niet meer reageert op IMiD’s alleen. De moleculaire reden voor deze synergie was echter onduidelijk gebleven.
Een gemeenschappelijke drukpunt: MYC omlaag brengen
De onderzoekers testten systematisch combinaties van verschillende IMiD’s met diverse HDAC‑remmers in een reeks myeloomcellijnen, waarbij ze een gestandaardiseerde score gebruikten om te meten hoe veel krachtiger de combinaties waren dan elk middel afzonderlijk. Ze ontdekten dat pomalidomide plus panobinostat bijzonder sterke synergie liet zien in de meeste celmodellen, en dat dit effect afhankelijk was van een eiwit genaamd cereblon, dat IMiD’s gebruiken om hun eiwit“slachtoffers” voor afbraak te markeren. Door de globale genactiviteit te analyseren, vonden ze dat panobinostat en een verwante breedwerkende HDAC‑remmer MYC sterk uitschakelden — MYC is een hoofdgen dat de groei aanstuurt en vaak als een “oncogene motor” in kankercellen wordt beschreven — en dat IMiD’s extra druk uitoefenden op datzelfde knooppunt. Wanneer de wetenschappers myeloomcellen dwongen MYC te blijven produceren vanuit een middelongevoelige bron, verdween het krachtige effect van het draakpaar grotendeels, wat aantoont dat het uitschakelen van MYC centraal staat in hun samenwerking.
Resistentie kraken via een alternatieve route
Sommige myeloomcellen zijn intrinsiek resistent tegen IMiD’s: hoewel de verwachte vroege doelen worden vernietigd, worden MYC en andere overlevingssignalen niet adequaat stilgelegd, zodat de cellen blijven groeien. In één dergelijk resistent model was de standaard IMiD‑route die vroege doelen met MYC verbindt “ontkoppeld”. Het team vroeg zich af of een alternatieve route IMiD’s nog steeds met MYC kon verbinden. Ze concentreerden zich op ARID2, een onderdeel van een groot DNA‑herbouwend complex genaamd SWI/SNF. Eerder werk had aangetoond dat pomalidomide ARID2 kan markeren voor afbraak en dat dit helpt MYC te verlagen. In resistentcellen verminderde pomalidomide ARID2 slechts in geringe mate, deels omdat de cel als reactie de ARID2‑productie verhoogde. Toen panobinostat werd toegevoegd, onderdrukte het het ARID2‑gen zelf en doorbrak zo deze terugkoppelingslus. Samen verminderden de twee geneesmiddelen ARID2‑eiwit en vervolgens MYC sterk, wat leidde tot krachtige celdoding zelfs in IMiD‑resistente lijnen.
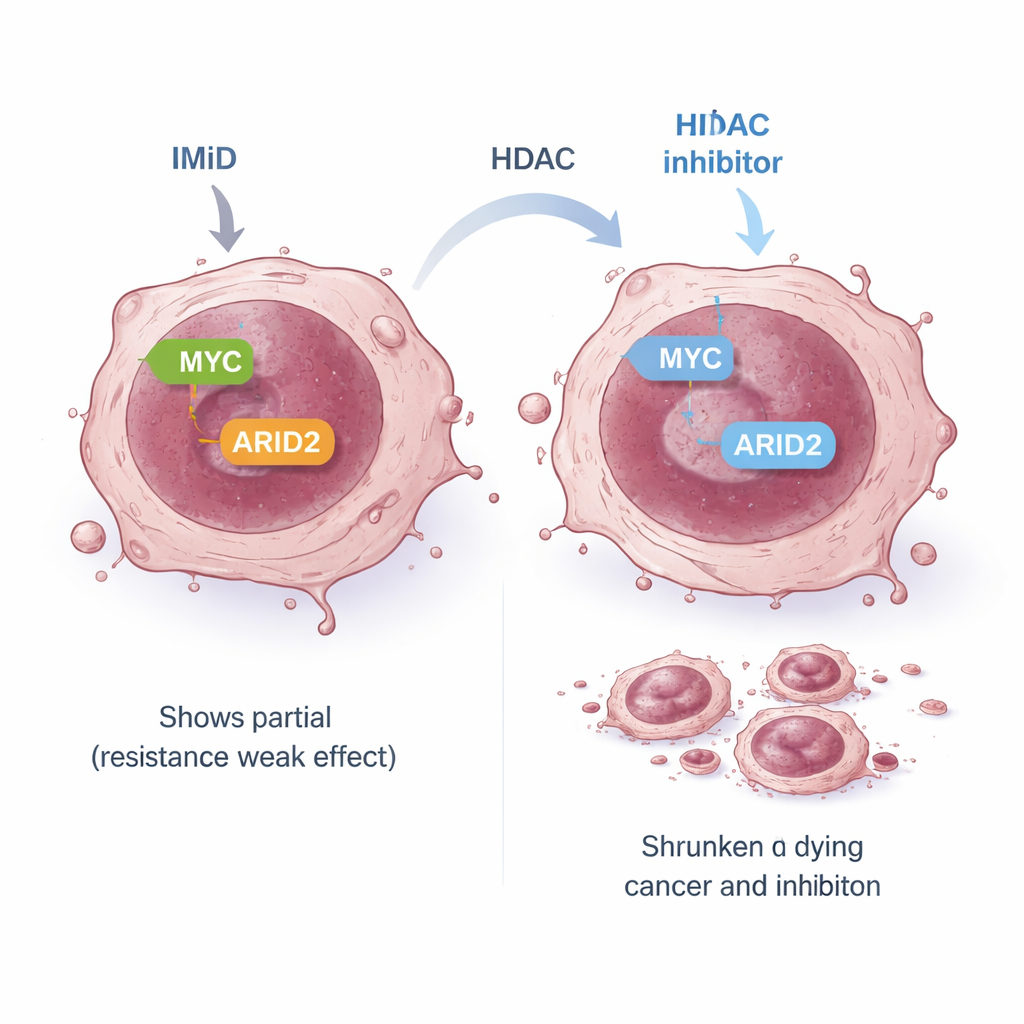
Een bredere zwakke plek in kankercellen blootleggen
Aangezien ARID2 slechts één lid is van het SWI/SNF‑complex, vroegen de auteurs zich af of het hele complex een therapeutisch zwak punt zou kunnen vormen. Ze vonden dat HDAC‑remmers de niveaus van meerdere SWI/SNF‑componenten verlagen, en dat een apart kleinmoleculair middel dat is ontworpen om de kernmotoren van het complex (BRG1/BRM) te blokkeren, op zichzelf de groei van myeloomcellen kan vertragen en MYC kan verlagen. Belangrijk is dat deze SWI/SNF‑remmer ook synergetisch werkte met zowel pomalidomide als panobinostat, en dat een driedubbele combinatie ARID2 en MYC nog verder naar beneden bracht terwijl celproliferatie sterk werd onderdrukt. Door te onderzoeken welke specifieke HDAC‑enzymen betrokken waren, wezen de onderzoekers HDAC1 aan als een sleutelspeler die de ARID2–MYC‑route helpt ondersteunen, terwijl andere HDAC’s MYC via parallelle wegen lijken te beïnvloeden.
Wat dit betekent voor toekomstige myeloombehandeling
Voor niet‑specialisten is de kernboodschap dat myeloomcellen lijken te vertrouwen op een gedeeld "groeiregelcentrum" rond MYC, en dat er meer dan één weg naar dat centrum leidt. Standaard IMiD‑therapie treft vooral één weg; in sommige resistente kankers is die weg geblokkeerd, waardoor MYC actief blijft. Deze studie toont aan dat een alternatieve weg — lopend via ARID2 en het SWI/SNF‑complex — nog openstaat, en dat het gebruik van panobinostat naast pomalidomide die weg kan afsluiten. Door geneesmiddelen doelbewust te combineren die op MYC vanuit meerdere richtingen drukken, kunnen clinici mogelijk sommige vormen van ingebouwde geneesmiddelresistentie overwinnen terwijl ze mogelijk lagere doses van elk middel gebruiken. Hoewel verder preklinisch en klinisch onderzoek nodig is, bieden de bevindingen een helderder stappenplan voor het ontwerpen van slimmere, mechanismegebaseerde combinaties voor patiënten met moeilijk behandelbaar multipel myeloom.
Bronvermelding: Yamamoto, J., Asatsuma-Okumura, T., Ito, T. et al. Synergistic targeting of the ARID2–MYC axis by pomalidomide and panobinostat overcomes intrinsic IMiD resistance in multiple myeloma. Sci Rep 16, 7375 (2026). https://doi.org/10.1038/s41598-026-37740-3
Trefwoorden: multipel myeloom, geneesmiddelresistentie, pomalidomide, panobinostat, MYC