Clear Sky Science · nl
Classificatie van gliomen op basis van lipidenmetabolisme
Waarom vetten in hersentumoren ertoe doen
Hersentumoren die gliomen worden genoemd behoren tot de gevaarlijkste vormen van kanker, maar patiënten met ogenschijnlijk dezelfde diagnose kunnen sterk uiteenlopende uitkomsten hebben. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote implicaties: op welke manier bepalen de manieren waarop tumoren vetten — de lipiden van het lichaam — gebruiken hoe agressief ze zijn, hoe ze op behandeling reageren en of we die verschillen kunnen zien op standaard hersenscans? Door het lipidengebruik in honderden tumoren te volgen, onthullen de auteurs verborgen subtypen van glioom die kunnen veranderen hoe artsen prognoses inschatten en therapieën ontwerpen.
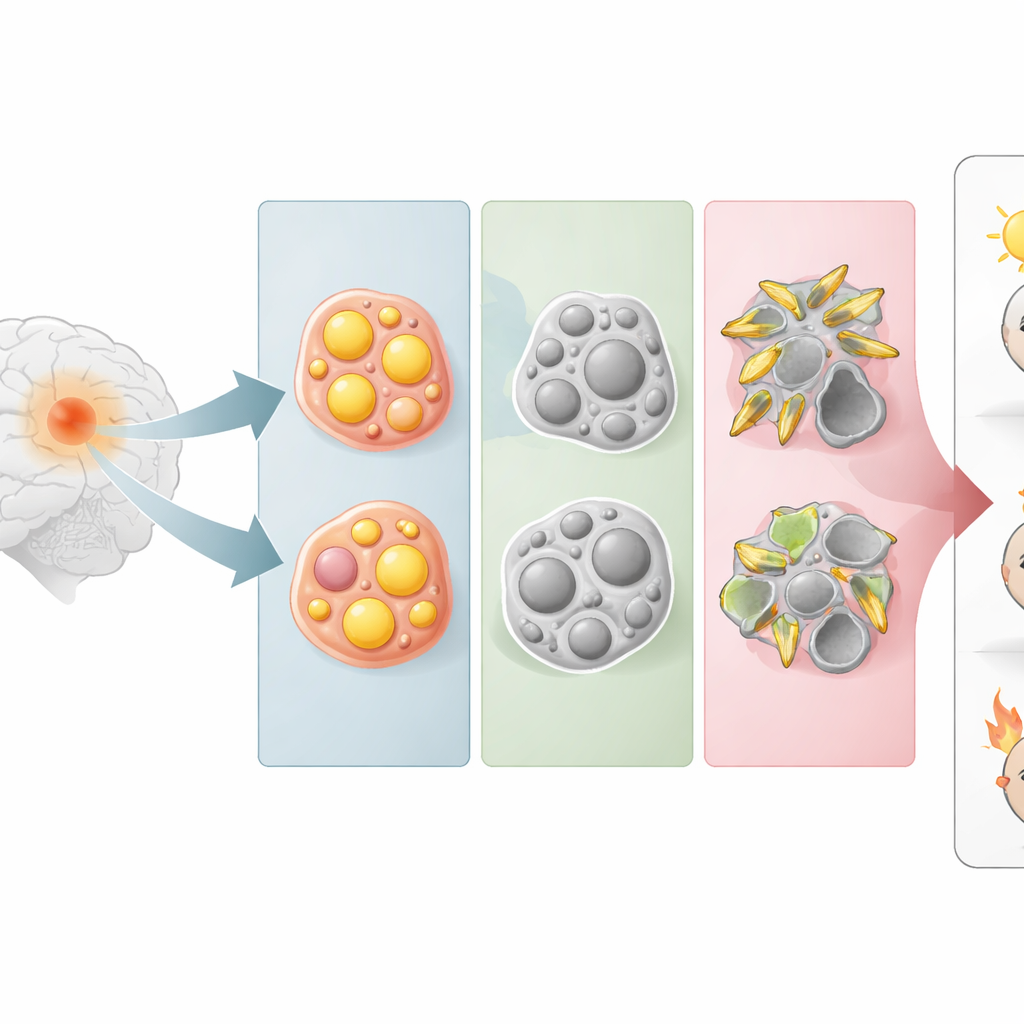
Drie verborgen gezichten van dezelfde hersentumor
In plaats van te beginnen met hoe tumorcellen eruitzien onder de microscoop, groepeerden de onderzoekers gliomen op basis van hoe sterk ze vijf belangrijke lipideroutes activeren, waaronder die voor steroïdevetten, triglyceriden en sfingolipiden (belangrijke bouwstenen van celmembranen). Met genactiviteitsprofielen uit grote openbare tumordatabases ontdekten ze dat gliomen van nature in drie groepen vielen. De ene groep leunde zwaar op steroïde-metabolisme (ST-type), een andere op triglyceride-metabolisme (TC-type) en een derde op sfingolipide-metabolisme (SP-type). Deze metabolische indelingen snijden dwars door klassieke tumorcategorieën heen en laten zien dat cellen met vergelijkbare lipidegewoonten voorkomen in anderszins verschillend ogende gliomen.
Van metabolisme naar patiëntenvooruitzicht
Het team vroeg vervolgens hoe deze drie vetgebruikstijlen zich verhouden tot uitkomsten in de praktijk. Patiënten met tumoren in de ST-type groep hadden over het algemeen de langste overleving, en hun tumoren waren vaker laaggradig en droegen bekende gunstige genetische veranderingen. Aan het andere uiterste bleken SP-type tumoren meestal hooggradige glioblastomen zonder beschermende mutaties en kwamen ze vaker voor bij oudere patiënten. Zelfs na statistische correctie voor tumorgraad en belangrijke genetische markers voorspelde behorend tot het SP-type nog steeds een veel slechter vooruitzicht, wat suggereert dat hoe de tumor sfingolipiden verwerkt een onafhankelijke risicodimensie vastlegt die standaardtests missen.
Een vijandige buurt binnenin de hersenen
Dieper gravend onderzochten de auteurs de tumormicro-omgeving — de mix van immuuncellen, bloedvaten en ondersteunend weefsel rond de kanker. SP-type tumoren vertoonden een druk en verdeeld immuunlandschap, met zowel aanvallende als onderdrukkende immuuncellen aanwezig, plus sterke signalen die effectieve anti-tumorreacties dempen. Paden die samenhangen met snelle celgroei, invasie, vorming van nieuwe bloedvaten, littekenvorming en ontsteking waren in dit subtype allemaal actiever. Maten die inschatten hoe tumoren op bestraling reageren suggereerden dat SP-type gliomen het meest resistent zijn tegen radiotherapie, wat overeenkomt met hun slechtere overleving. Ter vergelijking oogden ST-type tumoren meer ‘kalm’, met lagere niveaus van deze agressieve kenmerken.
Het uitlezen van tumormetabolisme uit MRI-scans
Aangezien het operatief verwijderen van tumorweefsel ingrijpend is en niet altijd mogelijk, onderzochten de onderzoekers of standaard magnetische resonantiebeeldvorming (MRI) een aanwijzing kan geven voor het lipidegedrag van een tumor. Ze haalden meer dan tweeduizend subtiele textuur- en vormkenmerken uit twee veelgebruikte MRI-sequenties en trainden een machine-learningmodel om SP-type te onderscheiden van alle andere tumoren. Het model presteerde goed in zowel een ziekenhuisgebaseerde trainingsset als een onafhankelijke openbare validatieset en scheidde SP-type tumoren veel vaker correct dan op toeval gebaseerd zou zijn. Dit suggereert dat het metabole vingerafdruk van een bijzonder agressief glioomsubtype een detecteerbare afdruk achterlaat op routinematige hersenscans.
Een sleutelgen in het centrum van een agressief netwerk
Om van brede paden naar concrete targets te komen, zocht het team naar genen die centraal stonden in lipidegerelateerde netwerken, sterk overactief waren in SP-type tumoren, gekoppeld waren aan slechtere overleving en nauwkeurig SP-type tumoren konden onderscheiden van anderen. Drie genen — GLA, GLB1 en HSD3B7 — voldeden aan alle criteria. Alle drie waren actiever in SP-type gliomen en vormden samen een krachtig diagnostisch handtekening. De auteurs richtten zich op HSD3B7, waarvan de rol in hersentumoren grotendeels ongerepresenteerd was. Weefselkleuring van 100 glioompatiënten toonde aan dat het HSD3B7-eiwit hoger was in meer gevorderde en maligne tumoren, en patiënten met tumoren die hoge niveaus van dit eiwit hadden, leefden significant korter.
Hoe één lipidegen het tumorecosysteem hervormt
Single-cell analyses, die individuele cellen binnen tumoren profileren, toonden aan dat HSD3B7 niet alleen actief is in kankercellen maar ook in meerdere typen immuun- en ondersteunende cellen. Hoge niveaus van dit gen waren geassocieerd met een netwerk van signalen die angiogenese, chronische ontsteking en immuunontduiking bevorderen. Communicatie tussen bepaalde beschermende celtypen leek verzwakt, terwijl zelfversterkende lussen binnen tumorondersteunende cellen versterkt waren. Samen suggereren deze patronen dat verhoogde HSD3B7-activiteit helpt een vijandige micro-omgeving te creëren en in stand te houden die tumor groei en therapieresistentie bevordert.
Wat dit betekent voor patiënten en toekomstige zorg
In praktische termen laat dit werk zien dat gliomen zinnig kunnen worden verdeeld in drie op lipiden gebaseerde subtypen, waarbij het sfingolipiden-rijke SP-type eruit springt als bijzonder gevaarlijk en therapieresistent. Deze verschillen zijn niet alleen academisch: ze zijn afleesbaar op routine-MRI-scans met geavanceerde beeldanalyse en terug te voeren op specifieke genen zoals HSD3B7 die in de toekomst medicijntargets kunnen worden. Hoewel experimenteel werk nog nodig is om te testen of het blokkeren van deze lipidepaden tumorgroei kan vertragen of radiotherapie kan verbeteren, biedt de studie een nieuw metabool perspectief op hersenkanker en brengt ze het veld dichter bij meer gepersonaliseerde, biologisch onderbouwde behandelbeslissingen.
Bronvermelding: Tu, S., Zhang, P., Chi, X. et al. Lipid metabolism classification of gliomas. Sci Rep 16, 8219 (2026). https://doi.org/10.1038/s41598-026-37697-3
Trefwoorden: glioma, lipidenmetabolisme, beeldvorming van hersentumoren, radiomics, tumormicro-omgeving