Clear Sky Science · nl
Een vetrijk dieet herstructureert de genregulerende netwerken in het preoptische gebied
Waarom je hersenen ertoe doen bij diabetes
De meeste mensen zien diabetes vooral als een probleem van de alvleesklier en bloedsuiker, maar je hersenen spelen ook een belangrijke rol. Deze studie onderzoekt hoe een vetrijk dieet en een krachtige experimentele behandeling de genactiviteit veranderen in een klein maar cruciaal hersengebied dat het preoptische gebied heet. Door in kaart te brengen welke hersencellen "resetten" wanneer diabetes in remissie gaat, hopen de onderzoekers aanwijzingen te geven voor nieuwe therapieën die gebruikmaken van het vermogen van de hersenen zelf om de bloedsuiker te helpen reguleren.
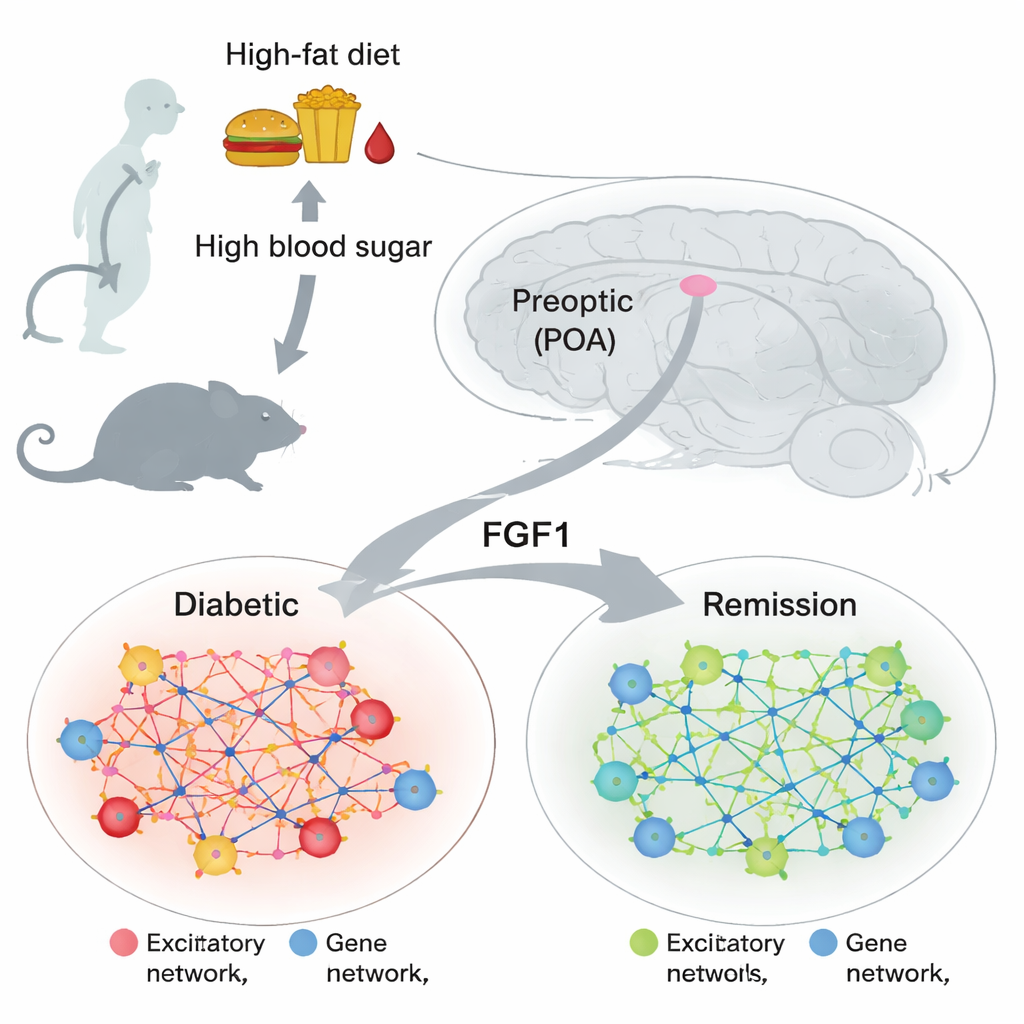
Een klein knooppunt met grote metabole invloed
Het preoptische gebied ligt aan de voorkant van de hypothalamus, een deel van de hersenen dat helpt bij de regulatie van lichaamstemperatuur, slaap, voeding en hormonale signalen. Eerder werk toonde aan dat cellen in dit gebied kunnen beïnvloeden hoe het lichaam glucose verwerkt en reageert op warmte, maar hun rol bij diabetes was nog slecht begrepen. Tegelijkertijd vonden andere studies dat een enkele dosis van een eiwit genaamd fibroblastgroeifactor 1 (FGF1), toegediend in de hersenen, obese diabetische muizen in langdurige remissie kan brengen. Dat riep een belangrijke vraag op: welke hersencellen en genprogramma’s veranderen wanneer de bloedsuiker normaliseert, en verschijnen vergelijkbare veranderingen in het preoptische gebied?
Genactiviteit per cel lezen
Om dit te beantwoorden, gebruikte het team single-cell RNA-sequencing, een techniek die meet welke genen in duizenden individuele cellen tegelijk actief zijn. Ze heranalyseerden een bestaande dataset van muizen waarvan de diabetes in remissie was geraakt na FGF1-behandeling, met focus op zenuwcellen in de hypothalamus. Met statistische hulpmiddelen identificeerden ze groepen genen die samen omhoog of omlaag gingen toen dieren van een diabetische toestand naar remissie gingen. Deze "remissie-modules" werken als vingerafdrukken van herstel: in plaats van één gen tegelijk te volgen, leggen ze gecoördineerde verschuivingen vast over veel genen binnen bepaalde typen neuronen.
Vetrijk dieet, hersencellen en verlaagde energiebehoefte
De onderzoekers vergeleken deze remissie-modules vervolgens met genactiviteit in een andere dataset die cellen uit het preoptische gebied van normale muizen bemonsterde. Ze verdeelden neuronen eerst in twee brede klassen: exciterende cellen, die de activiteit in hun circuits neigen te verhogen, en inhibitorische cellen, die deze dempen. Bij diabetische muizen behandeld met FGF1 lieten beide typen neuronen brede verminderingen zien in genen die verband houden met energieproductie—met name die betrokken bij oxidatieve fosforylering, cellulaire ademhaling en het mitochondriale apparaat dat actieve cellen van brandstof voorziet. In exciterende neuronen werd een grote "turquoise" genmodule die gekoppeld is aan energiegebruik en synaptische activiteit sterk naar beneden bijgesteld tijdens remissie, wat suggereert dat deze cellen minder metabolisch veeleisend worden wanneer de bloedsuiker onder controle is gebracht.
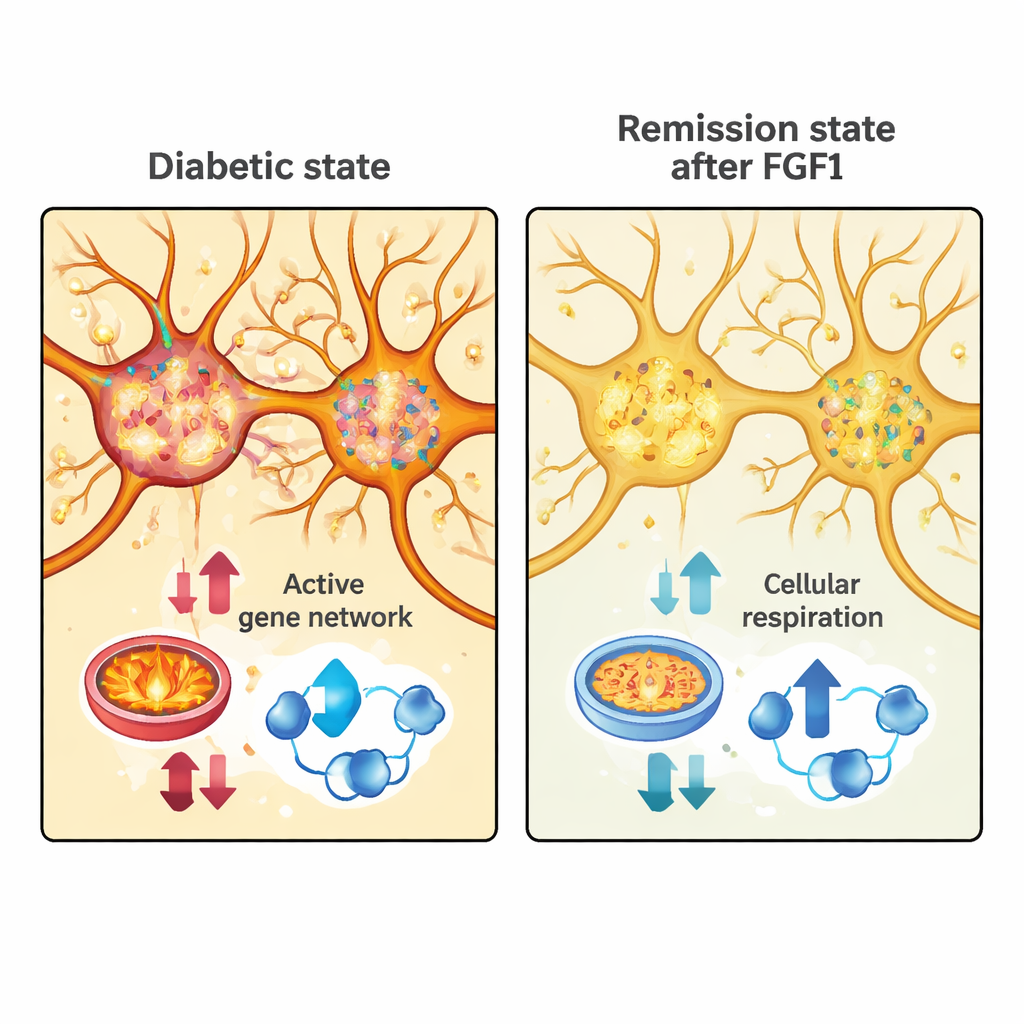
Remissiesignaturen terugvoeren naar specifieke neurongroepen
Vervolgens vroeg het team of deze remissie-gerelateerde genpatronen overeenkwamen met bepaalde celpopulaties in het preoptische gebied. Door de twee datasets computationeel samen te voegen, ontdekten ze dat sommige preoptische neuronclusters veel van dezelfde genen tot expressie brachten die veranderden bij FGF1-geïnduceerde remissie. Ze belichtten meerdere genen—zoals Trpc4, Dgkg en Ryr3—die op het kruispunt van deze analyses lagen. Met een hooggevoelige microscopiemethode genaamd RNAscope toonden ze aan dat deze genen inderdaad tot expressie komen in afzonderlijke zones van het muizenpreoptische gebied, voornamelijk in dorsale subregio’s. Dit bevestigt ze als reële merkers van specifieke neurongroepen die mogelijk meewerken aan de hersenreactie op metabole ziekte.
Wat dit betekent voor toekomstige diabetesbehandelingen
Voor niet-specialisten is de conclusie dat diabetes niet alleen een probleem van de bloedsuiker is—het is ook een probleem van hersennetwerken. De studie toont dat wanneer diabetes bij muizen in remissie gaat, bepaalde preoptische neuronen overschakelen naar een lagere energiestaat en hun genactiviteit op gecoördineerde wijze veranderen. Door deze remissie-modules te definiëren en ze te koppelen aan concrete celtypen en merkggenen, biedt het werk een routekaart voor vervolgonderzoek: onderzoekers kunnen nu deze specifieke neuronen richten om te testen hoe ze de glucoseregulatie, obesitas en aanverwante complicaties beïnvloeden. Op de lange termijn kan een beter begrip van deze hersencircuits helpen behandelingen te inspireren die organen in het lichaam aanvullen of zelfs omzeilen door het ingebouwde controlemechanisme van de hersenen over de stofwisseling te benutten.
Bronvermelding: Lazaro, O., Beimfohr, C., App, B. et al. High fat diet remodels the gene regulatory networks in the preoptic area. Sci Rep 16, 7042 (2026). https://doi.org/10.1038/s41598-026-37692-8
Trefwoorden: hersenen en diabetes, preoptisch gebied, vetrijk dieet, genenetwerken, FGF1 remissie