Clear Sky Science · nl
Identificatie van schadelijke varianten in het gehele transcriptoom van kandidaatgenen gekoppeld aan rundertuberculose (paratuberculose)
Verborgen genen achter een kostbare rundziekte
Rundertuberculose, ook bekend als Johne’s disease, ondermijnt geruisloos de gezondheid en productiviteit van melkveehouderijen wereldwijd, kost veehouders jaarlijks honderden miljoenen dollars en vergroot de zorgen over mogelijke verbanden met menselijke darmaandoeningen. Deze studie kijkt onder de genetische motorkap van Holsteinkoeien om een eenvoudige maar cruciale vraag te stellen: welke verschillen in hun genen kunnen sommige dieren helpen deze infectie te weerstaan terwijl andere eraan bezwijken? Door het lezen van RNA—de werkende kopieën van genen—in bloed en darmweefsel, volgden de onderzoekers hoe subtiele DNA-veranderingen in sleutelgenen van het immuunsysteem de loop van de ziekte kunnen sturen.
Waarom deze rundziekte ertoe doet
Paratuberculose wordt veroorzaakt door de bacterie Mycobacterium avium subspecies paratuberculosis (MAP). Koeien raken meestal vroeg in hun leven geïnfecteerd, maar tekenen verschijnen vaak pas jaren later. In de stille en subklinische stadia lijken dieren gezond maar kunnen wel lage niveaus bacteriën uitscheiden en minder melk produceren. In klinische stadia ontwikkelen ze chronische diarree, ernstig gewichtsverlies en aanzienlijke dalingen in melkproductie. Herd-niveaus van infectie kunnen in veel regio’s, waaronder delen van Europa en Noord-Amerika, boven de 50% uitkomen, wat een economische en dierenwelzijnsuitdaging vormt. Omdat de bacterie ook als omgevingsfactor voor menselijke ontstekingsziekten zoals de ziekte van Crohn kan fungeren, neemt de druk toe om de beheersingsstrategieën bij rundvee te verbeteren.
Het werkende genoom lezen
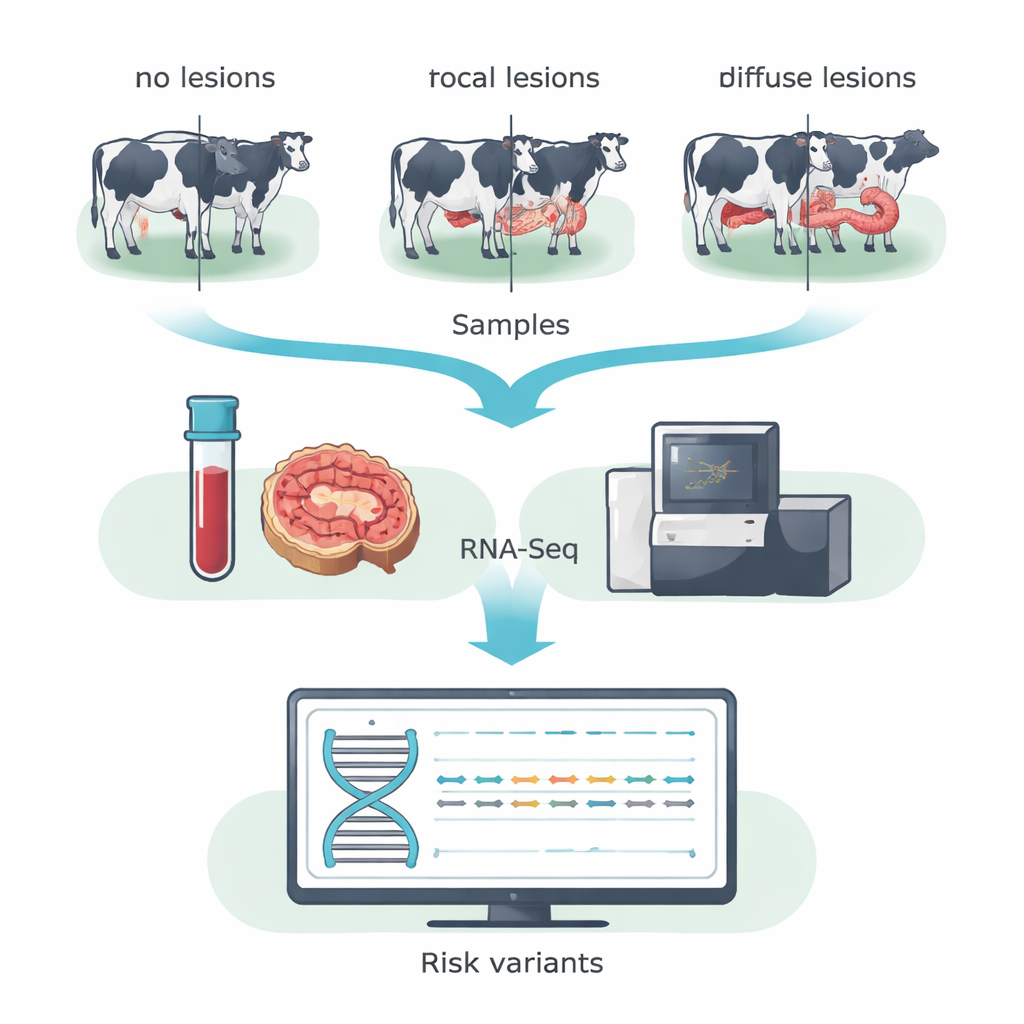
In plaats van het hele DNA te scannen, gebruikte het team RNA-sequencing (RNA-Seq) om zich te richten op genen die daadwerkelijk actief zijn in het dier. Ze verzamelden bloed en monsters van de ileocaecale klep—een darmregio die sterk door MAP wordt aangetast—van 14 Holsteinkoeien uit een Spaanse melkveestal. Op basis van microscopisch onderzoek van darmweefsels werden koeien in drie categorieën ingedeeld: dieren zonder aantoonbare laesies, dieren met kleine, gelokaliseerde (focale) laesies typisch voor langdurige subklinische infectie, en dieren met ernstige, wijdverspreide (diffuse) laesies geassocieerd met klinische ziekte. Door data van bloed en darm binnen elke groep samen te voegen, vergrootten de onderzoekers hun vermogen om enkele-letter-DNA-veranderingen in geëxprimeerde genen te detecteren, bekend als coderende SNP’s.
Schadelijke veranderingen in sleutelgenen van het immuunsysteem vinden
Uit honderden duizenden varianten richtte het team zich op die welke de eiwitsequentie veranderen en waarvan voorspeld wordt dat ze de eiwitfunctie schaden—zogenoemde deleterie varianten. Ze pasten strenge filters toe om hoge betrouwbaarheid te waarborgen en gebruikten gevestigde predictietools om risicovolle veranderingen aan te wijzen. Dit filterproces onthulde 31 dergelijke varianten uniek voor koeien zonder laesies, 15 uniek voor koeien met focale laesies en 31 uniek voor koeien met diffuse laesies. Veel van deze vielen in genen die bepalen hoe immuuncellen infecties herkennen en opruimen, celdood reguleren en metabolisme beheren. Opvallend was de BOLA-genfamilie, de rundervariant van het major histocompatibility complex klasse II, die immuuncellen helpt bacteriële fragmenten aan T-cellen te presenteren. Verschillende mogelijk schadelijke varianten in BOLA werden in alle drie de koegroepen gevonden, wat suggereert dat specifieke BOLA-varianten dieren kunnen sturen richting resistentie, gecontroleerde infectie of schadelijke ontsteking.
Van DNA-varianten naar ziektepaden
Om te begrijpen wat deze gènesveranderingen in de praktijk kunnen betekenen, onderzochten de onderzoekers welke biologische paden in elke groep verrijkt waren. Koeien zonder laesies vertoonden gewijzigde varianten in genen die verbonden zijn met antigeenverwerking, vesikeltransport en intestinale immuimbalans, inclusief BOLA, AP3B1 en CHGA. Deze veranderingen kunnen efficiënte afbraak van bacteriën binnen immuuncellen en een stabiele darmomgeving bevorderen die schade beperkt. Bij koeien met focale laesies concentreerden schadelijke varianten zich in genen (ORMDL3 en KANK2) die geprogrammeerde celdood onderdrukken en cellulair metabolisme afstemmen, mogelijk waardoor de gastheer het aantal bacteriën laag kan houden tijdens een lange, subklinische fase. Bij koeien met diffuse laesies wezen de aangetaste genen op overactieve immuunpaden zoals Th1/Th2-celdifferentiatie en antigeenpresentatie, samen met galtransport- en medicijnresponspaden. Hier kunnen gewijzigde BOLA-genen een sterke, soms zelfschadende ontstekingsreactie stimuleren, wat echo’s oproept van patronen die gezien worden bij veel menselijke auto-immuun- en ontstekingsziekten.
Aanwijzingen voor het fokken van veerkrachtigere kuddes
Naast het verduidelijken van hoe verschillende genetische varianten de immuunrespons tegen MAP vormen, koppelde de studie deze risicovolle veranderingen ook aan bekende regio’s van het rundergenoom die geassocieerd zijn met gezondheidseigenschappen, waaronder gevoeligheid voor paratuberculose en andere infecties. Hoewel deze resultaten nog validatie vereisen in grotere kuddes en nog niet als op zichzelf staande diagnostische markers kunnen worden gebruikt, bieden ze een veelbelovend overzicht van kandidaatvarianten en -genen. Eenvoudig gezegd suggereert het werk dat sommige koeien genvarianten dragen die hen helpen infectie stilletjes onder controle te houden, terwijl anderen varianten dragen die runaway-ontsteking en ernstige ziekte bevorderen. In de toekomst zou dergelijke informatie selectief fokken en genetische tests kunnen ondersteunen die kuddes naar grotere natuurlijke resistentie sturen, waardoor zowel economische verliezen als de behoefte aan intensieve beheersmaatregelen afnemen.
Bronvermelding: Badia-Bringué, G., Lam, S., Cánovas, Á. et al. Whole-transcriptome identification of deleterious variants in candidate genes linked to bovine paratuberculosis. Sci Rep 16, 6243 (2026). https://doi.org/10.1038/s41598-026-37675-9
Trefwoorden: bovine paratuberculosis, Johne’s disease genetics, dairy cattle immunity, RNA sequencing, disease resistance breeding