Clear Sky Science · nl
Medische beeldvorming en deep learning inzetten voor de diagnose van borstkanker met histopathologische afbeeldingen
Waarom vroeg opsporen ertoe doet
Borstkanker is een van de belangrijkste oorzaken van kankerdoden bij vrouwen wereldwijd, maar de uitkomsten verbeteren aanzienlijk wanneer de ziekte vroeg wordt ontdekt. Artsen diagnosticeren borstkanker doorgaans door kleine weefseldunnetjes onder een microscoop te onderzoeken — een proces dat histopathologie wordt genoemd. Deze beelden bevatten rijke details over of cellen onschadelijk of gevaarlijk zijn, maar het lezen ervan is tijdrovend en kan per specialist verschillen. Deze studie onderzoekt hoe moderne kunstmatige intelligentie pathologen kan helpen borstkanker sneller en consistenter te herkennen, wat patiënten mogelijk sneller duidelijkheid en effectievere behandelingsopties kan bieden.
Een nadere blik op weefselbeelden
Onder de microscoop laat borstweefsel zich niet netjes opdelen in “gezond” en “kankerachtig.” Cellen overlappen, kleuren variëren per laboratorium en subtiele veranderingen in vorm of textuur kunnen levensbelangrijke betekenis hebben. Traditionele computerondersteunde systemen worstelden met deze complexiteit omdat ingenieurs handmatig de kenmerken moesten ontwerpen waarop de computer moest letten, en kleine veranderingen in kleuring of beeldkwaliteit hen al uit balans konden brengen. Deep learning, een tak van kunstmatige intelligentie die patronen direct uit data leert, heeft de afgelopen jaren de manier waarop computers beelden interpreteren getransformeerd, inclusief medische scans. De auteurs bouwen voort op deze vooruitgang om een systeem te ontwerpen dat is toegesneden op de rommelige realiteit van borstweefselpreparaten.
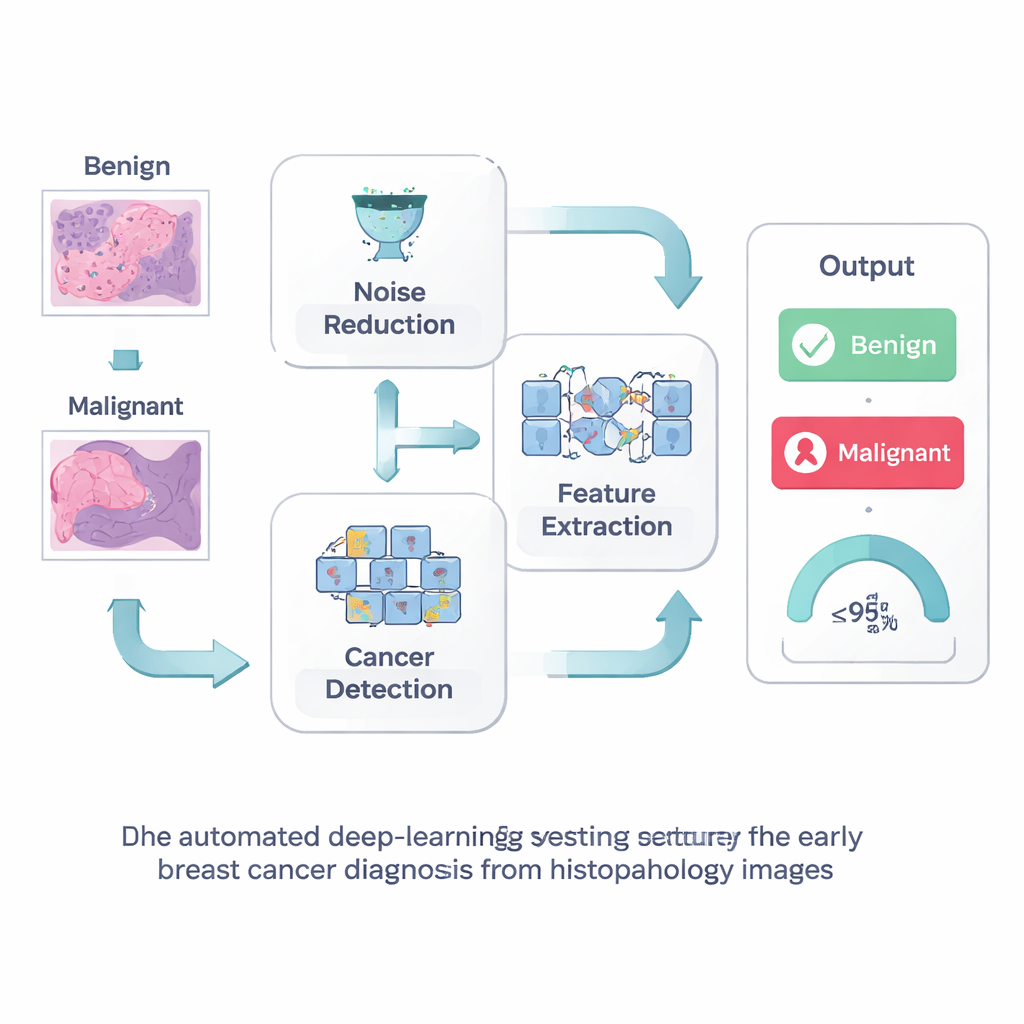
Het beeld schoonmaken voordat je het leest
De eerste stap in hun aanpak is eenvoudig maar krachtig: het beeld opschonen voordat je de computer het laat interpreteren. Histopathologische preparaten bevatten vaak visuele “ruis” door het kleuring- en afbeeldingsproces, wat de fijne structuren die vroege kanker signaleren kan verbergen. De onderzoekers gebruiken een techniek genaamd Wiener-filtering, die willekeurige spikkels wegvlakt terwijl scherpe randen en kleine details zoals celgrenzen en kleine klompjes behouden blijven. Door de computer een helderder beeld te presenteren helpt deze stap zowel gemiste kankers als valse alarmen te voorkomen die patiënten naar onnodige vervolgonderzoeken zouden kunnen sturen.
De computer leren waarop te letten
Vervolgens zet het team een verfijnd deep‑learningmodel in, bekend als SE‑ResNet, om de opgeschoonde beelden te bestuderen. In eenvoudige woorden scant dit model het preparaat stukje voor stukje en bouwt geleidelijk een interne “vocabulaire” van visuele patronen op: hoe normale kanaaltjes eruitzien, hoe tumorcellen zich groeperen en hoe texturen veranderen naarmate kanker agressiever wordt. Een ingebouwd aandachtsmechanisme helpt het netwerk om de meest informatierijke beeldkanalen te benadrukken en irrelevante achtergrond te onderdrukken. Dit maakt het model gevoeliger voor subtiele, ziektegerelateerde patronen en tegelijk efficiënt genoeg om op apparatuur in echte ziekenhuizen te kunnen draaien.
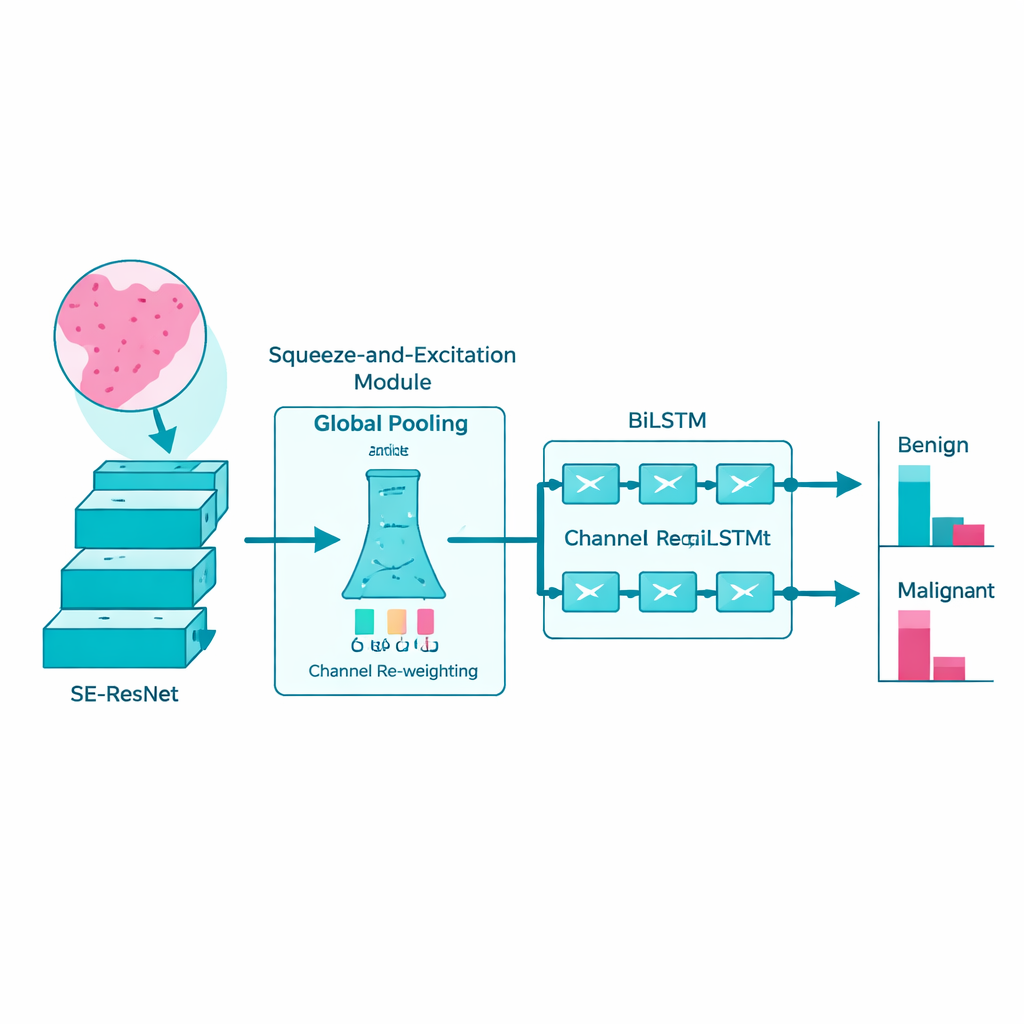
Patronen ruimtelijk volgen als een verhaal
In plaats van elk weefselstukje als een geïsoleerde foto te behandelen, erkennen de onderzoekers dat ziekteverschijnselen zich vaak als een verhaal over het preparaat ontvouwen. Om dit vast te leggen voeren zij de door SE‑ResNet geëxtraheerde kenmerken in een bidirectioneel long short‑term memory‑netwerk, of BiLSTM. Dit type model is ontworpen om sequenties te begrijpen: het kijkt hoe patronen van het ene gebied naar het andere veranderen, zowel vooruit als achteruit, vergelijkbaar met het lezen van een zin in beide richtingen om de volledige betekenis te vatten. Door deze ruimtelijke relaties te leren, wordt de BiLSTM beter in het onderscheiden van goedaardige veranderingen en werkelijk kwaadaardige afwijkingen.
Hoe goed het systeem in de praktijk werkt
De auteurs hebben hun volledige pijplijn — ruisreductie, feature‑learning en sequentiemodellering — getest op grote openbare verzamelingen van borstweefselbeelden, waaronder de veelgebruikte BreakHis‑dataset. Ze verdeelden de data in trainings‑ en testgroepen met verschillende verhoudingen en vergeleken hun methode met tal van gevestigde deep‑learningmodellen. Over deze experimenten heen classificeerde hun systeem goedaardige versus kwaadaardige monsters bijna 99% van de tijd correct, liet het betere prestaties zien dan concurrerende methoden en draaide het bovendien sneller. Het model bleef sterk bij verschillende vergrotingen van het weefsel, wat suggereert dat het zich kan aanpassen aan preparaten die onder wisselende omstandigheden zijn gemaakt. De studie noemt echter ook beperkingen: de datasets zijn nog van bescheiden omvang, het model richt zich op een eenvoudige tweeklassebeslissing in plaats van gedetailleerde tumortypen, en het is nog niet bewezen in echte klinische werkwijzen.
Wat dit betekent voor patiënten en artsen
Voor de leek is de belangrijkste boodschap dat computers veel beter worden in het lezen van microscoopbeelden van borstweefsel en het markeren van verdachte gebieden. Het voorgestelde systeem vervangt de patholoog niet; het fungeert als een zeer oplettende assistent die regio’s aangeeft die waarschijnlijk kankergevoelig zijn en een second opinion biedt met zeer hoge nauwkeurigheid. Als het gevalideerd wordt in grotere en meer diverse patiëntengroepen, kunnen zulke hulpmiddelen de tijd tot diagnose verkorten, de kans verkleinen dat een kleine kanker wordt gemist en overbelaste ziekenhuizen helpen om toenemende patiëntenaantallen te verwerken. Toekomstig werk zal het nodig hebben de methode op meer gevarieerde preparaten te testen en deze te integreren in dagelijkse laboratoriumroutines, maar deze studie laat zien dat zorgvuldig ontworpen deep‑learningsystemen een krachtige bondgenoot kunnen zijn in de strijd tegen borstkanker.
Bronvermelding: Nagalakshmi, V., Ahammad, S.H. Leveraging medical imaging and deep learning for diagnosis of breast cancer using histopathological images. Sci Rep 16, 6236 (2026). https://doi.org/10.1038/s41598-026-37663-z
Trefwoorden: borstkankerdiagnose, histopathologie afbeeldingen, deep learning, medische beeldvorming, computerondersteunde detectie