Clear Sky Science · nl
Type I-interferonsignaal definieert een nieuw ziektesignatuur in xeroderma pigmentosum C menselijke keratinocyten
Waarom zonlicht voor sommige mensen zo gevaarlijk kan zijn
Voor de meesten van ons staat zonlicht voor warmte en vitamine D. Maar voor mensen met een zeldzame erfelijke aandoening genaamd xeroderma pigmentosum C (XP-C) kan zelfs bescheiden daglicht ernstige huidschade veroorzaken en het risico op huidkanker extreem verhogen. Deze studie kijkt verder dan het bekende DNA-herstelprobleem bij XP-C en onthult een verborgen laag van overactieve, immuunachtige signaalvoering binnen hun huidcellen, wat nieuwe aanwijzingen biedt waarom hun huid zo kwetsbaar en ontstoken wordt na blootstelling aan de zon.
Wanneer DNA-herstel in de huid faalt
Onze huidcellen repareren voortdurend DNA-schade veroorzaakt door ultraviolet B (UVB)-straling van de zon. Een eiwit genaamd XPC is een van de eerste “sensoren” die UV-geïnduceerde beschadigingen herkent en een groot reparatieteam op gang brengt. Bij XP-C maken mutaties in het XPC-gen deze vroege waarschuwingsstap onbruikbaar, waardoor UV-schade zich ophoopt in plaats van wordt hersteld. Patiënten met XP-C krijgen duizenden malen vaker huidkanker dan de algemene bevolking en moeten zonlicht strikt vermijden. Hoewel dit defect in DNA-herstel goed bekend is, is veel minder duidelijk hoe het de interne communicatiesystemen van de cellen herschakelt—vooral diegenen die ontsteking regelen.
Cellulaire signalen in de tijd onderzoeken
Om dit probleem aan te pakken, creëerden de onderzoekers menselijke keratinocyten—de belangrijkste cellen in de buitenste huidlaag—die volledig geen XPC meer bevatten en vergeleken die met anders identieke normale cellen. Ze bestraalden beide celtypen met een zorgvuldig gekozen, realistische UVB-dosis vergelijkbaar met een matige verbranding. Daarna onderzochten ze de cellen in twee fasen. Een uur na bestraling maten ze de activiteit van vele enzymen genaamd proteïne-tyrosinekinasen, die signalen aan- en uitzetten door kleine fosfaatlabels toe te voegen. Vierentwintig uur later gebruikten ze geavanceerde massaspectrometrie om een breed overzicht van duizenden eiwitten te maken en te zien welke in hoeveelheid toenamen of afnamen. Deze tweeledige aanpak stelde hen in staat zowel de vroege “alarmsignalen” als de latere “downstream-responsen” binnen de cellen te volgen.
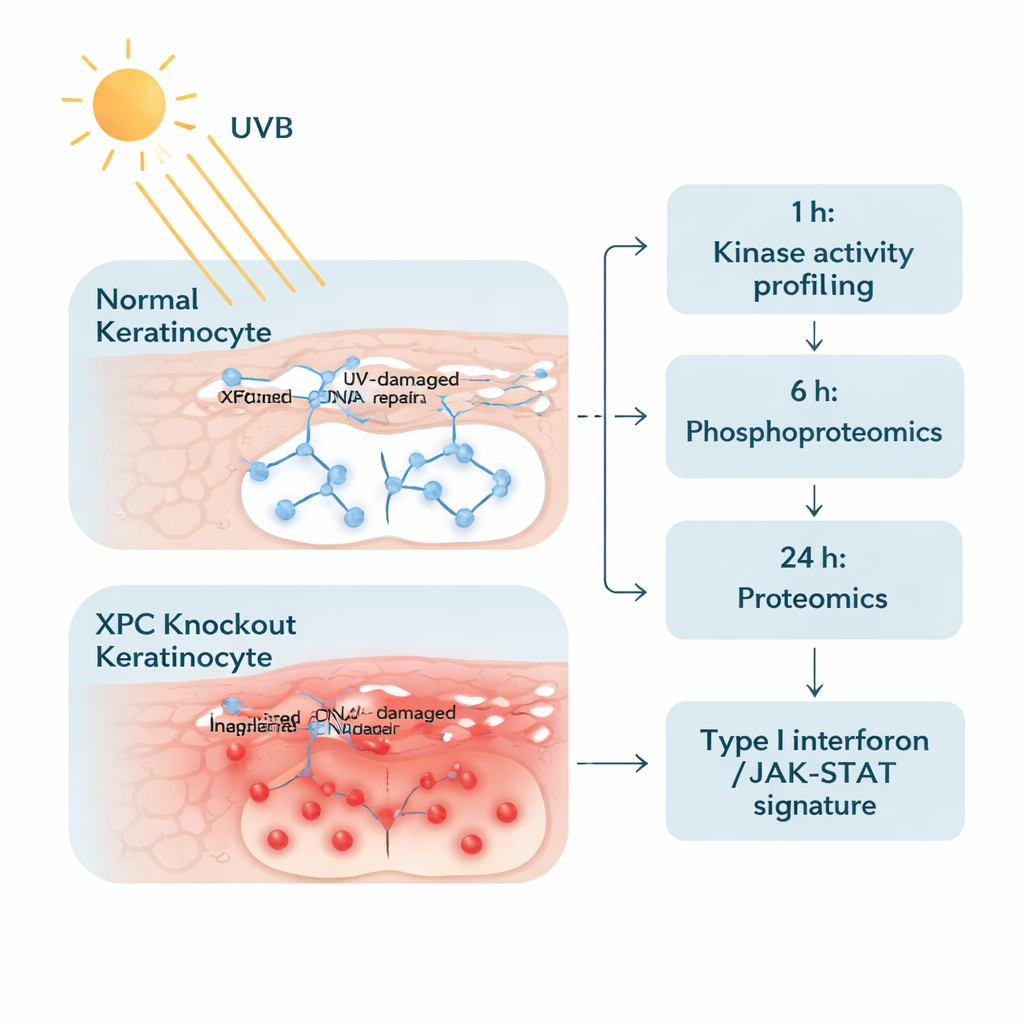
Een ontstekingsroute licht op
De vroege kinasescreen toonde aan dat XPC-deficiënte keratinocyten op UVB reageren met een toename van fosforylering op meer dan honderd sites vergeleken met normale cellen. Opmerkelijk was dat veel van deze veranderingen zich concentreerden in de JAK/STAT-signaleringsroute—een centrale communicatieweg die normaal gesproken wordt gebruikt door immuunboodschappers zoals interferonen. Merkers gekoppeld aan JAK1, JAK2, JAK3, TYK2 en STAT-eiwitten waren actiever in XP-C-cellen, zelfs vóór UVB, en werden na bestraling verder versterkt. Dit suggereert dat de cellen zich in een “hoge-alert”-toestand bevinden, klaar om ontstekingssignalen te versterken telkens wanneer ze UV-geïnduceerde stress tegenkomen.
Interferonachtige alarmsgenen in huidcellen
De latere, bredere eiwitanalyse bevestigde en breidde dit beeld uit. In XPC-knockoutcellen, vooral na UVB, waren honderden eiwitten veranderd en een grote cluster correspondeerde met genen die normaal worden ingeschakeld door type I-interferonen—dezelfde antivirale signalen die ons lichaam gebruikt om infecties te bestrijden. Eiwitten zoals MX1, MX2, IFIT1, IFIT2, IFIT3, ISG15, OAS1 en IRF9, klassieke “interferon-gestimuleerde genen”, waren sterk verhoogd. Netwerk- en routeanalyses brachten deze eiwitten terug naar JAK/STAT- en type I-interferonsignalering als het dominante thema. Vervolg-westernblotexperimenten bevestigden dat sleutel-STAT-eiwitten zwaarder gefosforyleerd waren en dat deze interferon-responsieve eiwitten in veel hogere niveaus werden geproduceerd in XP-C-cellen dan in normale keratinocyten, zowel in rust als vooral na UVB.
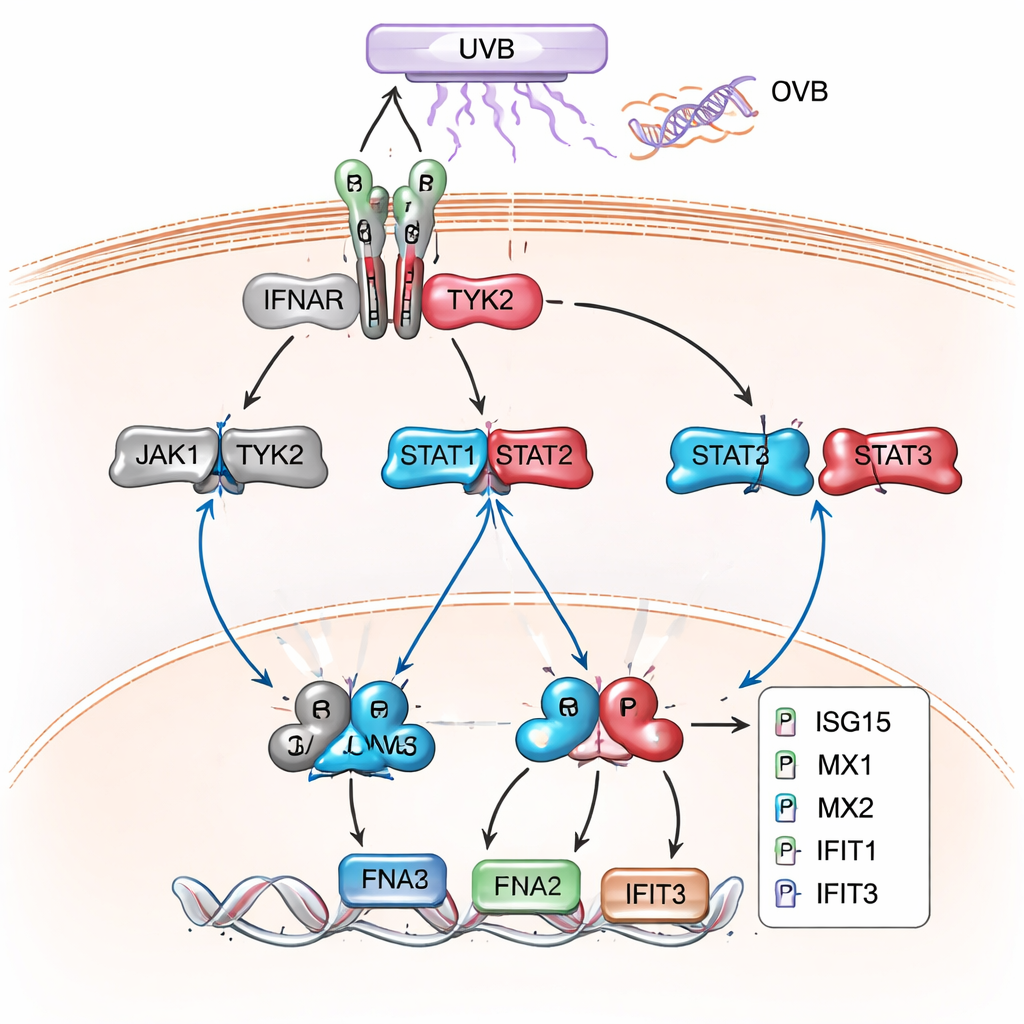
Wat dit betekent voor patiënten en toekomstige behandelingen
Gezamenlijk laten deze resultaten zien dat XP-C niet alleen een ziekte is van gebrekkig DNA-herstel; het wordt ook gekenmerkt door een aanhoudende, interferonachtige ontstekingsstatus in huidcellen, gestuurd via de JAK/STAT-route en versterkt door UV-licht. Voor een leek betekent dit dat XP-C-keratinocyten zich gedragen alsof ze voortdurend een onzichtbare infectie bestrijden telkens wanneer ze zonlicht zien, waardoor chronische ontsteking bovenop ongerepareerde DNA-schade komt te liggen. Hoewel de studie geen behandelingen direct toetst, wekt ze de mogelijkheid dat zorgvuldig afgestemde geneesmiddelen die JAK/STAT of verwante ontstekingscircuits remmen, op een dag kunnen helpen de door UV getriggerde schade bij XP-C te verminderen en misschien ook bij andere ontstekingshuidziekten die dit moleculaire patroon delen.
Bronvermelding: Nasrallah, A., Rezvani, HR., Belmudes, L. et al. Type I interferon signaling defines a novel disease signature in xeroderma pigmentosum C human keratinocytes. Sci Rep 16, 6559 (2026). https://doi.org/10.1038/s41598-026-37662-0
Trefwoorden: xeroderma pigmentosum, huidkanker, DNA-herstel, interferonsignalering, JAK STAT-route