Clear Sky Science · nl
APOL1-plasmamembraanpools weerstaan snelle proteïneafbraak
Waarom het “verdwijnen” van een nierproteïne ertoe doet
Een groot deel van ernstige nierziekten bij mensen met recente Afrikaanse voorouders is terug te voeren op twee varianten van één gen, APOL1. Wetenschappers worstelen echter nog steeds om precies te begrijpen hoe dit gen niercellen beschadigt zonder de meeste dragers te schaden. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote implicaties: zodra het APOL1‑proteïne in cellen is gemaakt, hoe lang blijft het aanwezig en waar is het het meest stabiel? De antwoorden onthullen een verrassende tweedeling — APOL1 wordt snel afgebroken binnenin cellen, maar blijft hardnekkig stabiel wanneer het ingebed is in het buitenoppervlak van de cel, een aanwijzing die toekomstige therapieën kan sturen.
Risicogen met een dubbele kant
Het APOL1-gen helpt mensen beschermen tegen bepaalde parasieten, een evolutionair voordeel dat waarschijnlijk verklaart waarom de risicovarianten, G1 en G2, veel voorkomen in Afrikaanse populaties. Helaas hebben mensen die twee kopieën van deze varianten erven een sterk verhoogd risico op nierstoornissen die samen APOL1‑gemedieerde nierziekten worden genoemd. Eerder werk toonde aan dat wanneer APOL1‑niveaus stijgen — vaak als reactie op ontsteking — het proteïne toxisch kan worden, vooral in kwetsbare nierfiltercellen, de zogenaamde podocyten. Maar de meeste studies richtten zich op wat APOL1 aanzet. Veel minder was bekend over hoe cellen het weer uitschakelen, bijvoorbeeld door het proteïne af te breken.
Een fragiel proteïne volgen binnenin cellen
Om de stabiliteit van APOL1 te onderzoeken, maakten de onderzoekers menselijke cellijnen die fluorescent gelabelde versies van APOL1 en zijn naaste verwant, APOL2, produceerden. Zo konden ze volgen hoeveel van elk proteïne zich ophoopte of verdween onder verschillende omstandigheden met behulp van western blotting, microscopie en flowcytometrie. Ze blokkeerden het belangrijkste eiwit‑vermalende systeem van de cel, het proteasoom, en blokkeerden apart de nieuwe eiwitsynthese. Wanneer het proteasoom werd geremd, stegen de APOL1‑niveaus snel, wat aantoont dat het normaal gesproken in hoog tempo wordt afgebroken. Wanneer de nieuwe eiwitsynthese werd gestopt, daalden APOL1‑niveaus snel. In scherp contrast veranderde APOL2 nauwelijks onder een van beide behandelingen, wat het tot een veel stabieler proteïne maakt. Belangrijk is dat de hoge omloopsnelheid van APOL1 hetzelfde was voor de normale versie (G0) en de nier‑risicoversies (G1 en G2), en dat dit gold voor meerdere van nature voorkomende APOL1‑vormen die verschillen in hoe ze in membranen liggen.
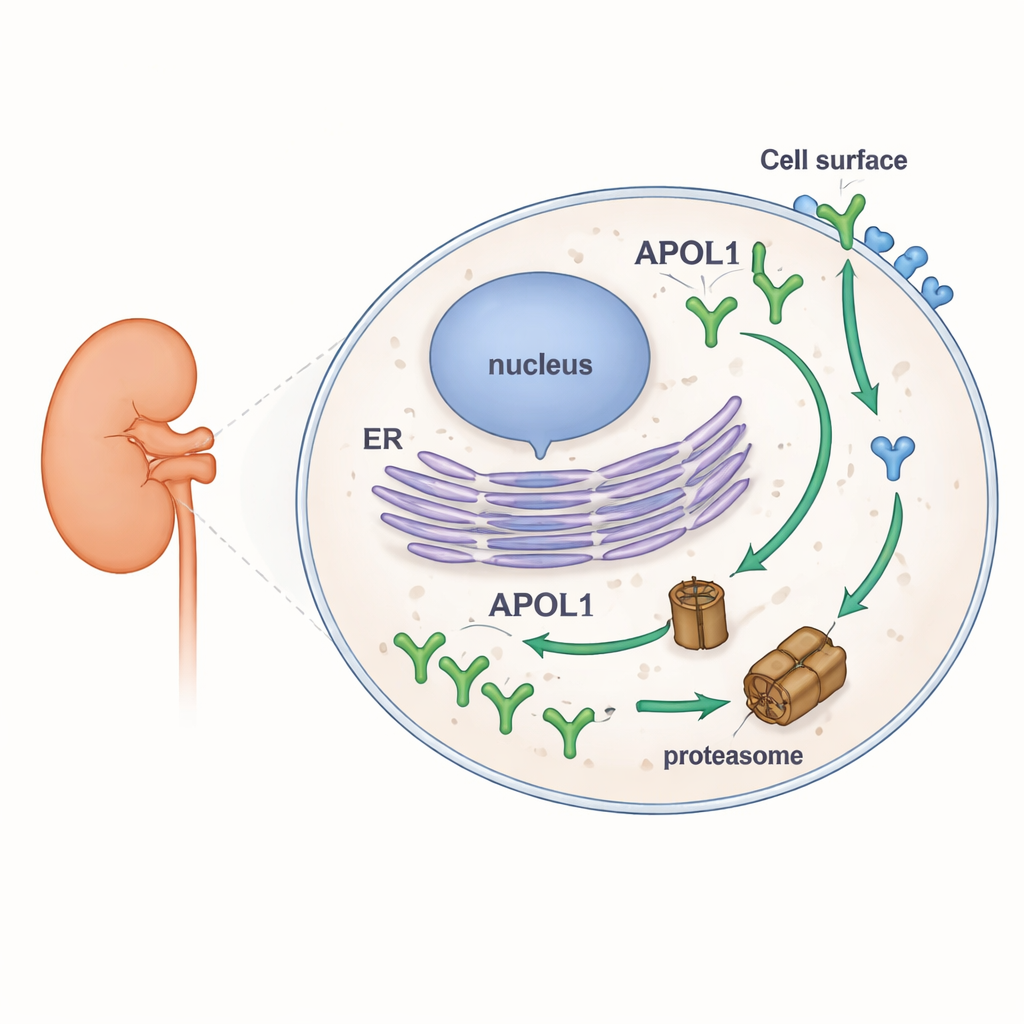
Sequentieaanwijzingen en een verhaal van twee buurten
Diepgaand in de structuur van het proteïne gebruikten de onderzoekers computertools om APOL1 en APOL2 te scannen op slappe, ongestructureerde segmenten die bekendstaan als intrinsiek ongeordende regio’s. Dergelijke regio’s fungeren vaak als “eet mij”-signalen voor het proteasoom. Ze identificeerden twee sterke kandidaatregio’s in APOL1 die grotendeels afwezig waren in APOL2. Om te testen of het unieke voorste deel van APOL1 bijdraagt aan zijn broosheid, creëerden ze hybriden: een verkorte APOL1 zonder de eerste 59 aminozuren, en een APOL2‑chimera die dat APOL1‑segment droeg. Het toevoegen van APOL1’s N‑terminale stukje aan APOL2 zorgde ervoor dat APOL2 sneller afgebroken werd, terwijl de verkorte APOL1 onstabiel bleef, wat suggereert dat meer dan één deel van APOL1 snelle afbraak bevordert. Gezamelijk koppelen deze resultaten APOL1’s ongebruikelijke flexibele segmenten aan zijn snelle omloopsnelheid, zonder dit gedrag specifiek te verbinden aan de ziekteveroorzakende varianten.
Hardnekkig proteïne aan het celoppervlak
De meest opmerkelijke bevinding verscheen toen de auteurs een onderscheid maakten tussen APOL1 binnenin de cel en APOL1 op het celoppervlak. Met behulp van antilichamen die alleen dat deel van APOL1 herkennen dat naar buiten is gericht, maten ze oppervlaktespiegels apart van de totale spiegels. Binnenin de cel gedroeg APOL1 zich zoals verwacht: het stapelde zich op wanneer het proteasoom werd geblokkeerd en verdween snel wanneer nieuwe synthese werd stopgezet. Oppervlakte‑APOL1 veranderde echter nauwelijks onder een van beide condities. Zodra APOL1‑moleculen het plasmamembraan bereikten, bleken ze zeer resistent tegen snelle afbraak. Bovendien, hoewel de risicovarianten minder totaal APOL1 produceerden dan de normale versie, waren hun oppervlaktespiegels vergelijkbaar. Dit suggereert dat risico‑ en normale APOL1 met vergelijkbare snelheden in de cel worden verwijderd, maar dat de membraan‑gebonden pools — waarvan wordt gedacht dat ze ionkanalen vormen en toxiciteit aanjagen — in alle varianten behouden blijven.
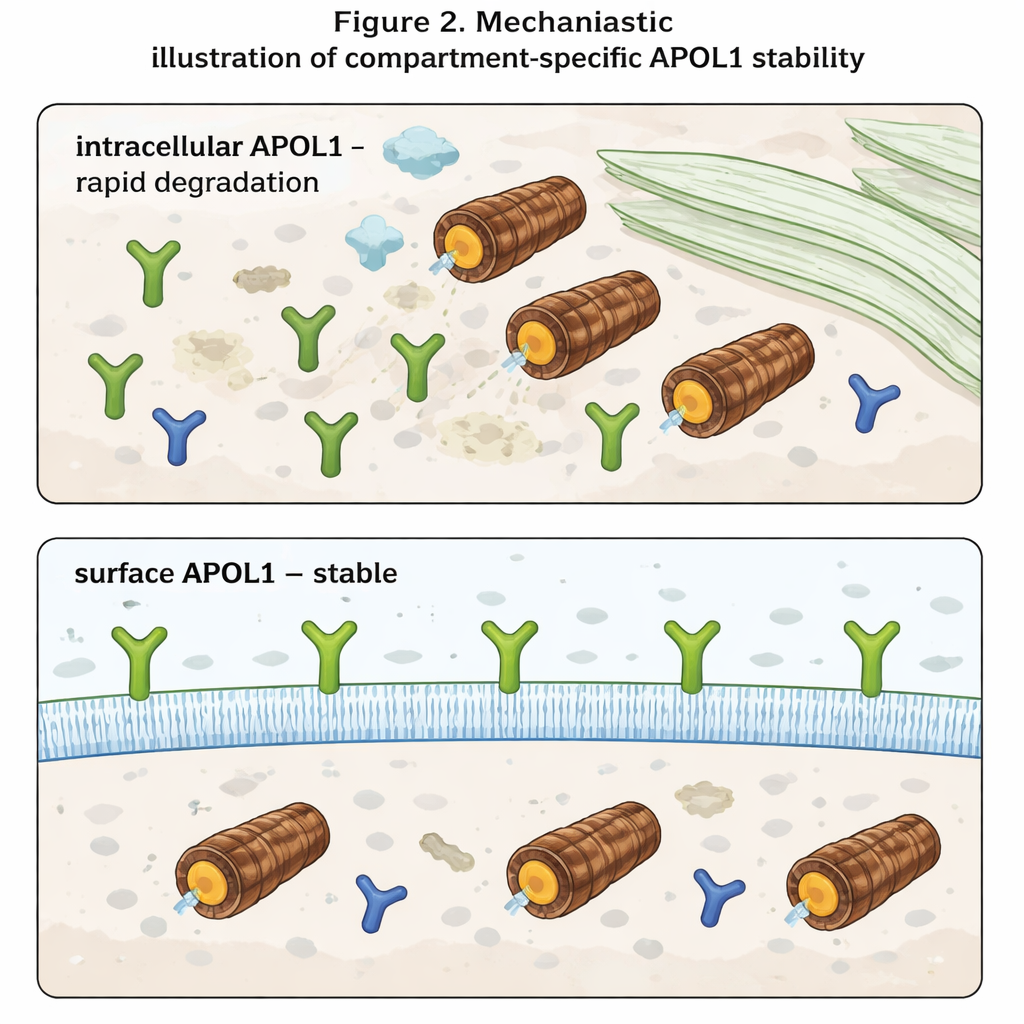
Wat dit betekent voor toekomstige behandelingen
Voor niet‑specialisten is de hoofdboodschap dat APOL1 zich erg verschillend gedraagt, afhankelijk van waar het zich bevindt. Binnenin de cel is het een kortlevend proteïne, snel herkend en afgebroken. Aan het celoppervlak wordt het langlevend en relatief beschermd, zelfs wanneer het afbraaksysteem van de cel verandert. Omdat de ziekte lijkt te ontstaan wanneer APOL1‑kanalen aan het oppervlak het evenwicht van ionen zoals natrium en kalium verstoren, moeten therapieën zich mogelijk minder richten op totale APOL1‑niveaus en meer op hoeveel ervan het plasmamembraan bereikt en daar blijft bestaan. Strategieën die het verkeer van APOL1 naar het oppervlak verminderen of selectief de oppervlaktpool destabiliseren, zouden in principe nierbeschadiging kunnen dempen zonder volledig de gunstige immuunfuncties van het gen uit te schakelen.
Bronvermelding: Höffken, V., Alvermann, L., Niggemeier, D. et al. APOL1 plasma membrane pools resist rapid protein degradation. Sci Rep 16, 6718 (2026). https://doi.org/10.1038/s41598-026-37647-z
Trefwoorden: APOL1, nierziekte, proteïneafbraak, plasmamembraan, proteasoom