Clear Sky Science · nl
Verbeterde meropenemactiviteit door een peptide uit het microbioom dat oxacillinasen 48-carbapenemase bij carbapenemresistente Klebsiella pneumoniae-isolaten target
Waarom dit van belang is voor alledaagse gezondheid
Antibioticaresistentie maakt infecties die vroeger behandelbaar waren steeds moeilijker en soms onmogelijk te genezen, vooral in ziekenhuizen. Deze studie onderzoekt een nieuwe manier om een bestaand antibioticum van laatste redmiddel, meropenem, weer effectief te maken tegen een gevaarlijke bacterie genaamd Klebsiella pneumoniae, die vaak IC-patiënten besmet. In plaats van een gloednieuw geneesmiddel te ontwikkelen, testen de onderzoekers een klein hulpmolecuul — een peptide afkomstig uit het humane microbioom — dat één van de belangrijkste weerstandsmiddelen van de bacterie uitschakelt zodat meropenem weer kan werken.
Een hardnekkige ziekenhuisbacterie en haar chemische schild
Klebsiella pneumoniae is een veelvoorkomende veroorzaker van longontsteking, bloedbaaninfecties en urineweginfecties bij opgenomen patiënten. Sommige stammen zijn resistent geworden tegen carbapenems, een krachtige klasse antibiotica die artsen normaal gesproken reserveren voor ernstige, moeilijk te behandelen gevallen. Veel van deze bacteriën produceren een speciaal enzym, OXA-48, dat als een chemisch schild functioneert en carbapenemmiddelen afbreekt voordat ze de microbe kunnen doden. In het Midden-Oosten, inclusief Iran, komen OXA-48-producerende stammen bijzonder veel voor, en de behandelopties slinken nu ook omdat weerstand tegen nieuwere geneesmiddelcombinaties opduikt. Dit maakt OXA-48 een prioriteitsdoel voor nieuwe therapieën.
Ontwerpen van een hulppeptide uit het menselijke microbioom
De onderzoekers gebruikten eerder computermodellen om databases van natuurlijke menselijke antimicrobiële peptiden — korte eiwitfragmenten gemaakt door ons eigen lichaam en residentiële microben — te verkennen op kandidaten die sterk aan het OXA-48-enzym zouden kunnen binden. Door virtueel docken en lange moleculaire dynamicasimulaties verfijnden ze deze kandidaten en selecteerden één peptide, M104, waarvan werd voorspeld dat het stabiel aan het actieve centrum van het enzym bindt en de functie blokkeert, terwijl het wateroplosbaar en chemisch stabiel blijft. In deze studie zetten ze M104 in het laboratorium op de proef, gecombineerd met meropenem tegen 20 patiënt-afgeleide Klebsiella-isolaten: 10 die OXA-48 produceerden en resistent waren tegen meropenem, en 10 zonder carbapenemase-enzymen die gevoelig waren voor geneesmiddelen.
Een oud antibioticum weer laten werken
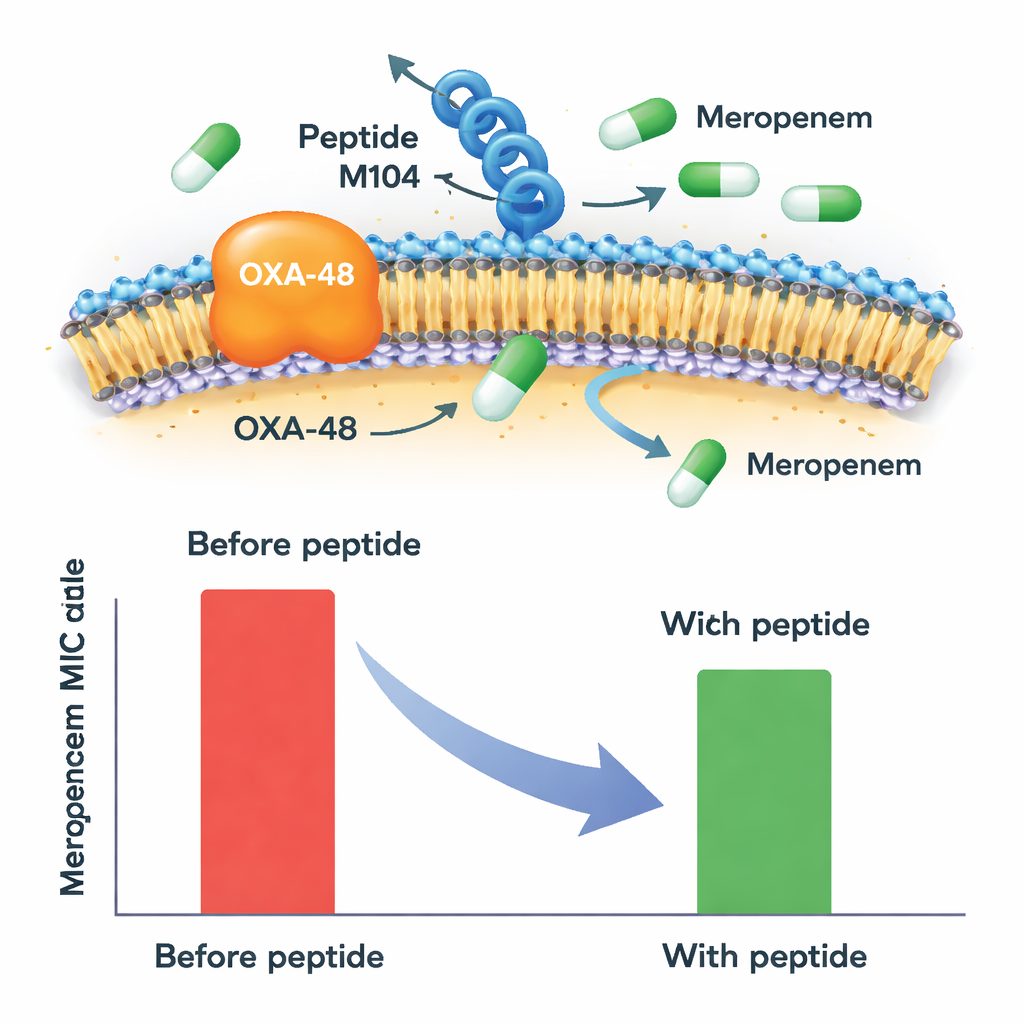
Wanneer meropenem alleen werd gebruikt, waren alle OXA-48-positieve Klebsiella-isolaten duidelijk resistent. Het toevoegen van peptide M104 veranderde dat beeld. Op het hoogste geteste niveau verminderde M104 de hoeveelheid meropenem die nodig was om bacteriegroei te stoppen met minstens de helft — en in sommige gevallen tot wel zes keer — voor elke geteste resistente OXA-48-producer. Dit duwde veel stammen van duidelijk resistent naar een intermediaire of zelfs gevoelige categorie, op basis van geaccepteerde klinische grenswaarden. Belangrijk is dat M104 op zichzelf geen dodelijk effect had en meropenem niet versterkte wanneer de bacteriën het OXA-48-enzym misten, wat wijst op een zeer specifieke werking op dat resistentiemechanisme in plaats van een brede, niet-selectieve toxiciteit.
Uitdagingen met slijmerige biofilms en veiligheidscontroles
Veel ziekenhuisinfecties omvatten biofilms — slijmerige, gelaagde bacteriegemeenschappen die zich hechten aan apparatuur en weefsels en veel moeilijker uit te roeien zijn dan vrijzwevende cellen. Het team testte daarom of M104 meropenem kon helpen bij het voorkomen van biofilmvorming of het opruimen van reeds bestaande biofilms voor Klebsiella-stammen die sterke biofilms vormen. Hoewel de peptide-meropenemcombinatie over het algemeen de hoeveelheid benodigde medicatie halveerde om biofilmgroei te blokkeren of te beginnen met het opruimen van rijpe biofilms, waren deze effecten bescheiden en bereikten ze in deze kleine steekproef geen duidelijke statistische significantie. Wat de veiligheid betreft, toonde M104 geen aantoonbare schade aan menselijke rode bloedcellen en verminderde het de levensvatbaarheid van menselijke huidfibroblasten niet na 24 uur bij een concentratie die hoger was dan in de bacterietests; pas na 48 uur daalde de celoverleving met ongeveer 10 procent. Sequentievergelijkingen suggereerden ook weinig risico dat het peptide per ongeluk andere bacteriële of menselijke eiwitten zou targeten.
Wat dit kan betekenen voor toekomstige behandelingen
Samengevat suggereren de bevindingen dat peptide M104 specifiek het OXA-48-resistentie-enzym kan uitschakelen en veel van de werkzaamheid van meropenem kan herstellen tegen anders onhandelbare Klebsiella pneumoniae, althans voor vrijzwevende bacteriën. Hoewel de impact op hardnekkige, gevestigde biofilms onder de geteste omstandigheden beperkt was, introduceert de studie de eerste gerapporteerde peptidegebaseerde remmer van OXA-48 en toont aan dat dergelijke gerichte hulpstoffen zowel effectief als relatief mild voor menselijke cellen kunnen zijn op korte termijn. Met verdere tests op meer bacteriestammen, andere carbapenemmiddelen, geoptimaliseerde formuleringen en diermodellen zou dit soort precisiemiddelen kunnen helpen de bruikbare levensduur van onze krachtigste antibiotica te verlengen, in plaats van artsen met een lege gereedschapskist tegenover resistente infecties te plaatsen.
Bronvermelding: Sadeghi, S., Faramarzi, M.A. & Siroosi, M. Enhanced meropenem activity by a microbiome derived peptide targeting oxacillinase 48 carbapenemase in carbapenem resistant Klebsiella pneumoniae isolates. Sci Rep 16, 7589 (2026). https://doi.org/10.1038/s41598-026-37644-2
Trefwoorden: antibioticaresistentie, carbapenem-resistente Klebsiella, OXA-48-enzym, meropenem, peptide-remmers