Clear Sky Science · nl
In vitro karakterisering van het katalytische domein van humane histon-deacetylase 5
Waarom kleine schakelaars in onze DNA-opslag ertoe doen
In elke cel is ons DNA omwikkeld rond eiwitten die als spoelen fungeren en helpen meters aan genetisch materiaal in een microscopische ruimte te passen. Of een gen aan- of uitgezet is, hangt vaak af van kleine chemische labels op deze spoeleiwitten. Deze studie zoomt in op één specifiek eiwit-"schakelaartje" genoemd HDAC5, dat verband houdt met hartziekten, hersenaandoeningen, kanker en meer. Door te begrijpen hoe HDAC5 op moleculair niveau werkt, hopen de onderzoekers de weg vrij te maken voor preciezere medicijnen met minder bijwerkingen.
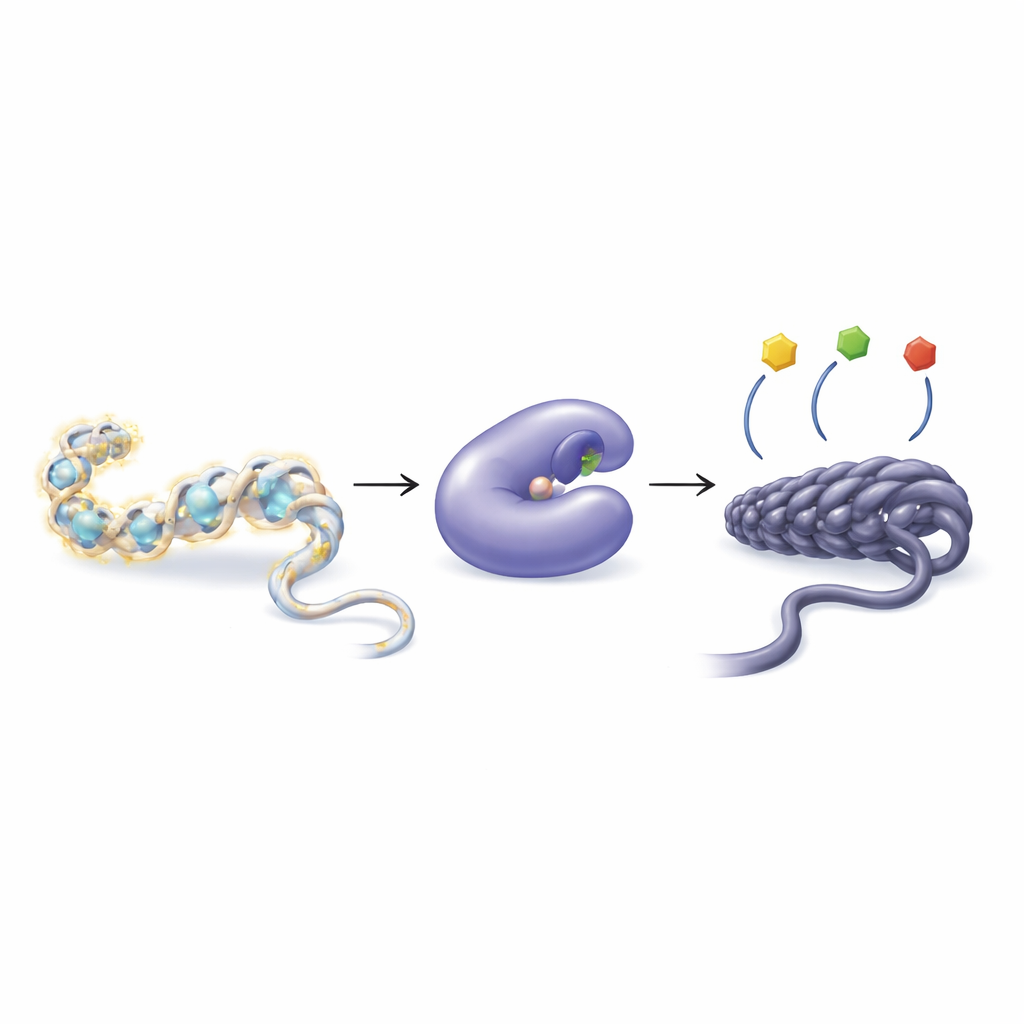
Hoe cellen genen afstemmen met kleine chemische labels
Ons DNA zweeft niet vrij maar is gewikkeld rond eiwitten die histonen worden genoemd, waarbij een structuur ontstaat die bekendstaat als chromatine. Cellen kunnen kleine chemische groepen, zoals acetylgroepen, aan histonstaarten toevoegen of ervan verwijderen om de chromatine losser of strakker te maken. Losser verpakken maakt genen doorgaans gemakkelijker afleesbaar; strakkere verpakking werkt vaak onderdrukkend. Twee groepen enzymen beheren dit evenwicht: histon-acetyltransferases voegen acetylgroepen toe, terwijl histon-deacetylases (HDACs) ze verwijderen. Als dit evenwicht verstoord raakt, kan dat bijdragen aan een breed scala aan ziekten, waaronder kanker, hartproblemen, spierafbraak en immuunstoornissen.
Waarom HDAC5 een veelbelovende maar lastige geneesmiddeldoelwit is
HDACs vormen een grote familie van verwante enzymen die in verschillende klassen zijn verdeeld. Veel van de medicijnen die nu klinisch gebruikt worden, blokkeren meerdere HDAC-typen tegelijk, wat belangrijke normale functies kan uitschakelen en sterke bijwerkingen kan veroorzaken. Klasse IIa HDACs, waaronder HDAC5, vallen op omdat ze verrijkt zijn in specifieke weefsels zoals de hersenen, het hart en skeletspier, en omdat ze met andere eiwitten samenwerken om sleutelgenenetwerken te reguleren. HDAC5 fungeert vaak als een brug, door een zeer actieve partnerenzym (HDAC3) naar bepaalde genen te brengen zodat chromatine kan worden aangespannen en die genen worden onderdrukt. Vanwege deze gerichte rollen wordt HDAC5 gezien als een aantrekkelijk doelwit voor selectievere medicijnen, maar er is een gebrek aan gedetailleerde biochemische gegevens en er ontbreekt een hogeresolutiestructuur van zijn actieve kern, wat rationeel geneesmiddelontwerp bemoeilijkt.
HDAC5 herbouwen in een reageerbuis
Om deze lacune aan te pakken, produceerden de onderzoekers alleen de katalytische kern van humane HDAC5 – het deel dat de chemische reactie uitvoert – in bacteriën, zuiverden het en bevestigden dat het een stabiel, enkelvoudig eiwit vormt in oplossing. Ze testten vervolgens hoe goed het werkt onder verschillende zoutconcentraties en zuurtegraad. De activiteit van HDAC5 bleef robuust over een breed bereik aan zoutwaarden en was maximaal bij licht basische condities, vergelijkbaar met die in veel cellen. Met speciale fluorescerende testmoleculen ontdekten ze dat de natuurlijke vorm van HDAC5 slechts één bepaald type substraat herkent dat vaak wordt gebruikt om klasse IIa-enzymen te onderzoeken. Geleid door eerder werk aan verwante HDACs, vervingen ze een enkel aminozuur (histidine) door tyrosine op een kritieke plek. Remarkabel genoeg maakte deze kleine wijziging het gemuteerde HDAC5 mogelijk om beide typen testsubstraten efficiënt te verwerken, wat laat zien hoe één residu in het actieve centrum de chemische voorkeuren van het enzym stuurt.
Testen en vergelijken van twee nieuwe kandidaatgewassen
Het team onderzocht vervolgens twee experimentele HDAC5-blokkerende moleculen, bekend als NT160 en FFK24. Deze verbindingen gebruiken een nieuwer zink-bindend groepje dat enkele van de toxiciteit en het slechte selectiviteitsprofiel van oudere, hydroxamaatgebaseerde medicijnen vermijdt. Door te meten hoe elke remmer HDAC5 vertraagde in nauwkeurig gecontroleerde reacties, bepaalden de auteurs zeer lage remmingsconstanten in het nanomolaire bereik, wat betekent dat beide verbindingen sterk aan het enzym binden. NT160 bond consequent ongeveer tien keer sterker dan FFK24. Om te begrijpen waarom gebruikten de onderzoekers computerdocking met een AlphaFold-voorspelde structuur van HDAC5’s kern. Beide remmers deelden een gemeenschappelijk kopgedeelte dat diep in het actieve pocket nestelde en contact maakte met het metaalion, maar de staart van NT160 vormde extra stabiliserende contacten met specifieke aminozuren in het pocket. Deze aanvullende interacties verklaren waarschijnlijk zijn grotere potentie.
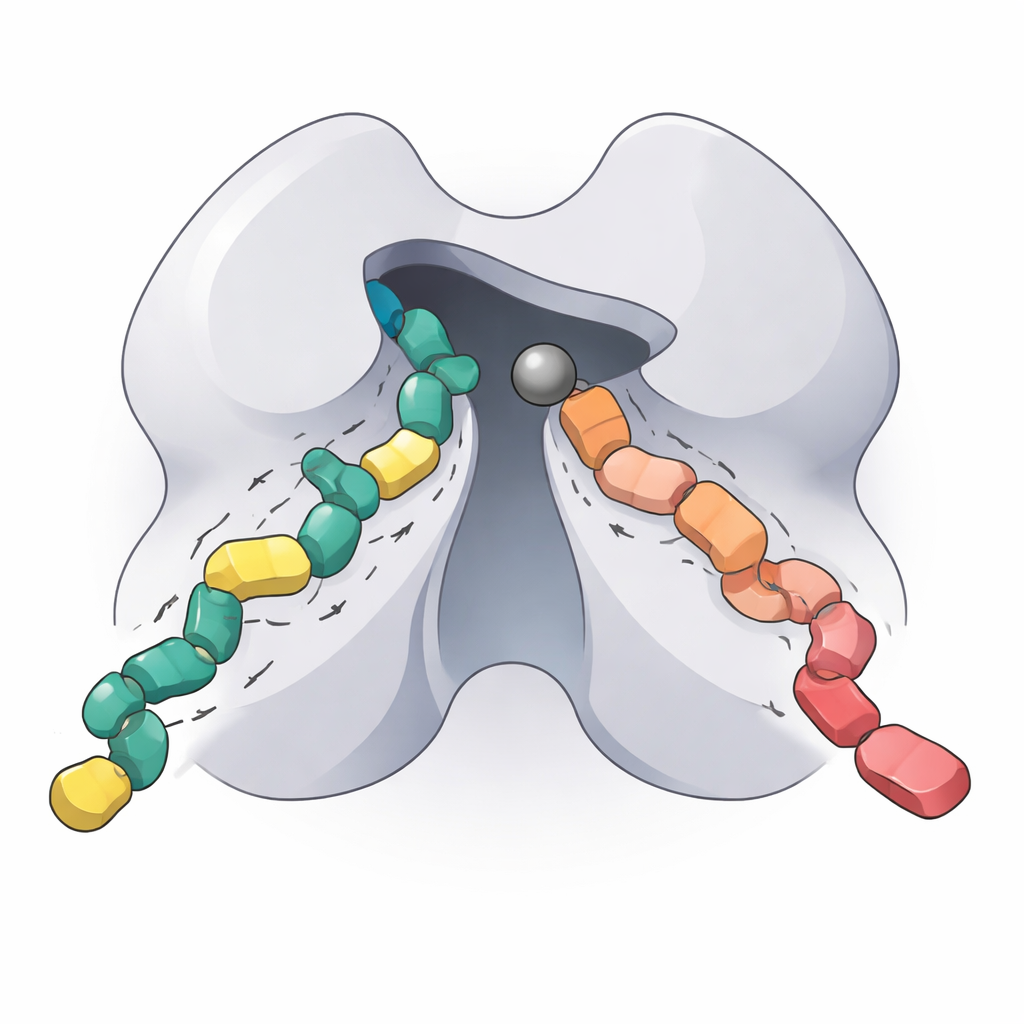
Wat dit betekent voor toekomstige gerichte therapieën
Door de werkende kern van HDAC5 te reconstrueren, zijn optimale werkcondities in kaart te brengen, te ontleden hoe een enkele aminozuurverandering het gedrag verandert en te kwantificeren hoe twee next-generation remmers binden, levert deze studie een gedetailleerd biochemisch "vingerafdruk" van een belangrijk maar eerder ondergekarakteriseerd enzym. Voor niet-specialisten is de kernboodschap dat HDAC5 helpt bepalen of bepaalde genen aan- of uitgezet zijn, en dat het nauwkeurig afstemmen van deze schakelaar nuttig kan zijn bij de behandeling van hartziekten, neurodegeneratie, kanker en immuunstoornissen. De nieuwe inzichten en tools die hier worden gepresenteerd, zouden onderzoekers moeten helpen HDAC5- en klasse IIa-selectieve geneesmiddelen te ontwerpen die daar werken waar ze nodig zijn, terwijl ongewenste effecten elders in het lichaam worden geminimaliseerd.
Bronvermelding: Mammen, C., Hornung, F.M., Anzenhofer, C. et al. In vitro characterization of the catalytic domain of human histone deacetylase 5. Sci Rep 16, 7935 (2026). https://doi.org/10.1038/s41598-026-37633-5
Trefwoorden: histon-deacetylase 5, epigenetische regulatie, HDAC-remmers, gerichte kankertherapie, chromatine-structuur