Clear Sky Science · nl
Geoptimaliseerde gradient van gevriesdroogd plaatjesrijk plasma in biomimetische 3D-geprinte triphasische scaffold op basis van alginaat en gelatine voor osteochondrale weefselengineering
Waarom het herbouwen van gewrichtsoppervlakken ertoe doet
Wanneer de gladde oppervlakken in onze knieën of andere gewrichten beschadigd raken, kunnen dagelijkse bewegingen zoals lopen, trappen oplopen of zelfs opstaan pijnlijk worden. Deze oppervlakken bestaan uit een complex "osteochondraal" geheel: een glijdend kraakbeenlaagje bovenop, een dunne verhardingszone in het midden en ondersteunend bot eronder. Huidige chirurgische reparaties falen vaak omdat ze deze driedelige structuur niet volledig herstellen. Dit artikel verkent een nieuw, 3D-geprint meerlagig scaffold dat bedoeld is om natuurlijke gewrichtsweefsels beter na te bootsen en de eigen stamcellen van het lichaam te begeleiden bij het opnieuw laten groeien van gezond kraakbeen.
Het bouwen van een gelaagde ondersteuning voor beschadigde gewrichten
Om de echte gewrichtsanatomie na te bootsen, ontwierpen de onderzoekers een "triphasisch" scaffold met drie gestapelde lagen: een bovenste kraakbeenachtige laag, een middelste gekalkte laag en een onderste botachtige laag. Ze gebruikten een mengsel van twee natuurlijke polymeren, alginaat en gelatine, als basisinkt voor 3D-printen. Om de botzijde van het scaffold te versterken voegden ze kleine velletjes graphene oxide toe, een koolstofgebaseerd nanomateriaal dat bekendstaat om zijn mechanische sterkte en gunstige interactie met cellen. Om de kraakbeenzijde biologisch actiever te maken, mengden ze gevriesdroogd plaatjesrijk plasma (PRP) — een geconcentreerde bron van groeifactoren die onze bloedplaatjes tijdens genezing afgeven. Door de hoeveelheid PRP geleidelijk van onder naar boven te veranderen, creëerden ze een zachte biologische gradient die beter weergeeft hoe signalen variëren doorheen echt gewrichtsweefsel. 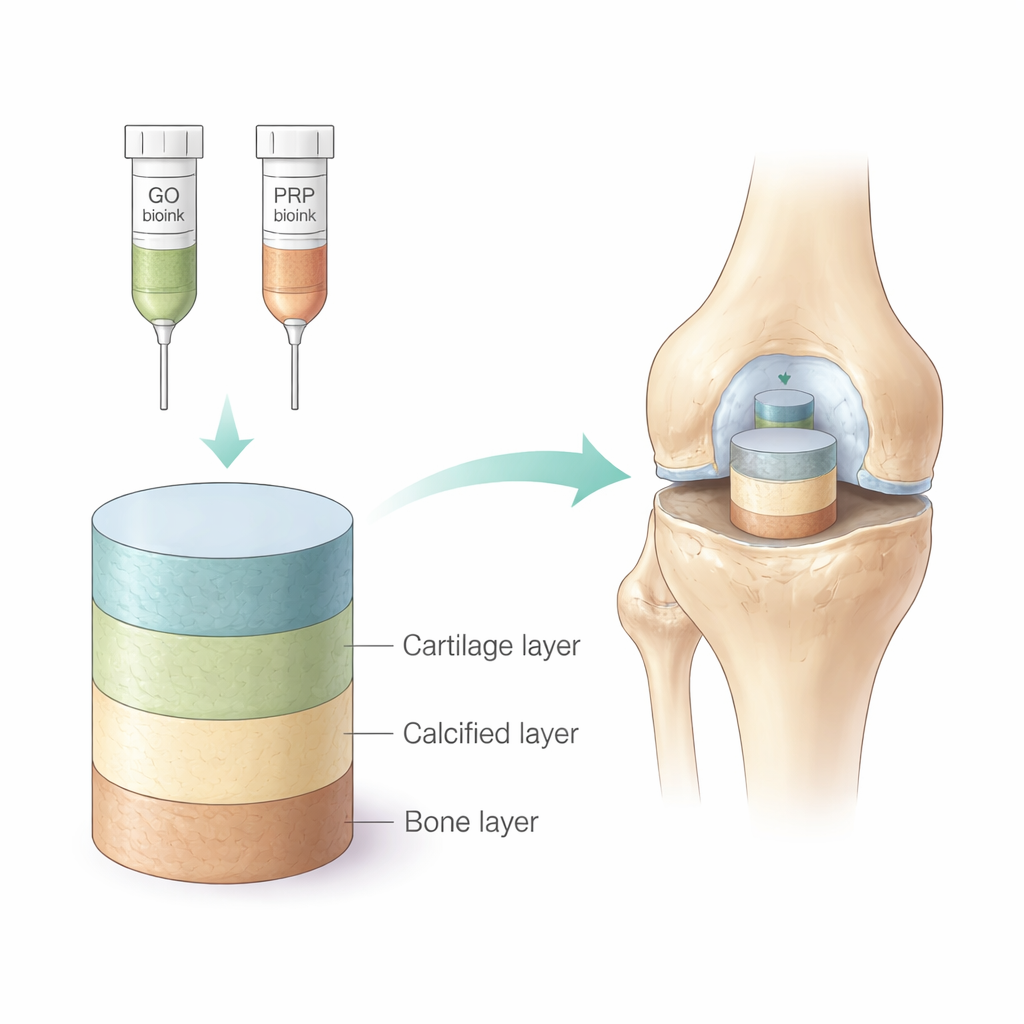
Het vinden van de juiste balans tussen sterkte en stabiliteit
Een grote uitdaging bij het printen van levende weefselondersteuning is ze sterk genoeg maken om krachten in het lichaam te weerstaan, terwijl ze toch zacht en vochtig blijven zoals natuurlijk kraakbeen. Het team optimaliseerde eerst het graphene oxide-gehalte in de botlaag. Ze toonden aan dat het toevoegen van een kleine hoeveelheid (1% naar gewicht) de druksterkte aanzienlijk verhoogde en hielp de geprinte draden hun vorm te behouden, terwijl het materiaal nog steeds kon zwellen met water en permeabel bleef voor voedingsstoffen. Hogere graphene-niveaus hielpen niet verder en begonnen zelfs de stabiliteit te verminderen. Vervolgens testten ze verschillende hoeveelheden PRP in het kraakbeengebied. Scaffolds met 1% of 2% PRP waren gemakkelijker netjes te printen en degradeerden in een gecontroleerd tempo over ongeveer een maand — lang genoeg om nieuwe weefselvorming te ondersteunen, maar niet zo lang dat het materiaal bleef hangen nadat het zijn taak had voltooid.
Hoe stamcellen reageren in het scaffold
Om te onderzoeken of dit gelaagde ontwerp echt kraakbeenherstel bevordert, zaaiden de onderzoekers stamcellen uit rattenmerg in de geprinte scaffolds en kweekten ze onder omstandigheden die kraakbeenvorming stimuleren. Ze maten hoe goed de cellen overleefden, zich verspreidden en kraakbeen-gerelateerde genen activeerden. Alle scaffolds ondersteunden gezonde cellen, maar die met PRP bevorderden duidelijk celgroei vergeleken met PRP-vrije versies. In het bijzonder toonde het scaffold met 2% PRP de sterkste signalen van kraakbeenopbouwende activiteit: stamcellen produceerden meer van de kenmerkende kraakbeengenen SOX9 en collageen type II, terwijl collageen type I, dat geassocieerd is met minder gewenste vezelachtige reparatie, verminderd was. Kleuringstests toonden ook grotere hoeveelheden glycosaminoglycanen — de suikerrijke moleculen die kraakbeen zijn schokabsorberende eigenschappen geven — in de 2% PRP-groep.
Langzame, gestage afgifte van het lichaamseigen herstelsignaal
Het gevriesdroogde PRP-poeder in het scaffold fungeerde als een ingebouwd reservoir van herstellende signalen. Tests van het materiaal alleen en binnen de 3D-structuur toonden aan dat belangrijke groeifactoren zoals PDGF en TGF-β op een gecontroleerde manier werden vrijgegeven over ongeveer drie weken. Deze langzame afgifte is belangrijk: in plaats van een korte piek die snel vervaagt, kan een langdurig signaal stamcellen op een kraakbeenvormend pad houden en hen helpen een rijkere, duurzamere matrix op te bouwen. Tegelijkertijd maakte de geprinte architectuur — een open, onderling verbonden raster van poriën — het mogelijk dat voedingsstoffen door het scaffold diffundeerden en gaf het cellen ruimte om zich te hechten, uit te spreiden en met elkaar te interageren, vergelijkbaar met hun gedrag in inheems weefsel. 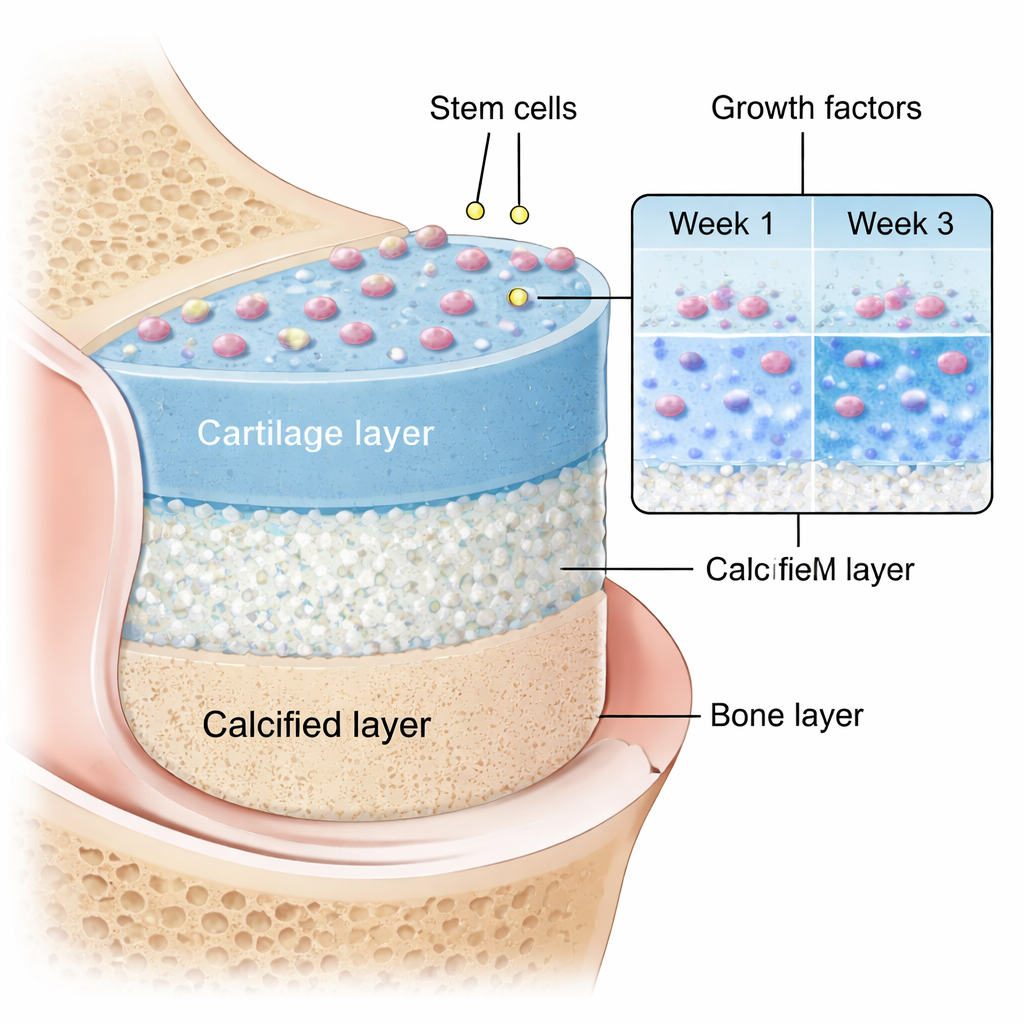
Wat dit kan betekenen voor toekomstige gewrichtsreparatie
Kort gezegd laat deze studie zien dat een zorgvuldig afgestemd, 3D-geprint drielaags scaffold zowel mechanische ondersteuning kan bieden aan een beschadigd gewrichtsoppervlak als biologisch kan sturen zodat stamcellen kraakbeen herbouwen in plaats van littekenachtig weefsel. Een mengsel met alginaat, gelatine, 1% graphene oxide aan de botzijde en 2% PRP aan de kraakbeenzijde bleek het veelbelovendste recept. Hoewel deze resultaten afkomstig zijn van laboratoriumonderzoek met ratcellen en nog niet van proeven in levende dieren of mensen, wijzen ze op een weg naar meer natuurlijke, langdurige reparaties van versleten of beschadigde gewrichten door slimme materialen, bloedafgeleide groeifactoren en precieze 3D-printtechnieken te combineren.
Bronvermelding: Ghobadi, F., Mohammadi, M., Kalantarzadeh, R. et al. Optimized gradient of lyophilized platelet-rich plasma in biomimetic 3D-printed triphasic scaffold based on alginate and gelatin for osteochondral tissue engineering. Sci Rep 16, 6332 (2026). https://doi.org/10.1038/s41598-026-37615-7
Trefwoorden: 3D-geprint scaffold, osteochondrale reparatie, plaatjesrijk plasma, graphene oxide, kraakbeenregeneratie