Clear Sky Science · nl
Ubiquitinering van SMAD2 via PY-motief reguleert skeletspiermassa en fibrotische degeneratie
Waarom deze spieronderzoek belangrijk is
Naarmate we ouder worden, merken velen van ons dat spieren zwakker en kleiner worden, en bij chronische ziekte of letsel kunnen spieren geleidelijk worden vervangen door stug littekenweefsel. Deze studie pakt een fundamentele vraag achter die veranderingen aan: hoe voorkomen spiercellen dat een krachtig groeiregulerend signaal, TGF‑beta genoemd, te ver doorschiet en spierverlies en fibrose (littekenvorming) veroorzaakt? Door een klein ingebouwd "uit‑knopje" in een belangrijk TGF‑beta-eiwit te onthullen, laten de auteurs een nieuw mechanisme zien dat helpt spiermassa en gezonde weefselstructuur te behouden.
Een ingebouwde rem op een krachtig signaal
TGF‑beta is een signaalmolecuul dat cellen vertelt wanneer ze de groei moeten vertragen, van identiteit moeten veranderen of bindweefsel moeten produceren. In skeletspier krimpt teveel TGF‑beta spiervezels en bevordert het fibrose; te weinig kan de normale groeiregulatie verstoren. Binnen cellen werkt TGF‑beta vooral via een relais-eiwit genaamd SMAD2. Nadat TGF‑beta aan zijn receptoren op het celoppervlak bindt, wordt SMAD2 geactiveerd en verhuist naar de kern om de genactiviteit te veranderen. Om te voorkomen dat dit permanent wordt, taggen cellen SMAD2 chemisch met kleine ubiquitinemoleculen, waarmee het voor verwijdering wordt bestemd. Een korte sequentie in SMAD2, bekend als het PY‑motief, is de aanhechtingsplaats voor enzymen die deze ubiquitinetags vastzetten. De onderzoekers vroegen: als deze aanhechtingsplaats in een levend dier wordt verwijderd, faalt dan de SMAD2‑rem, en wat gebeurt er na verloop van tijd met de spieren?
Muizen met een ontbrekende veiligheidstag maken
Met moderne genoom‑bewerkingsinstrumenten creëerde het team muizen waarin slechts 15 DNA‑"letters" uit het Smad2‑gen werden verwijderd, waardoor het PY‑motief precies werd weggelaten zonder de rest van het eiwit te verstoren. Deze Smad2dPY‑muizen werden normaal geboren, groeiden op tot volwassenen en waren vruchtbaar, wat aangeeft dat dit fijnafgestelde systeem niet essentieel is voor de basale ontwikkeling onder standaard laboratoriumomstandigheden. Wanneer de wetenschappers hun spieren echter nader onderzochten, ontstond een ander beeld. Jonge volwassen muizen vertoonden slechts subtiele veranderingen, maar rond 12 maanden — ongeveer middelbare leeftijd voor een muis — wogen de grote achterbeenspieren minder en waren individuele vezels kleiner vergeleken met normale nestgenoten. In deze spieren waren de SMAD2‑eiwitniveaus hoger, terwijl de ubiquitinering afnam, wat bevestigt dat het ontbrekende PY‑motief SMAD2 stabieler en minder afbreekbaar maakte.
Overgevoelige spiercellen en stilgevallen herstel
Om te begrijpen wat dit op cellulair niveau betekende, isoleerden de onderzoekers spiervoorlopercellen (myoblasten) uit de mutantmuizen. Wanneer deze myoblasten in een petrischaaltje aan TGF‑beta werden blootgesteld, toonden ze sterkere activatie van SMAD2 en grotere inductie van TGF‑beta‑responsieve genen dan cellen van normale muizen. Tegelijkertijd was hun vermogen om samen te smelten tot lange, meerkernige spiervezels — een belangrijke stap in spiergroei en regeneratie — verminderd. Vergelijkbare veranderingen werden gezien in fibroblasten, de bindweefselcellen die tussen spiervezels liggen: mutantfibroblasten reageerden sterker op TGF‑beta en brachten makkelijker genen tot expressie die gekoppeld zijn aan littekenvormende myofibroblasten. Samen suggereren deze bevindingen dat zonder het PY‑motief zowel spiervormende cellen als ondersteunende cellen overgevoelig voor TGF‑beta worden, waardoor de balans doorslaat naar kleinere vezels en meer vezelig weefsel.
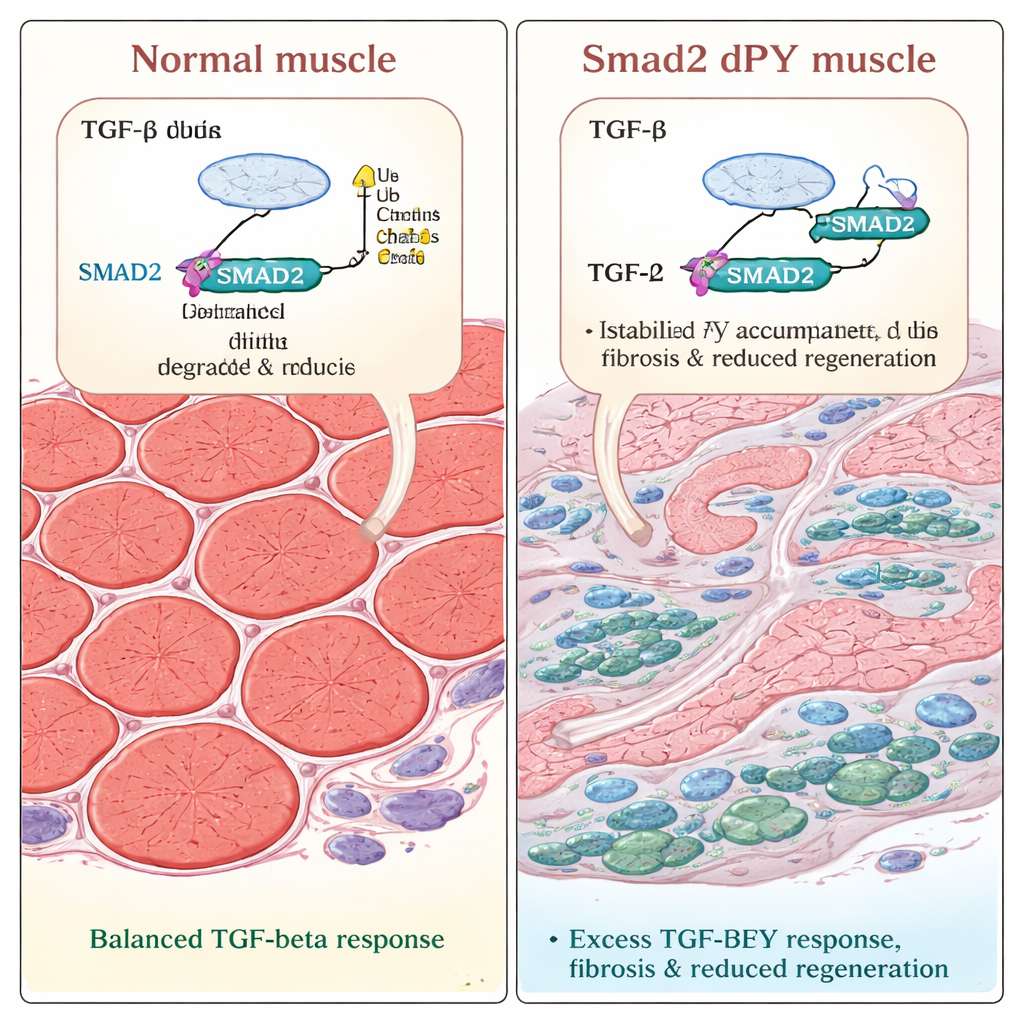
Als letsel toeslaat, wint littekenvorming
Het team testte vervolgens hoe deze gewijzigde spieren met schade omgaan. Ze injecteerden een toxine in de beenspieren om letsel en herstel uit te lokken, een goed vastgesteld model voor regeneratie. Zowel bij normale als mutantmuizen braken beschadigde vezels aanvankelijk af en begonnen daarna weer te groeien. Maar drie weken na het letsel waren de geregenereerde vezels in de Smad2dPY‑muizen opvallend dunner. Microscopie toonde grotere gebieden gevuld met collageen, het belangrijkste bestanddeel van littekenweefsel, en een toegenomen aantal alfa‑gladde‑spier‑actine‑positieve myofibroblasten, cellen die bekendstaan om het aandrijven van fibrose. Deze resultaten laten zien dat wanneer SMAD2 niet goed getagd en afgebroken kan worden, het herstelproces verstoord raakt: in plaats van volledig sterke spiermassa te herbouwen, geneest het weefsel met overtollig littekenweefsel en verminderde contractiele massa.
Wat dit betekent voor spiergezondheid
Voor niet‑specialisten is de belangrijkste boodschap dat een heel kleine moleculaire eigenschap — het PY‑motief op SMAD2 — fungeert als een stille maar belangrijke waarborg in skeletspier. Het stelt cellen in staat het TGF‑beta‑signaal terug te schroeven door de verwijdering van SMAD2 te bevorderen, waardoor de normale spiergrootte wordt behouden en fibrose wordt beperkt, vooral wanneer TGF‑beta‑niveaus van nature stijgen met leeftijd of chronisch letsel. Wanneer deze waarborg bij muizen wordt uitgeschakeld, worden spieren geleidelijk kleiner en vatbaarder voor littekenvorming, en herstellen ze niet volledig na schade. Hoewel dit werk nog in dieren is gedaan, benadrukt het ubiquitinering van SMAD2 als een potentieel doelwitpad voor toekomstige strategieën bedoeld om spiermassa te behouden en fibrotische degeneratie bij veroudering of ziekte te voorkomen.
Bronvermelding: Yamasaki, Y., Sakamoto, K., Yashiro, S. et al. SMAD2 ubiquitination through PY motif regulates skeletal muscle mass and fibrotic degeneration. Sci Rep 16, 6666 (2026). https://doi.org/10.1038/s41598-026-37582-z
Trefwoorden: skeletspier, TGF-beta-signaal, SMAD2, ubiquitinering, fibrose