Clear Sky Science · nl
Veranderingen in EGFR-activiteit na CRISPR/Cas9-bewerking van het EGF-bindingsdomein
Waarom het herschakelen van een kankersignaal ertoe doet
Baarmoederhalskanker hangt vaak af van een krachtige groeischakelaar genaamd het epidermale groeifactorreceptor (EGFR). Veel tumoren hebben enorme aantallen van deze receptoren, maar medicijnen die erop gericht zijn ze uit te schakelen hebben slechts een deel van de patiënten geholpen. Deze studie stelde een fundamentele vraag met grote behandelimplicaties: wat gebeurt er als je het vermogen van EGFR om zijn favoriete groeisignaal, epidermale groeifactor (EGF), te grijpen verwijdert, zonder de receptor zelf te verwijderen?
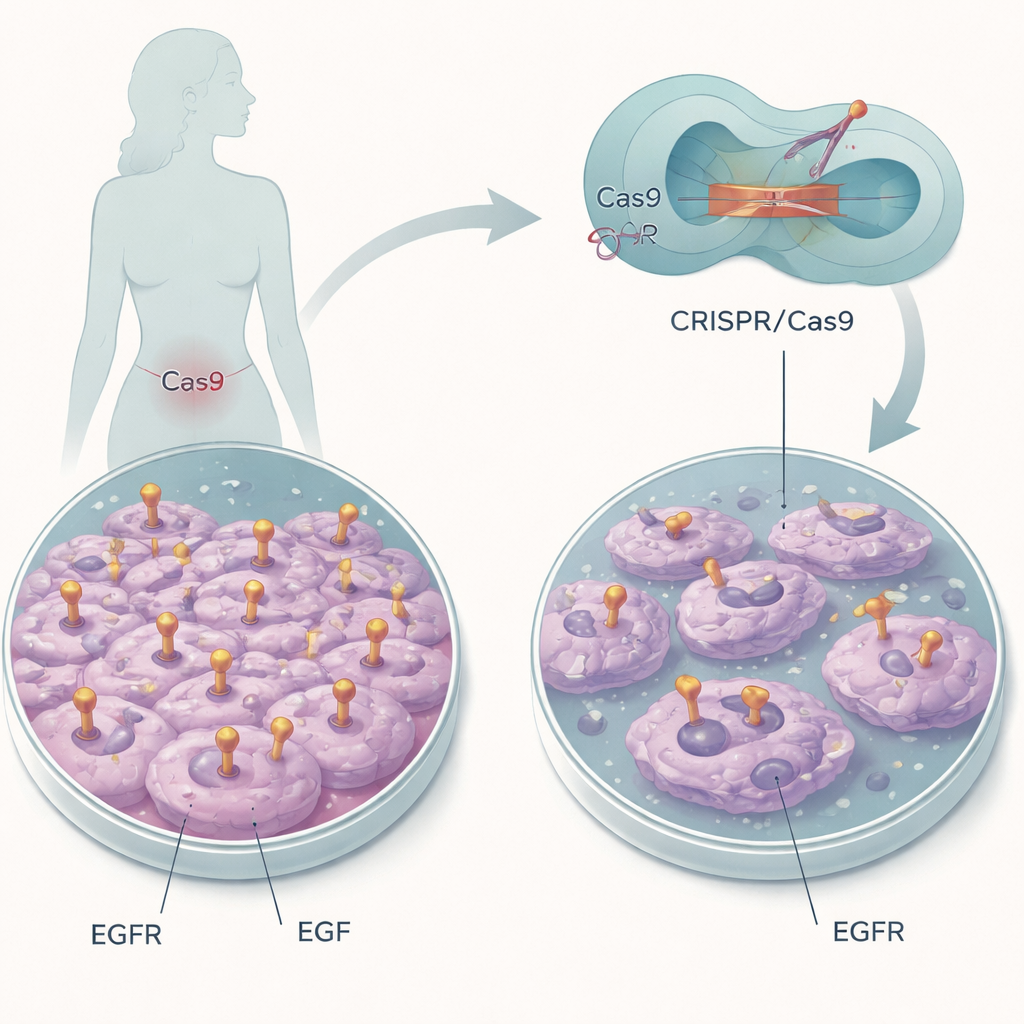
Een moleculaire "aan-schakelaar" uitschakelen
De onderzoekers richtten zich op een baarmoederhalskankercellijn die grote hoeveelheden anders normale EGFR draagt. In plaats van het gen te vernietigen gebruikten ze CRISPR/Cas9-genoomediting als een moleculaire scalpel om slechts een paar aminozuren in EGFR’s EGF-bindingspoort te veranderen. Twee specifieke posities, genoemd L14 en Y45, helpen EGF zich aan de receptor te hechten. Door deze bouwstenen te vervangen door andere, wilde het team EGFR aanwezig houden maar blind voor EGF maken, zodat ze de rol van deze ene interactie in het gedrag van kankercellen konden isoleren.
Ontwerpen van aangepaste kankercellijnen
In een eerste stap testte het team deze mutaties in cellen met behulp van plasmiden die tijdelijk normale of gewijzigde EGFR produceren. Fluorescent gelabeld EGF toonde aan dat alle gemuteerde vormen veel minder ligand binden dan de normale receptor, vooral wanneer zowel L14 als Y45 samen werden veranderd. Vervolgens introduceerden de onderzoekers deze veranderingen rechtstreeks in het kankercelgenoom met CRISPR/Cas9 en genereerden ze verschillende nieuwe celnklonen. Sommige droegen een enkele mutatie, andere droegen de dubbele mutatie op één EGFR-kopie en inactiverende veranderingen op de andere. Computermodellering van de resulterende eiwitvormen liet zien dat deze aanpassingen de bindingsplaats voldoende vervormden om EGF-hechting te verzwakken of te aboleren, in overeenstemming met de bindingsproeven.
Wanneer de receptor beweegt maar de cellen overleven
Gedetailleerde beeldvorming toonde aan dat de bewerkte receptoren zich heel anders binnen de cel gedroegen. In niet-bewerkte kankercellen zit EGFR aan het celoppervlak, vangt EGF en verplaatst zich daarna naar binnen terwijl het chemisch geactiveerd wordt via fosforylering. In klonen met de dubbele mutatie verdween EGF-binding nagenoeg en werd EGFR niet langer op het membraan waargenomen; in plaats daarvan stapelde de kleine hoeveelheid resterende receptor zich op in het celinterieur. Zelfs een enkele Y45-verandering verminderde de binding aanzienlijk en verlaagde de totale EGFR-niveaus. Toch bleven de kankercellen ondanks deze verstoring van de standaard EGF–EGFR-signaleringsroute levensvatbaar en doorgroeien in cultuur, met slechts bescheiden veranderingen in hun celfasepatronen.
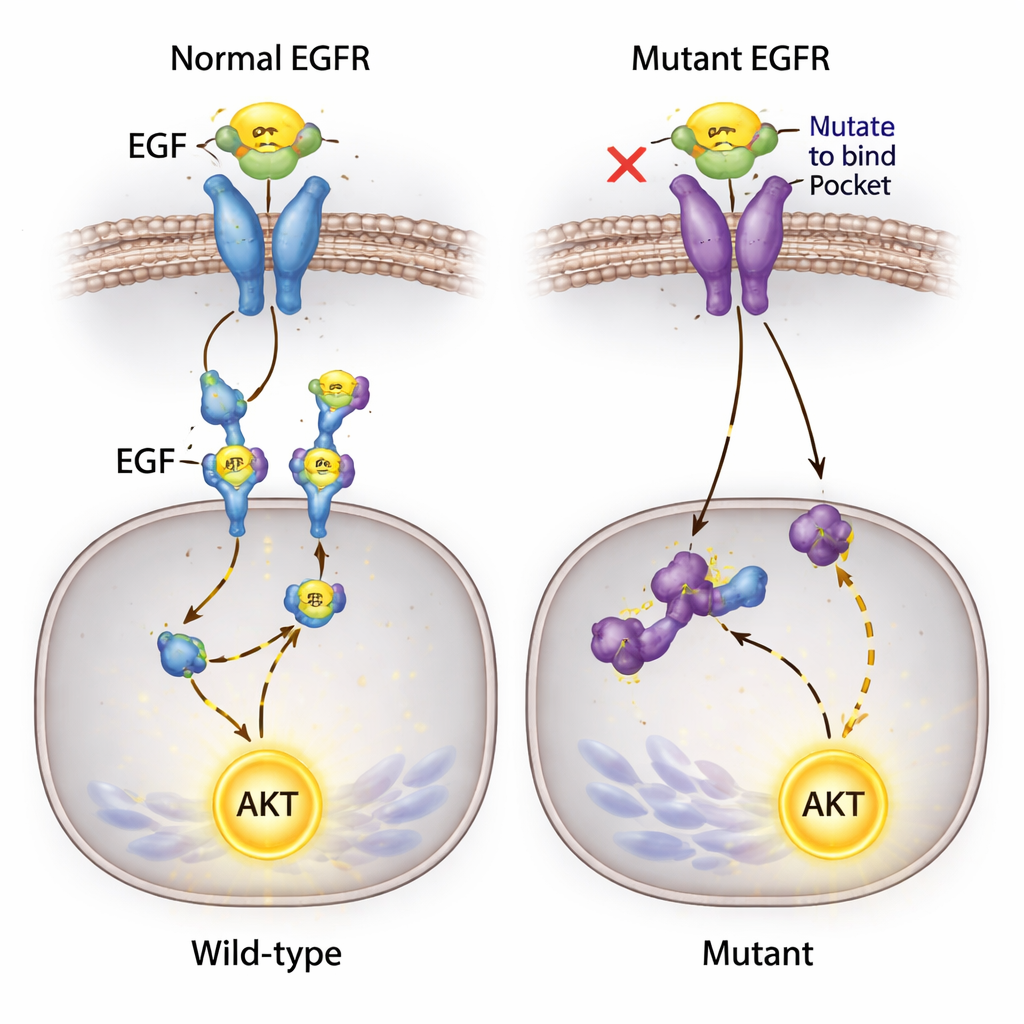
Een onverwacht signaal dat niet stopt
Een van de meest verrassende bevindingen betrof AKT, een sleutelproteïne dat celsurvival bevordert en gewoonlijk stroomafwaarts van EGFR geactiveerd wordt. De onderzoekers verwachtten dat het blokkeren van EGF–EGFR-binding dit pad zou dempen. In plaats daarvan activeerde AKT zich sterk in alle cellijnen toen ze EGF aan het medium toevoegden — ook in die waar EGF niet langer aan EGFR kon binden en waar receptorfosforylering ondetecteerbaar was. Omdat deze cellen een bekende mutatie in een ander signaalgen, PIK3CA, dragen, vermoedt het team dat alternatieve routes EGF kunnen doorgeven aan AKT-activatie, mogelijk via andere oppervlakte-eiwitten of achtergrondmutaties, en zo de bewerkte EGFR omzeilen.
Verborgen genetische veranderingen en toekomstige therapieën
Om zeker te weten dat CRISPR geen wijdverspreide ongewenste bewerkingen veroorzaakte, sequentieerden de wetenschappers het volledige genoom van de nieuwe celnklonen. Ze bevestigden dat de gewenste EGFR-mutaties aanwezig waren en vonden geen bewijs van snijplaatsen op voorspelde off-targetlocaties voor de CRISPR-guides. Ze ontdekten echter wel veel spontane mutaties verspreid over het genoom, waarvan sommige het gedrag van de cellen kunnen beïnvloeden. Dit onderstreept dat zelfs wanneer CRISPR zijn beoogde adres raakt, het van nature instabiele DNA van kankercellen kan compliceren hoe we experimentele resultaten interpreteren en hoe we precieze gen-gebaseerde therapieën ontwerpen.
Wat dit voor patiënten betekent
Voor niet-specialisten is de belangrijkste boodschap dat het eenvoudigweg blokkeren van de handshake tussen EGF en EGFR — zelfs heel precies op atomair niveau — niet automatisch voorkomt dat kankercellen "groei en overlevings"-commando’s ontvangen. De studie laat zien dat kankercellen sleutelroutes zoals AKT-activatie kunnen omleiden rond een geblokkeerde receptor, en dat CRISPR-bewerking zelf zorgvuldig beoordeeld moet worden in zulke instabiele genomen. Deze ontworpen cellijnen bieden nu een krachtig laboratoriummodel om naar back-uproutes te zoeken die EGFR-afhankelijke tumoren in stand houden, informatie die uiteindelijk kan leiden tot combinatietherapieën die zowel EGFR als zijn verborgen medeplichtigen richten.
Bronvermelding: Popović, J., Hahut, A., Torres, G.E. et al. Changes in EGFR activity following CRISPR/Cas9-editing of the EGF binding domain. Sci Rep 16, 6797 (2026). https://doi.org/10.1038/s41598-026-37579-8
Trefwoorden: EGFR, baarmoederhalskanker, CRISPR, EGF-signaleringspad, AKT-pad