Clear Sky Science · nl
DNA-conjugatie op gefunctionaliseerde kunststofoppervlakken voor opeenvolgende, iteratieve enkelmolecuul-sequencing
De data van morgen opslaan in piepkleine strengen
Stel je voor dat je je foto’s, boeken of wetenschappelijke dossiers kunt back-uppen in een vorm die eeuwen kan meegaan en past in een deeltje kleiner dan een zandkorrel. DNA—dezelfde molecule die onze genen draagt—is in opkomst als een krachtige kandidaat voor ultra-dichte, duurzame gegevensopslag. Dit artikel verkent een nieuwe manier om DNA-gegevens veilig te ‘parkeren’ aan de binnenkant van gewone plastic buisjes, en ze vervolgens herhaaldelijk uit te lezen zonder de oorspronkelijke moleculen te vernietigen.
Een nieuw soort data-‘thumb drive’
Huidige harde schijven en flashgeheugen slijten en bevatten per gram veel minder informatie dan DNA potentieel kan. Onderzoekers hebben al laten zien hoe digitale bestanden kunnen worden vertaald naar reeksen DNA-‘letters’. Maar telkens wanneer die DNA-strengen worden gekopieerd of gesequenced, raakt een deel van het oorspronkelijke materiaal verbruikt—alsof inkt vervaagt als je een pagina te vaak photocopiert. In deze studie transformeerden de auteurs het eenvoudige plastic PCR-buisje—al standaard in biologielaboratoria—tot een herbruikbaar fysiek opslagmedium. Ze hechtten chemisch DNA-strengen met gecodeerde data aan het binnenoppervlak van het buisje, zodat het DNA op zijn plaats blijft terwijl kopieën herhaaldelijk worden gemaakt en uitgelezen. 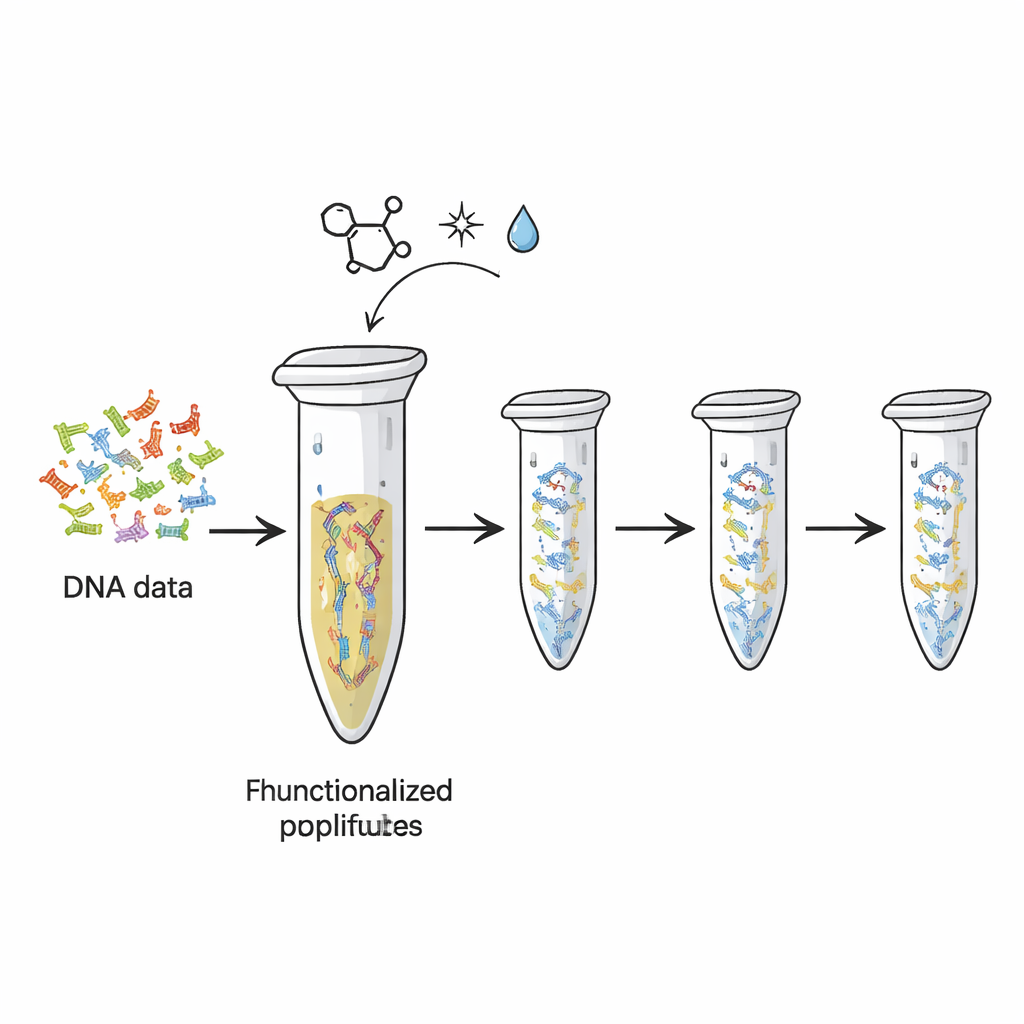
DNA op kunststof klikken
Het team maakte gebruik van een type zeer specifieke ‘click-chemie’—reacties die gewaardeerd worden omdat ze snel, betrouwbaar en mild zijn. Eerst voegden ze speciale chemische staarten toe aan de uiteinden van DNA-strengen die verschillende data-‘bestanden’ vertegenwoordigen. Deze staarten, gebaseerd op een molecuul genaamd TCO, zijn ontworpen om zich te vergrendelen aan overeenkomende groepen (MTz) die op het kunststofoppervlak van het buisje zijn aangebracht. Wanneer de twee elkaar tegenkomen, vormen ze een stabiele covalente binding en lijmen ze het DNA effectief aan het kunststof. Tests met een controle-DNA-fragment toonden aan dat na incubatie vrijwel al het DNA uit de oplossing verdwenen was, wat aangeeft dat het nu op de buiswand was geïmmobiliseerd. Het platform kon van de orde van honderden femtomol DNA vasthouden, wat duidt op voldoende capaciteit voor praktische datasets.
Digitale ‘bestanden’ op aanvraag ophalen
Om te onderzoeken of dit oppervlakgebonden DNA zich nog steeds als een bruikbaar archief gedroeg, codeerden de onderzoekers tekst en andere data in een pool van ongeveer 15.000 korte DNA-strengen, gegroepeerd in 18 ‘bestandsgroepen’. Elke groep kon selectief worden gekopieerd met zijn eigen paar primers—korte startssequenties die de kopieermachine naar de juiste doelen leiden. Het team voerde herhaaldelijk standaard PCR-reacties uit in hetzelfde buisje, waarbij ze elke keer een andere bestandsgroep kozen om te amplificeren. Na elke run haalden ze het gekopieerde DNA weg, reinigden het buisje met enzymen die achtergebleven producten in oplossing afbreken, en gingen door naar het volgende bestand. Nanopore-sequencing van het gekopieerde materiaal toonde aan dat de meeste bestandsgroepen met hoge nauwkeurigheid werden opgehaald, en dat kruisbesmetting van eerdere runs extreem laag bleef, doorgaans rond 1 procent of minder.
Een zachtere manier van uitlezen vinden
Er was echter een kanttekening: toen ze PCR herhaaldelijk in hetzelfde buisje uitvoerden tot wel 18 keer, nam de hoeveelheid opgehaald DNA gestaag af. PCR berust op snel verwarmen en afkoelen, en de auteurs concludeerden dat de herhaalde hoge temperaturen het geïmmobiliseerde DNA of de verbinding met het kunststof beschadigden, hoewel controletests suggereerden dat het DNA niet simpelweg uit werd gewassen naar de oplossing. Om dit op te lossen schakelden ze over op recombinase-polymerase-amplificatie (RPA), een nieuwere methode die werkt bij één relatief lage temperatuur dicht bij lichaamstemperatuur. Met RPA op vers DNA-gecoate buisjes vroegen ze opnieuw alle 18 bestandsgroepen achtereenvolgens op. Dit keer waren de opbrengsten hoog—rond 60 ng/µL—en lieten ze niet dezelfde dalende trend zien. Het patroon van welke strengen tijdens het kopiëren werden bevoordeeld of benadeeld, kwam ook goed overeen met wat werd gezien wanneer het DNA vrij in oplossing was. 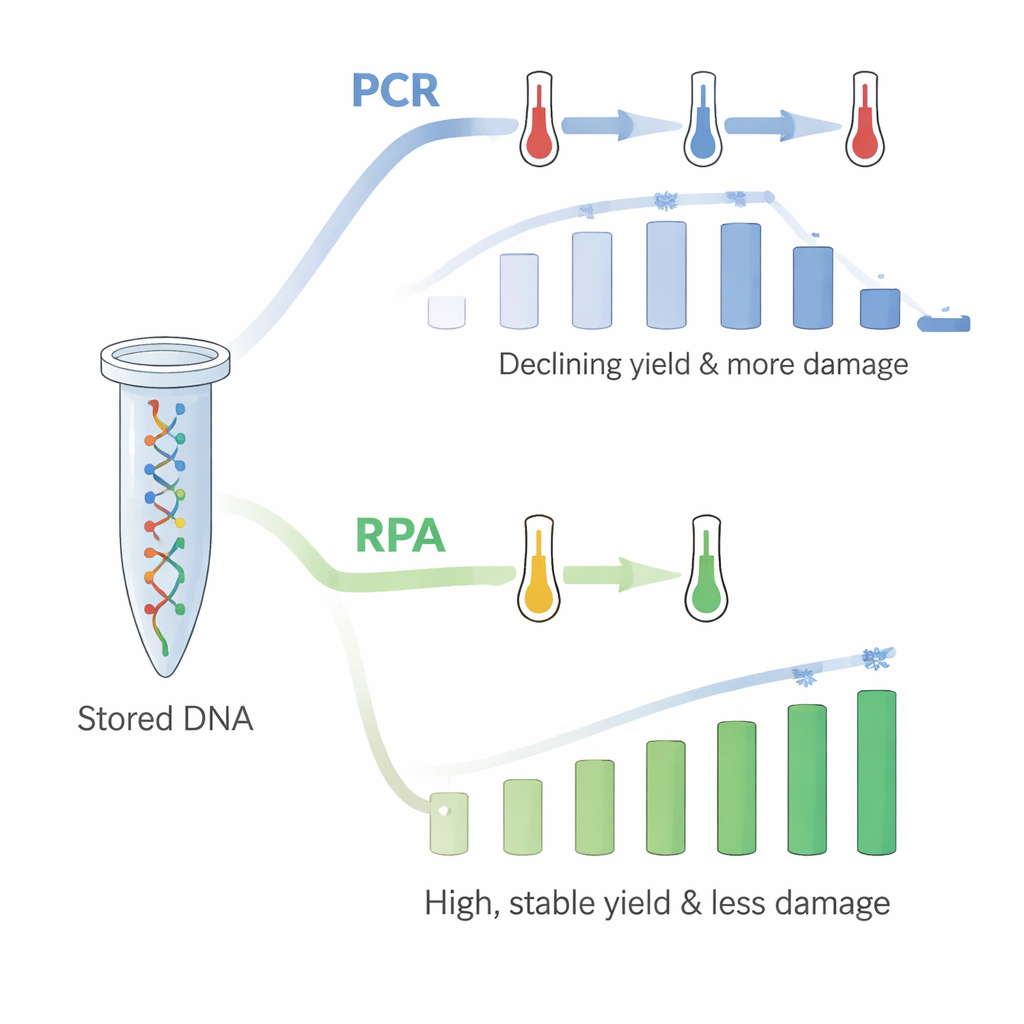
Op weg naar draagbaar, langlevend DNA-geheugen
Door robuuste click-chemie te combineren met laagtemperatuurskopie wijst dit werk op een praktische manier om eenvoudige plastic buisjes te veranderen in herbruikbare DNA-gegevenscartridges. Het DNA blijft fysiek vergrendeld aan het buisje, waar het herhaaldelijk kan worden bevraagd voor specifieke ‘bestanden’ zonder de oorspronkelijke moleculen te verbruiken, vooral bij gebruik van de zachtere RPA-methode. Voor niet-specialisten is de kernboodschap dat DNA niet alleen de code van het leven is—het kan ook fungeren als een compacte, duurzame opslagmedium voor digitale informatie. Methoden zoals deze brengen ons dichter bij een toekomst waarin je langetermijnback-ups niet op draaiende schijven staan, maar in zorgvuldig ontworpen moleculen die rustig op een labplankje liggen.
Bronvermelding: Roy, S., Ji, H.P. & Lau, B.T. DNA conjugation on functionalized plastic surfaces for sequential, iterative single molecule sequencing. Sci Rep 16, 6467 (2026). https://doi.org/10.1038/s41598-026-37575-y
Trefwoorden: DNA-gegevensopslag, click-chemie, conjugatie op kunststofoppervlak, recombinase-polymerase-amplificatie, nanopore-sequencing