Clear Sky Science · nl
Vermeerdering van kopieën stimuleert IFI30-overexpressie en gecoördineerde immuunactivatie, waarmee een nieuw diagnostisch en therapeutisch doelwit bij maagadenocarcinoom wordt geïdentificeerd
Waarom een eiwit in de maag ertoe doet
Maagkanker behoort tot de dodelijkste vormen van kanker, grotendeels omdat het vaak pas laat wordt ontdekt en moeilijk te behandelen kan zijn. Deze studie richt zich op een weinig bekend eiwit genaamd IFI30, gevonden in cellen die het immuunsysteem helpen bedreigingen te herkennen. Door na te gaan hoe IFI30 verandert in maagtumoren en hoe het de afweer van het lichaam beïnvloedt, suggereren de onderzoekers dat het een krachtig hulpmiddel kan worden voor vroegere diagnose en voor het kiezen van effectievere, gepersonaliseerde behandelingen.
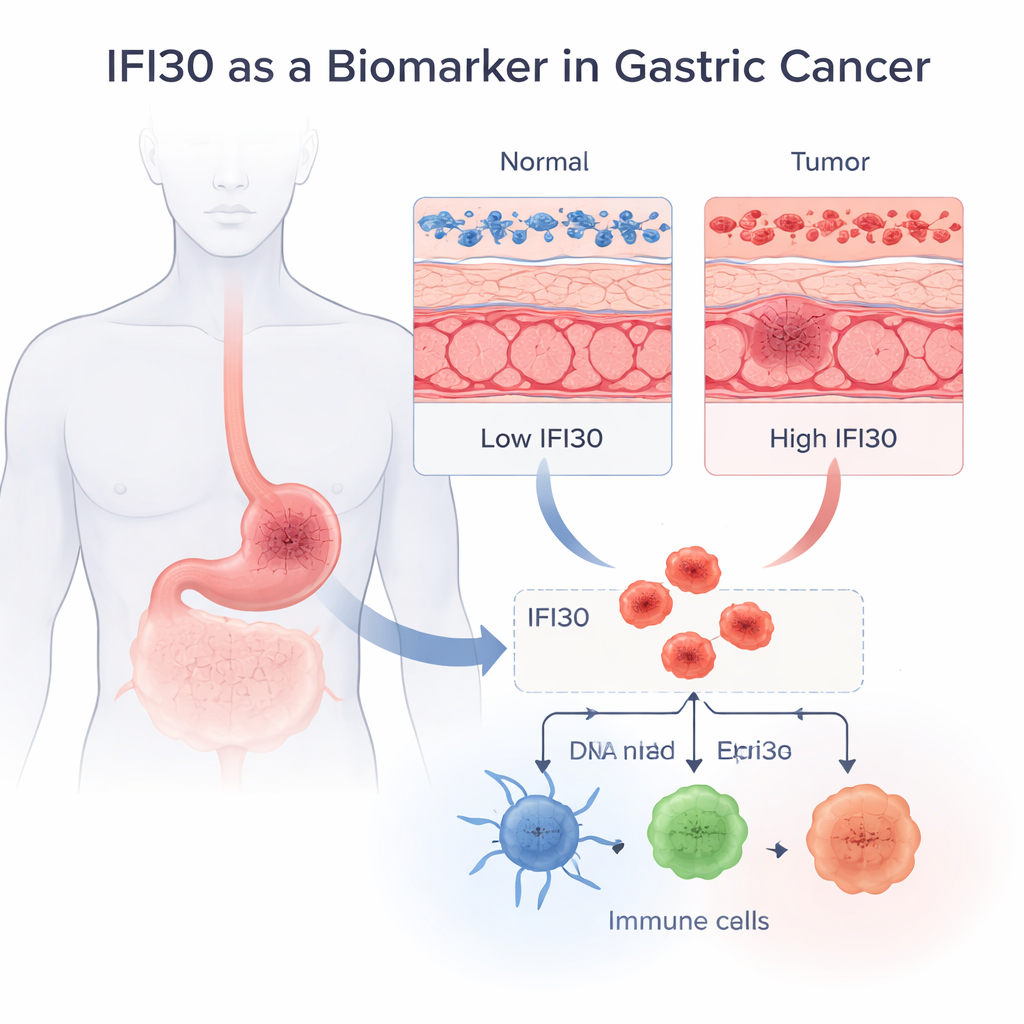
Een verborgen signaal in maagtumoren
Het team begon met een eenvoudige vraag: komt IFI30 anders tot expressie in gezond weefsel vergeleken met kankergezwel in de maag? Met behulp van grote openbare datasets waarin genactiviteit van duizenden monsters is samengebracht, vonden zij dat IFI30 consequent veel hoger is bij maagadenocarcinoom—de meest voorkomende vorm van maagkanker—dan in het normale maagslijmvlies. Dit bleek waar te zijn in meerdere onafhankelijke patiëntgroepen en zowel op RNA- als eiwitniveau. Toen de auteurs onderzochten hoe goed IFI30 op zichzelf tumorweefsel van gezond weefsel kon onderscheiden, was de prestatie opvallend: een diagnostische nauwkeurigheid (AUC) van 0,92, wat voor een enkele marker als uitstekend geldt. Microscopische beelden plaatsten IFI30 bovendien binnen het intracellulaire recycle-systeem, waar antigenen worden verwerkt voor immuunherkenning.
DNA-veranderingen die IFI30 opschroeven
Vervolgens onderzochten de onderzoekers waarom IFI30 in deze tumoren zo sterk verhoogd is. Door de genomen van kankers uit The Cancer Genome Atlas te scannen, vonden zij dat extra kopieën van het IFI30-gen—bekend als copy-number amplificaties—de belangrijkste aanstichter van de overexpressie waren. Tumoren met versterking van IFI30 vertoonden vaak grotere algehele genoominstabiliteit en droegen regelmatig bekende kankermutaties zoals TP53 en PIK3CA. Naarmate het aantal kopieën van IFI30 toenam, stegen ook de RNA-niveaus, wat wijst op een rechtstreeks verband tussen structurele DNA-veranderingen en de verhoogde productie van dit eiwit. Dit schetst IFI30 niet als een passieve omstander, maar als onderdeel van een breder patroon van agressieve tumorbiologie.
Immuuncrosstalk rond de tumor
Aangezien IFI30 betrokken is bij de verwerking van materiaal dat immuuncellen presenteren als "gezocht-affiches" aan T-cellen, onderzocht het team waar het precies in het tumor-micro-omgeving voorkomt. Single-cell sequencing, dat genexpressie in individuele cellen uitleest, toonde aan dat IFI30 vooral verrijkt is in dendritische cellen, macrofagen en CD8 T-cellen—sleutels spelers bij het opstarten en in stand houden van anti-tumorimmuniteit. Netwerkanalyses lieten dichte communicatie zien tussen IFI30-rijke immuuncellen en omliggende tumor- en ondersteunende cellen. Tumoren met hoge IFI30 vertoonden sterke activatie van paden die samenhangen met antigeenpresentatie, ontstekingssignalen en communicatie-moleculen die immuuncellen aantrekken en organiseren. Tegelijkertijd toonden deze tumoren kenmerken van invasie en stress, zoals versnelde celcyclus, weefselremodellering en aanpassing aan lage zuurstof, wat IFI30’s rol op de kruising van aanval en verdediging binnen de kanker benadrukt.
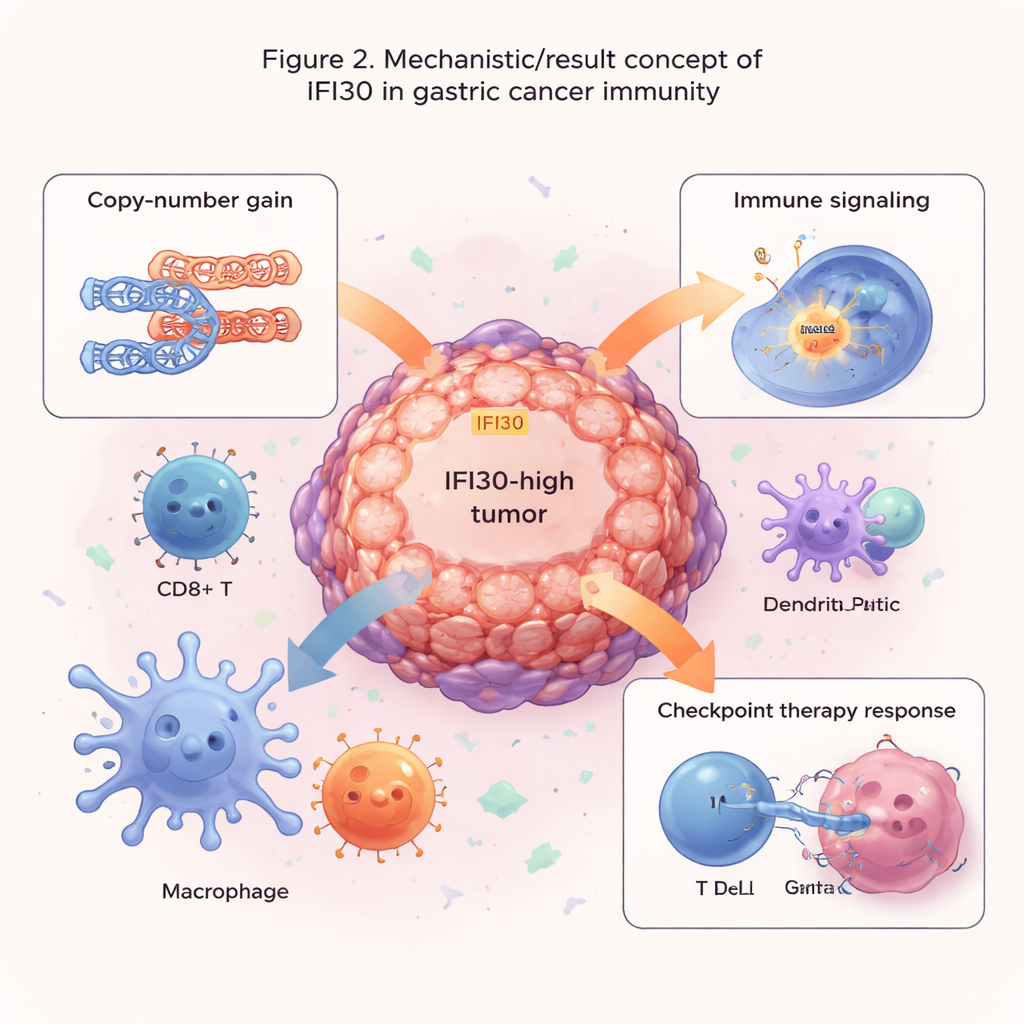
Aanwijzingen voor medicijnkeuze en immunotherapie
De auteurs vroegen zich vervolgens af of IFI30 kon helpen voorspellen hoe tumoren op behandeling reageren. Door IFI30-niveaus te koppelen aan grote datasets over medicijnrespons, vonden zij dat IFI30-rijke tumoren vaak resistent zijn tegen bepaalde middelen die de celdeling of een veelgebruikt groeipad (MAPK) remmen, maar juist gevoeliger lijken voor geneesmiddelen die EGFR en PI3K/AKT-signaalroutes blokkeren. Opmerkelijk genoeg correleerden IFI30-niveaus sterk met PD-L1, een belangrijke rem op T-cellen die wordt aangestuurd door hedendaagse checkpointremmers. In meerdere immunotherapie-studies waren patiënten met hogere IFI30-expressie in hun tumoren vaker ontvankelijk voor checkpointblokkade dan patiënten met lage niveaus. Een op IFI30 gebaseerde score overtrof gevestigde maatstaven zoals tumor mutatiebelasting en PD-L1 alleen, en kwam vooral veel voor in tumoren met hoge microsatellietinstabiliteit, een subgroep die al bekendstaat als beter reagerend op immunotherapie.
Van laboratoriumbank naar mogelijk nieuw doelwit
Om te testen of IFI30 slechts een marker is of ook bijdraagt aan tumorgroei, verlaagde het team de niveaus ervan in maagkankercellijnen met genetische middelen. Toen IFI30 werd onderdrukt, groeiden kankercellen langzamer, wat wijst op een directe rol bij het in stand houden van tumorproliferatie. Geleverd bij elkaar suggereren de gegevens dat IFI30 zowel een afspiegeling is van immuunactiviteit als een bijdrager aan kwaadaardig gedrag. Voor patiënten betekent dit dat een eenvoudige meting van IFI30 op termijn artsen zou kunnen helpen maagkanker betrouwbaarder op te sporen, voorspellen wie baat kan hebben bij bepaalde gerichte middelen of immunotherapieën, en mogelijk nieuwe behandelingen sturen die IFI30’s tumorbevorderende werking direct of indirect blokkeren.
Bronvermelding: Liu, Q., Yuan, W., Zhaowang, R. et al. Copy-number amplification drives IFI30 overexpression and coordinated immune activation, identifying a novel diagnostic and therapeutic target in gastric adenocarcinoma. Sci Rep 16, 6945 (2026). https://doi.org/10.1038/s41598-026-37574-z
Trefwoorden: maagkanker, IFI30, biomarker, tumorimmuniteit, immunotherapie