Clear Sky Science · nl
Computationale analyse van X2CaZnH6 (X = K, Rb en Cs) hydrides voor waterstofopslag
Waterstof in een doos
Waterstof wordt vaak geprezen als schone brandstof van de toekomst, maar het veilig en compact opslaan ervan blijft een grote uitdaging. Deze studie onderzoekt een nieuwe familie kristallijne materialen die waterstof in hun atomaire raamwerk kunnen vasthouden, vergelijkbaar met water in een spons. Door deze verbindingen eerst op de computer te ontwerpen voordat iemand ze in het laboratorium maakt, tonen de auteurs aan hoe ze als vaste brandstoffen voor toekomstige waterstofgedreven technologieën zouden kunnen dienen.
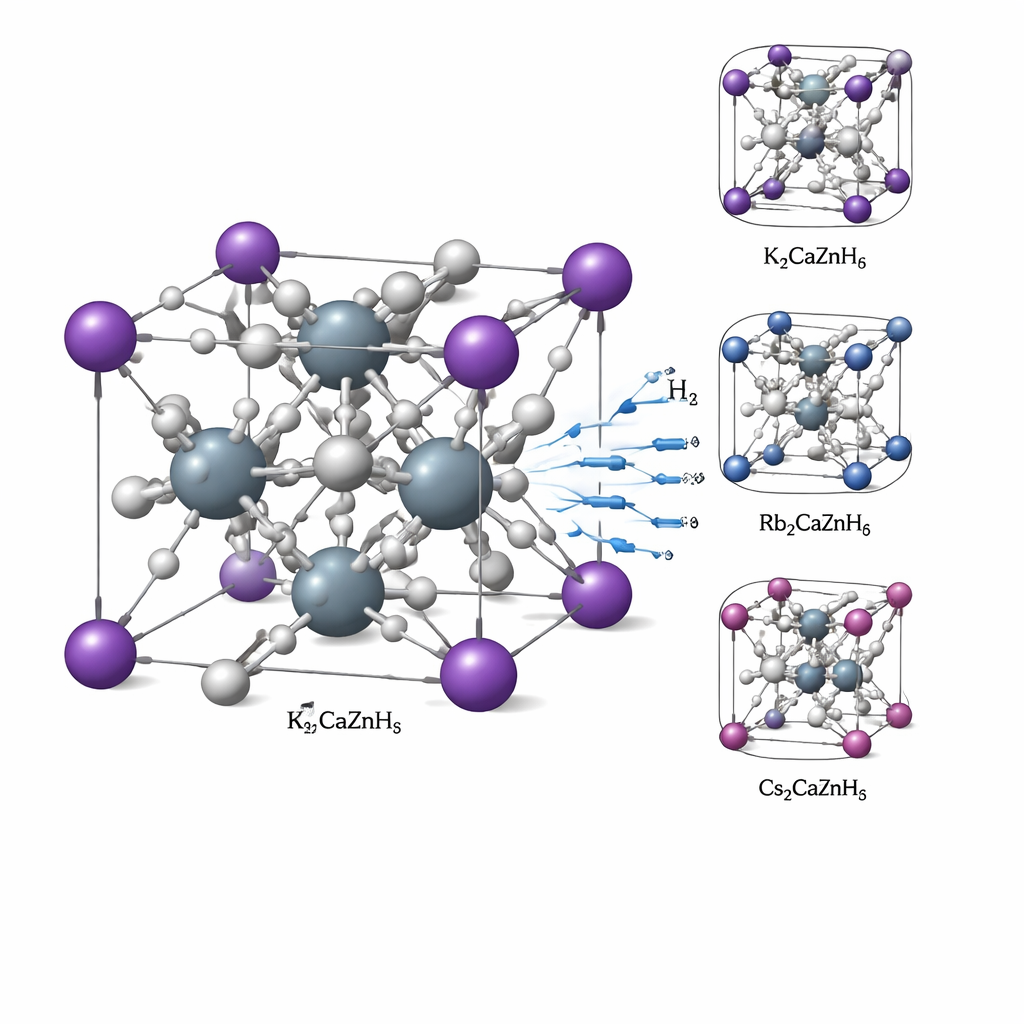
Een kristal opgebouwd als een 3D-rooster
De onderzochte materialen worden dubbele perovskiet-hydrides genoemd en hebben de formule X2CaZnH6, waarbij X kalium (K), rubidium (Rb) of cesium (Cs) kan zijn. Alle drie vormen een eenvoudig kubusachtig netwerk waarin zware atomen op vaste posities zitten en waterstofatomen ruimtes rondom innemen. Met kwantummechanische berekeningen bevestigen de auteurs dat deze kristallen structureel stabiel zijn: de atomen passen qua maat bij elkaar, de totale energie van het materiaal is laag genoeg dat het natuurlijk zou moeten vormen, en de trillingen van de atomen wijzen niet op verborgen instabiliteiten. Mechanische tests in silico tonen aan dat de kristallen stijf maar niet te bros zijn, een balans die hen helpt hun vorm te behouden terwijl kleine herschikkingen mogelijk blijven wanneer waterstof wordt opgenomen of vrijgegeven.
Hoeveel waterstof kunnen ze vasthouden?
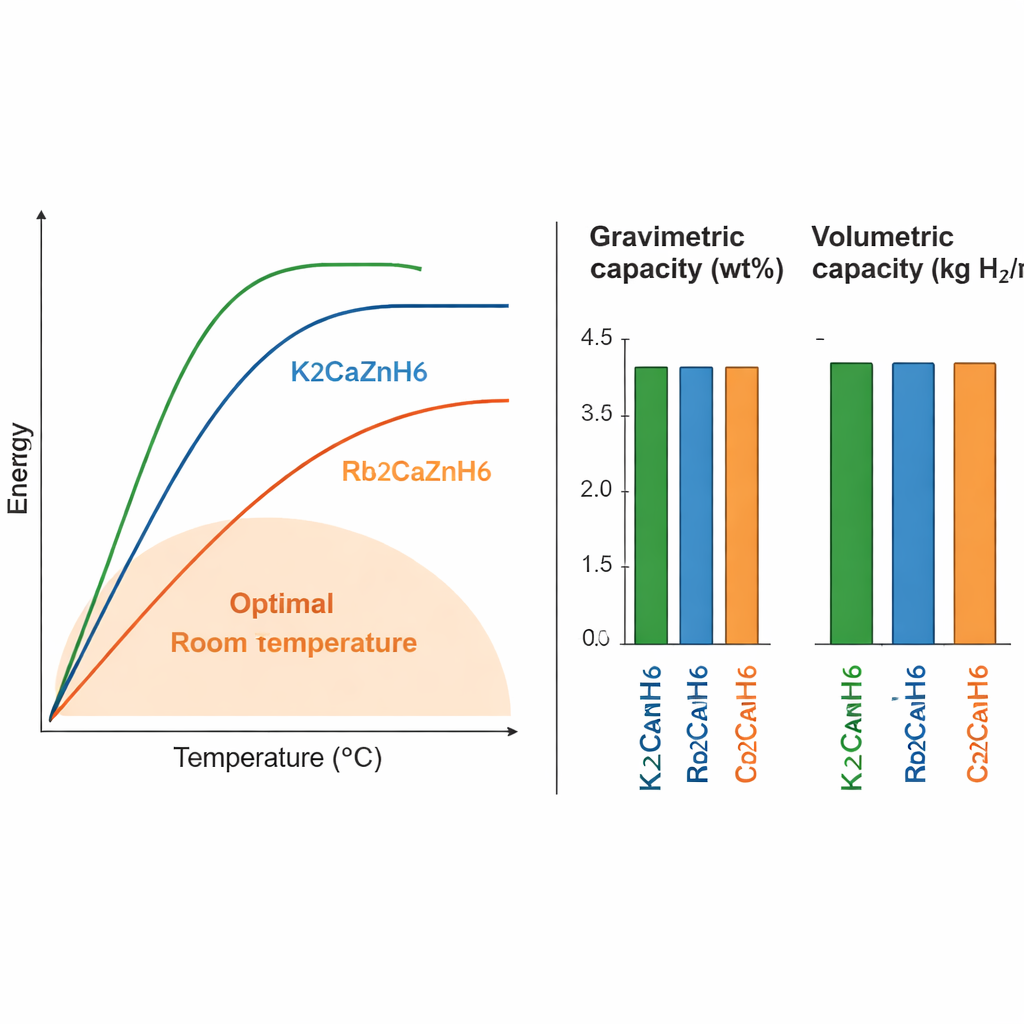
Voor elk opslagmateriaal zijn twee belangrijke grootheden hoeveel waterstof het kan bevatten naar gewicht (gravimetrische capaciteit) en naar volume (volumetrische capaciteit), en bij welke temperatuur waterstof vrijkomt. De drie bestudeerde verbindingen slaan tussen ongeveer 1,6 en 3,2% van hun gewicht als waterstof op, en ongeveer 15 tot 18 kilogram waterstof per kubieke meter materiaal. De kaliumvariant, K2CaZnH6, bevat de meeste waterstof maar vereist hogere temperaturen (ongeveer 658 K, of 385 °C) om deze vrij te geven. De cesiumvariant slaat iets minder waterstof op en vergt eveneens vrij hoge temperaturen. De rubidiumverbinding, Rb2CaZnH6, springt eruit: zij geeft waterstof vrij bij ongeveer 385 K (ongeveer 110 °C), een bereik dat veel dichter bij wat praktisch is voor echte apparaten ligt, terwijl de opslagdichtheid nog steeds respectabel blijft.
Waarom de atomen en elektronen ertoe doen
Om te begrijpen waarom deze materialen zich zo gedragen, onderzoeken de auteurs hoe elektronen tussen atomen worden gedeeld en hoe dit bindingen beïnvloedt. In alle drie de verbindingen fungeren kalium, rubidium of cesium als elektrondonoren, terwijl zink, calcium en waterstof elektronen aantrekken. De waterstofatomen nemen een gedeeltelijke negatieve lading op, en hun bindingen met calcium en zink zijn grotendeels ionisch met een vleugje covalente karakter. Dit soort binding houdt waterstof doorgaans sterk genoeg vast zodat het niet gemakkelijk ontsnapt, maar zwak genoeg dat verwarming het kan vrijgeven wanneer dat nodig is. Belangrijk is dat waterstofatomen binnen het kristal geen sterke H–H-bindingen vormen, wat betekent dat waterstof als losse atomen wordt opgeslagen in plaats van als vooraf gevormde moleculen — gunstig voor gecontroleerde vrijgave.
Licht, elektriciteit en sterkte
Deze kristallen zijn ook halfgeleiders, met een bescheiden energieruimte tussen gevulde en lege elektronische toestanden. Dat betekent dat ze met licht over een breed kleurenspectrum kunnen interageren, vooral in het zichtbare en ultraviolet. De berekeningen tonen sterke lichtabsorptie en aanzienlijke optische geleidbaarheid, waardoor de mogelijkheid ontstaat dat licht kan helpen om waterstof vrij te maken — een vorm van zonondersteunde opslag. Tegelijk voldoen de materialen aan standaardcriteria voor mechanische stabiliteit: ze weerstaan compressie, schuif- en breukbelastingen binnen redelijke grenzen, en hun atomaire trillingen blijven bij kamertemperatuur goed gedraagt in computergesimuleerde verhittingstests. Samen wijzen deze eigenschappen op een robuust raamwerk dat herhaaldelijk laden en lossen van waterstof kan doorstaan.
Wat dit betekent voor toekomstige energiesystemen
In alledaagse termen identificeert de studie drie nieuwe "waterstofspons"-materialen die stabiel, redelijk sterk zijn en waterstof compact in een vaste stof kunnen opslaan. Hoewel hun waterstofgehalte naar gewicht nog niet voldoet aan de meest ambitieuze doelen, is hun volumetrische opslag veelbelovend, en de rubidiumgebaseerde verbinding werkt in het bijzonder bij temperaturen die compatibel zijn met veel praktische systemen. Omdat hun gedrag eenvoudig te tunen is door één alkalimetalen element voor een ander te vervangen, bieden deze dubbele perovskiet-hydrides een flexibel platform voor het ontwerpen van betere vaste waterstofbrandstoffen en mogelijk voor het combineren van opslag met lichtgestuurde controle in toekomstige schone-energietechnologieën.
Bronvermelding: Al-Zoubi, N., Almahmoud, A., Almahmoud, A. et al. Computational analysis of X2CaZnH6 (X = K, Rb and Cs) hydrides for hydrogen storage. Sci Rep 16, 6889 (2026). https://doi.org/10.1038/s41598-026-37564-1
Trefwoorden: waterstofopslag, metalen hydrides, dubbele perovskiet, vaste-stof energie, schone brandstoffen