Clear Sky Science · nl
Prevalentie en genotypering van Pseudomonas aeruginosa uit voedsel- en menselijke bronnen
Waarom een veelvoorkomende kiem ertoe doet in het dagelijks leven
Pseudomonas aeruginosa is een mondvol om uit te spreken, maar het is een bacterie die geruisloos van water en rauwe voedingsmiddelen naar ziekenhuizen en mensen kan reizen en soms ernstige, moeilijk te behandelen infecties veroorzaakt. Deze studie, uitgevoerd in een Egyptische stad, bracht in kaart waar deze bacterie voorkomt in alledaagse items zoals kraanwater, vis, vlees en melk, en in etterende wondinfecties bij patiënten. Er werd ook onderzocht hoe weerbaar de bacterie is tegen antibiotica en of zij genetische “instrumenten” draagt die haar gevaarlijker maken. De bevindingen verklaren waarom voedselhygiëne, schoon water en zorgvuldig antibioticagebruik samenhangen met de bescherming van de volksgezondheid.
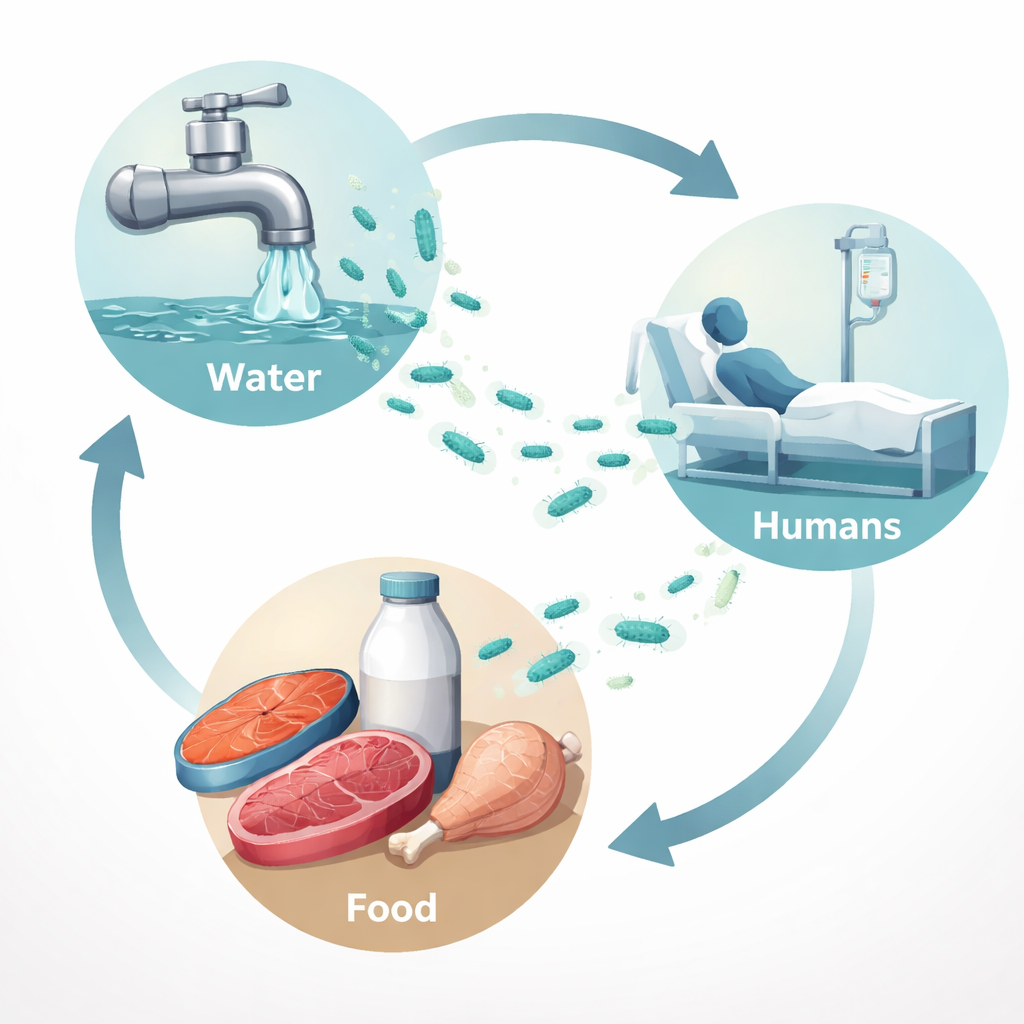
De kiem volgen van markt tot ziekenhuis
De onderzoekers verzamelden 350 monsters uit de omgeving van Sadat City in het gouvernoraat Menoufia, Egypte. Deze omvatten menselijke pus van geïnfecteerde wonden, kraanwater, visswabs, kippenvlees, gehakt, rauwe melk en oppervlakken in ziekenhuizen. Ze zochten specifiek naar P. aeruginosa. In totaal vonden ze de bacterie in ongeveer één op de zeven monsters. Ze kwam het vaakst voor in menselijke wondmonsters (ongeveer één op de vier), maar ook in kraanwater, vis en rauwe melk, en in mindere mate in kip en gehakt. Interessant was dat geen van de afgenomen ziekenhuisoppervlakken positief testte, wat suggereert dat in deze situatie de grotere dreiging mogelijk van voedsel en water is die het ziekenhuis binnenkomen, in plaats van van besmette aanrechten en apparatuur.
Hoe gevaarlijk zijn deze bacteriën?
De aanwezigheid van de kiem is slechts een deel van het verhaal; hoe ze zich gedraagt is even belangrijk. Het team testte elk bacterie-isolaat met standaard laboratoriummethoden om te zien of het een kleverige beschermlaag kon vormen, een biofilm genoemd. Ongeveer een derde van de isolaten deed dat, waarbij sommige sterke, dikke lagen vormden. Biofilms maken bacteriën veel moeilijker te doden omdat ze cellen beschermen tegen reinigingsmiddelen en antibiotica. Genetische tests op de biofilm-vormende stammen toonden aan dat ze meerdere ‘virulentie’-genen droegen, die eiwitten coderen die weefsel beschadigen of de bacterie helpen zich aan oppervlakken vast te hechten en het immuunsysteem te ontwijken. Simpel gezegd: veel van de gevonden stammen waren niet alleen aanwezig — ze waren goed uitgerust om ziekte te veroorzaken.
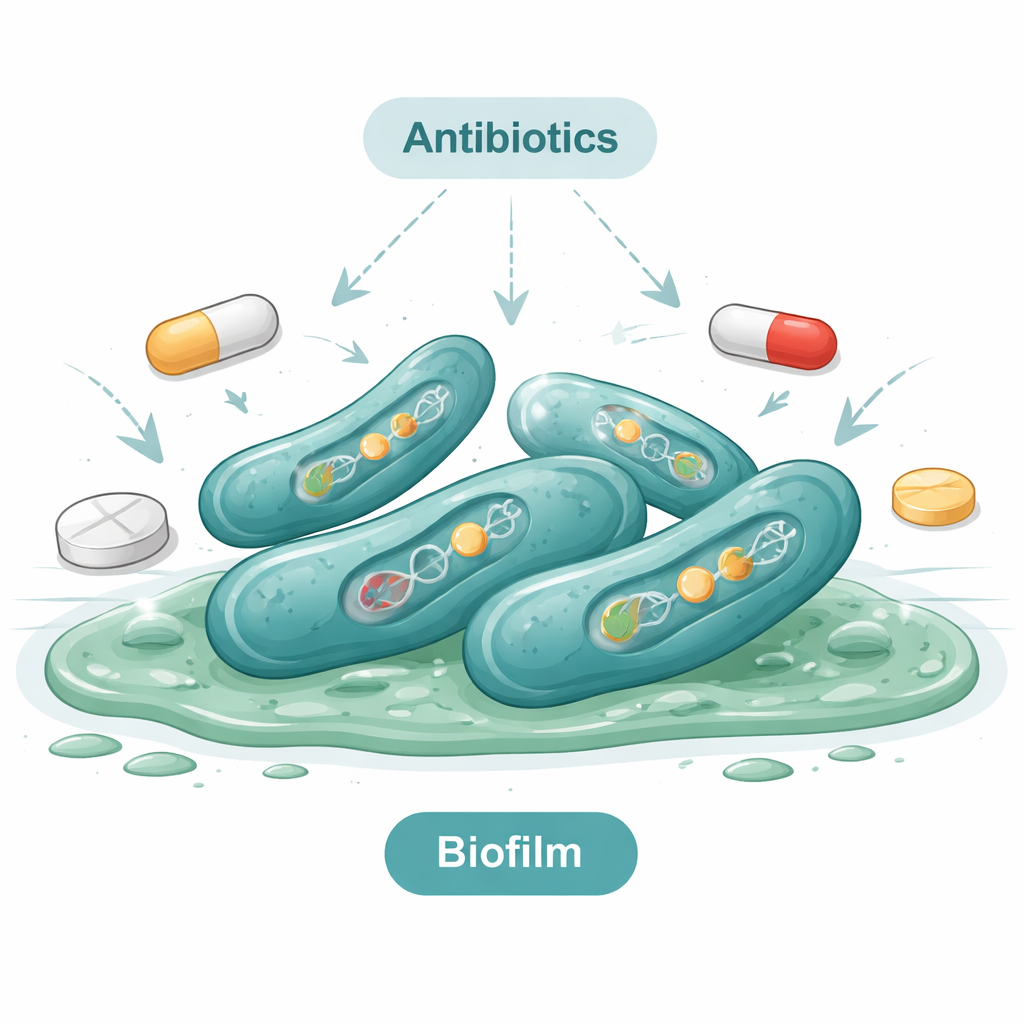
Antibiotica die falen — en enkele die nog werken
De studie stelde vervolgens een prangende vraag: welke antibiotica werken nog tegen deze stammen? Toen de onderzoekers 50 isolaten blootstelden aan 16 verschillende middelen, ontdekten ze dat veel gangbare antibiotica bijna nutteloos waren. Alle isolaten waren resistent tegen amoxicilline, en vrijwel alle isolaten waren resistent tegen erytromycine en verschillende andere oudere middelen. De meeste lieten zich ook niet beïnvloeden door colistine, een middel dat vaak als laatste redmiddel wordt bewaard. Positief was dat een handvol antibiotica — waaronder imipenem en enkele verwante middelen — nog steeds tegen veel isolaten werkte. Desondanks was meer dan vier op de vijf stammen resistent tegen meerdere typen geneesmiddelen tegelijk, een situatie die bekendstaat als multiresistentie. Genetische tests bevestigden dit: de bacteriën droegen resistentiegenen die hen helpen antibiotica inactief te maken of uit hun cellen te pompen.
Voedsel, water en menselijke infecties aan elkaar koppelen
Om te onderzoeken hoe verwant de stammen uit verschillende bronnen waren, gebruikte het team een DNA-‘vingerafdruk’-methode genaamd ERIC‑PCR op een subset van klinische isolaten. Deze techniek groepeert bacteriën op basis van herhaalde patronen in hun genoom. De analyse splitste de stammen in clusters die monsters van zowel mensen als voedingsmiddelen zoals vis, melk, kip en gehakt bevatten. Dit patroon suggereert dat voedsel en water als tussenstations kunnen fungeren, waardoor vergelijkbare stammen van P. aeruginosa zich tussen de omgeving en menselijke patiënten kunnen verplaatsen. In praktische termen kan de bacterie die in een stuk rauwe vis op de markt wordt gedetecteerd, nauw verwant zijn aan degene die een wondinfectie in een nabijgelegen ziekenhuis veroorzaakt.
Wat dit betekent voor de gezondheid van alledag
Voor leken is de boodschap helder: een veelvoorkomende omgevingsbacterie vindt haar weg van water en dierlijke voedingsmiddelen naar mensen, en veel stammen zijn bewapend met genen die hen taai, hardnekkig en schadelijk maken. Omdat zoveel isolaten resistent zijn tegen meerdere antibiotica, wordt de behandeling van infecties ingewikkelder, duurder en riskanter. De auteurs pleiten voor betere hygiëne in voedselproductie en -verwerking, veiligere watersystemen en zorgvuldiger antibioticagebruik bij zowel mensen als dieren om de verspreiding van deze hardnekkige stammen te vertragen. Ze roepen ook op tot voortdurende surveillance en gedetailleerdere genetische studies om in kaart te brengen hoe P. aeruginosa door de voedselketen en ziekenhuizen reist, zodat toekomstige uitbraken beter voorspeld en voorkomen kunnen worden.
Bronvermelding: Mousa, W.S., Abdeen, E.E., El-Gendy, H.F. et al. Prevalence and genotyping of Pseudomonas aeruginosa from food and human sources. Sci Rep 16, 7179 (2026). https://doi.org/10.1038/s41598-026-37559-y
Trefwoorden: Pseudomonas aeruginosa, voedselovergedragen bacteriën, antibioticaresistentie, biofilm, waterverontreiniging