Clear Sky Science · nl
Hybride deep learning nieuw raamwerk voor de classificatie van de ziekte van Parkinson
Waarom dit van belang is voor patiënten en families
De ziekte van Parkinson begint vaak met subtiele veranderingen — langzamere bewegingen, een zachtere stem of een lichte tremor — die gemakkelijk kunnen worden aangezien voor normaal ouder worden. Tegen de tijd dat de diagnose zeker is, is er vaak al veel schade in de hersenen aangericht. Deze studie presenteert een computergebaseerde methode die hersenscans leest om de ziekte van Parkinson met zeer hoge nauwkeurigheid te signaleren, zelfs wanneer de tekenen nog gering zijn. Als dergelijke hulpmiddelen betrouwbaar blijken en breed worden ingezet, kunnen ze artsen helpen eerder te diagnosticeren, eerder te behandelen en patiënten en hun families meer tijd te geven om te plannen.
In de hersenen kijken met slimme scans
De onderzoekers richtten zich op magnetische resonantiebeeldvorming (MRI), een scan die al veel gebruikt wordt in ziekenhuizen en geen straling inhoudt. Zij gebruikten een grote openbare verzameling hersenbeelden van de Parkinson’s Progression Markers Initiative, met scans van mensen met de ziekte van Parkinson en van gezonde vrijwilligers. In plaats van de gehele 3D-scan in één keer te analyseren, werkten ze met plak-voor-plak beelden door de hersenen, vooral het middenbrein waar cellen die dopamine produceren te vinden zijn. Deze cellen zijn cruciaal voor vloeiende bewegingen en hun verlies is kenmerkend voor de ziekte van Parkinson. Om vage structuren voor een computer beter zichtbaar te maken, werden de beelden eerst zorgvuldig aangepast om helderheid te standaardiseren en het contrast in sleutelgebieden te verbeteren.
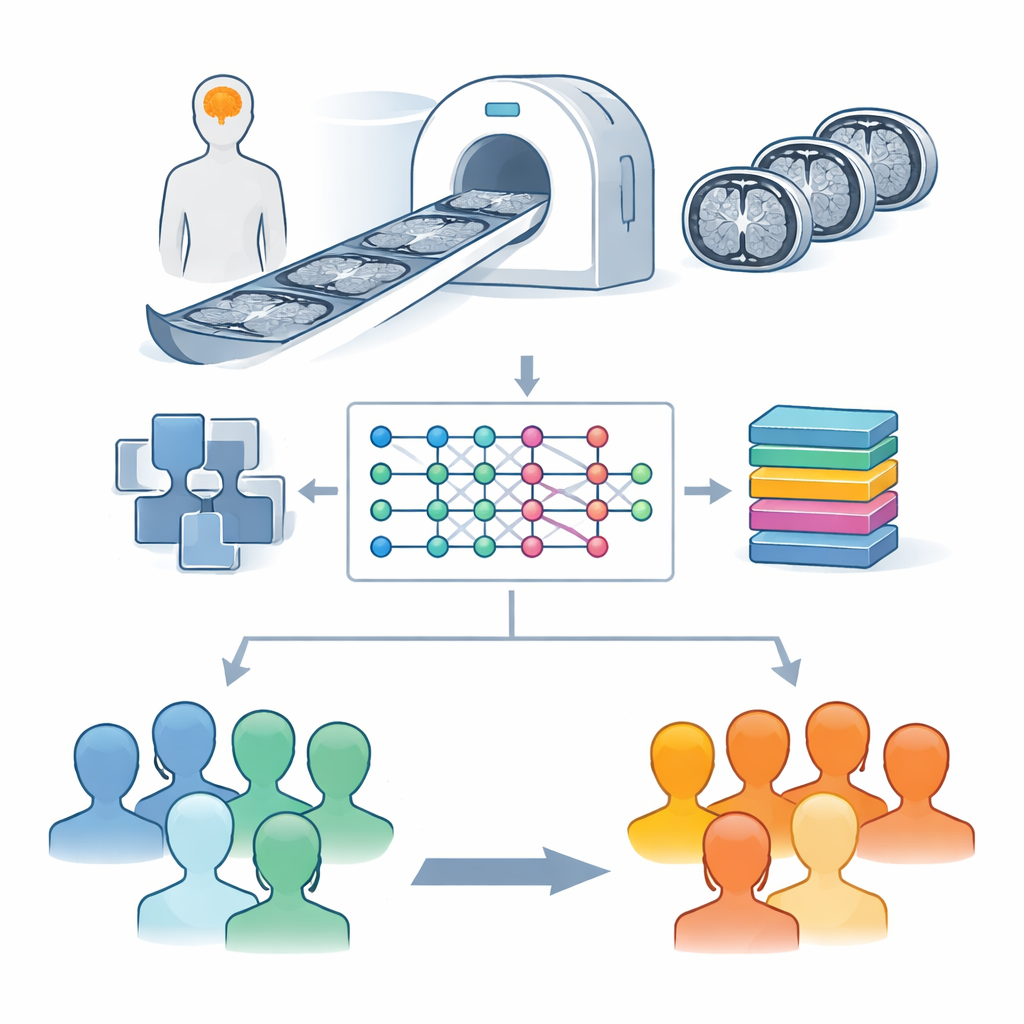
Een hybride model leren patronen te herkennen
Het hart van de studie is een hybride systeem dat twee krachtige ideeën uit de moderne informatica combineert. De eerste is een deep learning-netwerk genaamd EfficientNetB0, oorspronkelijk ontworpen voor algemene beeldherkenningstaken. Hier fungeert het als een sterk getraind oog dat elke hersenplak scant om subtiele patronen van vorm en textuur te extraheren die gezonde hersenen scheiden van hersenen die door Parkinson zijn aangetast. De tweede is een beslismethode bekend als XGBoost, die uitblinkt in het trekken van scherpe grenzen tussen categorieën zodra zij informatieve kenmerken krijgt. In eenvoudige bewoordingen distilleert EfficientNetB0 elke MRI-plak tot een compacte handtekening, en gebruikt XGBoost deze handtekeningen om te beslissen of de scan bij een gezond persoon hoort of bij iemand met de ziekte van Parkinson, en of de beelden van een bepaald MRI-type zijn.
Omgaan met beperkte en ongelijk verdeelde data
Een van de grootste praktische problemen in medische AI is dat gegevens vaak zowel schaars als onevenwichtig zijn: er kunnen veel meer scans van patiënten zijn dan van gezonde vrijwilligers, of omgekeerd. Hier begon het team met scans van 77 gezonde en 223 Parkinson-patiënten, een bescheiden aantal voor deep learning. Om te voorkomen dat het systeem scheve lessen zou leren, breidden ze de beeldset op gecontroleerde wijze uit. Elke oorspronkelijke hersenplak werd gedraaid of gespiegeld om de kleine verschillen in hoofdpositie tijdens echte scans na te bootsen. Zij pasten ook een contrastverbeteringstechniek toe genaamd CLAHE, die fijne details opheldert zonder ruis te overdrijven. Deze zorgvuldige "uitbreiding" van de dataset leverde meer dan 26.000 beelden op, waardoor het model genoeg variatie had om robuuste patronen te leren en het risico van overfitting aan eigenaardigheden in de oorspronkelijke scans werd verminderd.
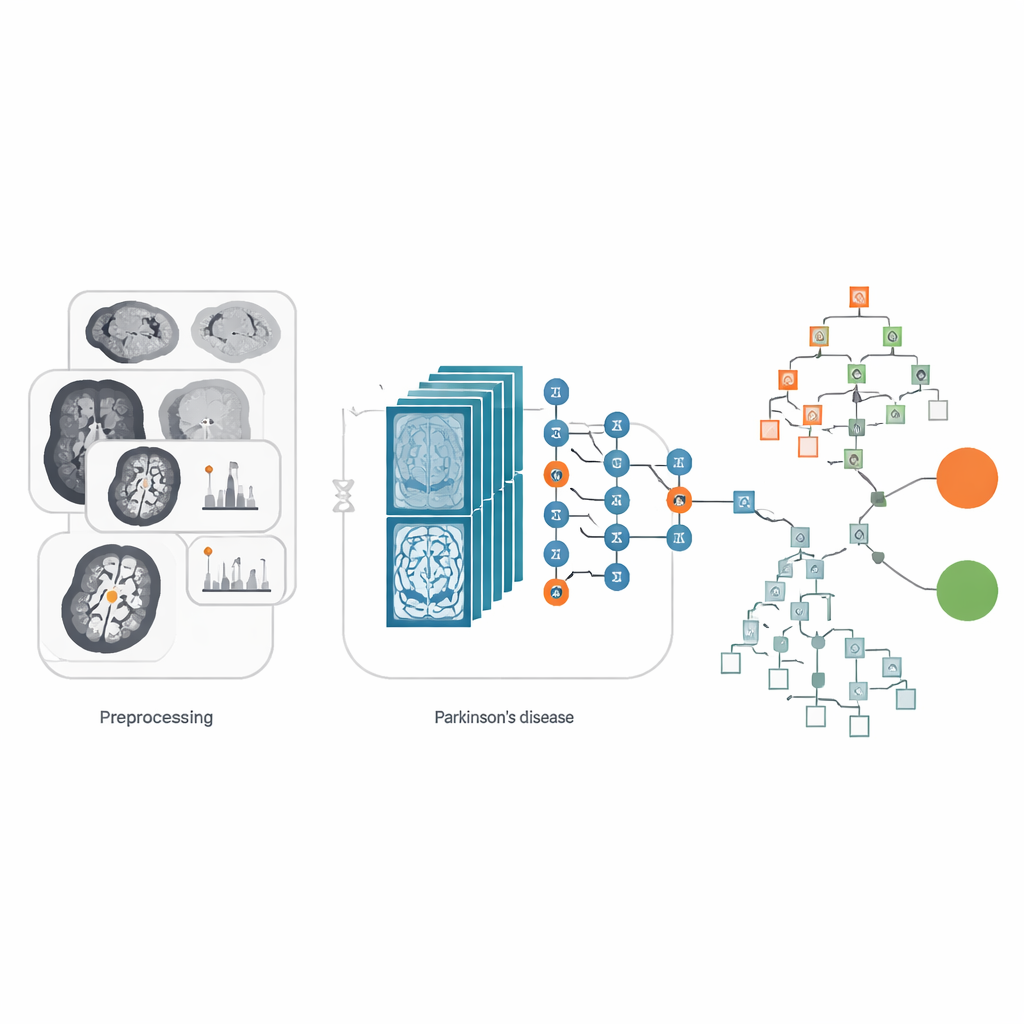
Hoe goed presteert het systeem?
Om de betrouwbaarheid te meten vergeleken de onderzoekers verschillende versies van hun aanpak. Ze testten drie populaire beeldnetwerken — VGG16, ResNet50 en EfficientNetB0 — in drie modi: ongewijzigd, fijn afgesteld en gecombineerd met de XGBoost-beslisfase. Over deze opties heen deden de hybride opstellingen het consequent het beste. De winnende configuratie, EfficientNetB0 plus XGBoost, classificeerde scans in de testset correct in 99,02 procent van de gevallen. Het behandelde alle vier de categorieën goed: gezond en Parkinson, elk met en zonder een bepaalde MRI-instelling bekend als FLAIR. Maatstaven die focussen op gemiste gevallen en foutieve alarmen, zoals recall en F1-score, waren eveneens zeer hoog, wat suggereert dat het hulpmiddel niet simpelweg het ene type fout tegen het andere wegruilt. Belangrijk is dat het model efficiënt bleef qua rekentijd, waardoor het realistischer wordt voor gebruik in drukke klinische omgevingen.
Wat dit in de kliniek zou kunnen betekenen
Hoewel geen enkel computersysteem een ervaren neuroloog kan vervangen, laat dit werk zien dat een zorgvuldig ontworpen hybride model kan fungeren als een krachtige assistent. Door routinematige MRI-beelden snel te scannen op subtiele tekenen van de ziekte van Parkinson, zouden dergelijke hulpmiddelen patiënten met verhoogd risico kunnen signaleren voor nauwkeuriger vervolgonderzoek lang voordat symptomen duidelijk worden. De auteurs wijzen erop dat hun aanpak nog getest moet worden op grotere en meer diverse patiëntgroepen, en uiteindelijk gecombineerd met andere informatie zoals bewegingsonderzoeken of bloedmarkers. Toch suggereren hun resultaten dat slimme software die is gebouwd op bestaande ziekenhuisscans een snelle, goedkope en breed inzetbare bondgenoot zou kunnen worden bij de vroege opsporing van de ziekte van Parkinson.
Bronvermelding: Desai, S., Vora, M., Shah, S. et al. Hybrid deep learning novel framework for classification of parkinson’s disease. Sci Rep 16, 9143 (2026). https://doi.org/10.1038/s41598-026-37553-4
Trefwoorden: Ziekte van Parkinson, hersenen MRI, deep learning, medische beeldvorming, vroege diagnose