Clear Sky Science · nl
Een split-biotine-ligase-aanpak onthult eiwitten geassocieerd met oligomerisch alpha-synucleïne tijdens aggregatie
Waarom samengeklonterde eiwitten in de hersenen ertoe doen
Bij de ziekte van Parkinson en aanverwante aandoeningen kan een normaal nuttig herseneiwit, alpha‑synucleïne, samenklitten tot plakkerige afzettingen die bekendstaan als Lewy‑lichaampjes. Deze afzettingen verschijnen decennia vóór symptomen en zijn een kenmerk dat bij autopsie wordt gezien, maar we weten nog steeds niet welke andere eiwitten alpha‑synucleïne helpen verschuiven van een onschadelijke toestand naar gevaarlijke aggregaten. Deze studie gebruikt een slimme moleculaire "nabijheidstag" om in kaart te brengen welke eiwitten dicht bij alpha‑synucleïne zitten terwijl het verandert van losse moleculen naar kleine klompjes, en biedt nieuwe aanwijzingen over hoe de ziekte begint en welke routes mogelijk doelwit kunnen zijn om deze te vertragen of te voorkomen.
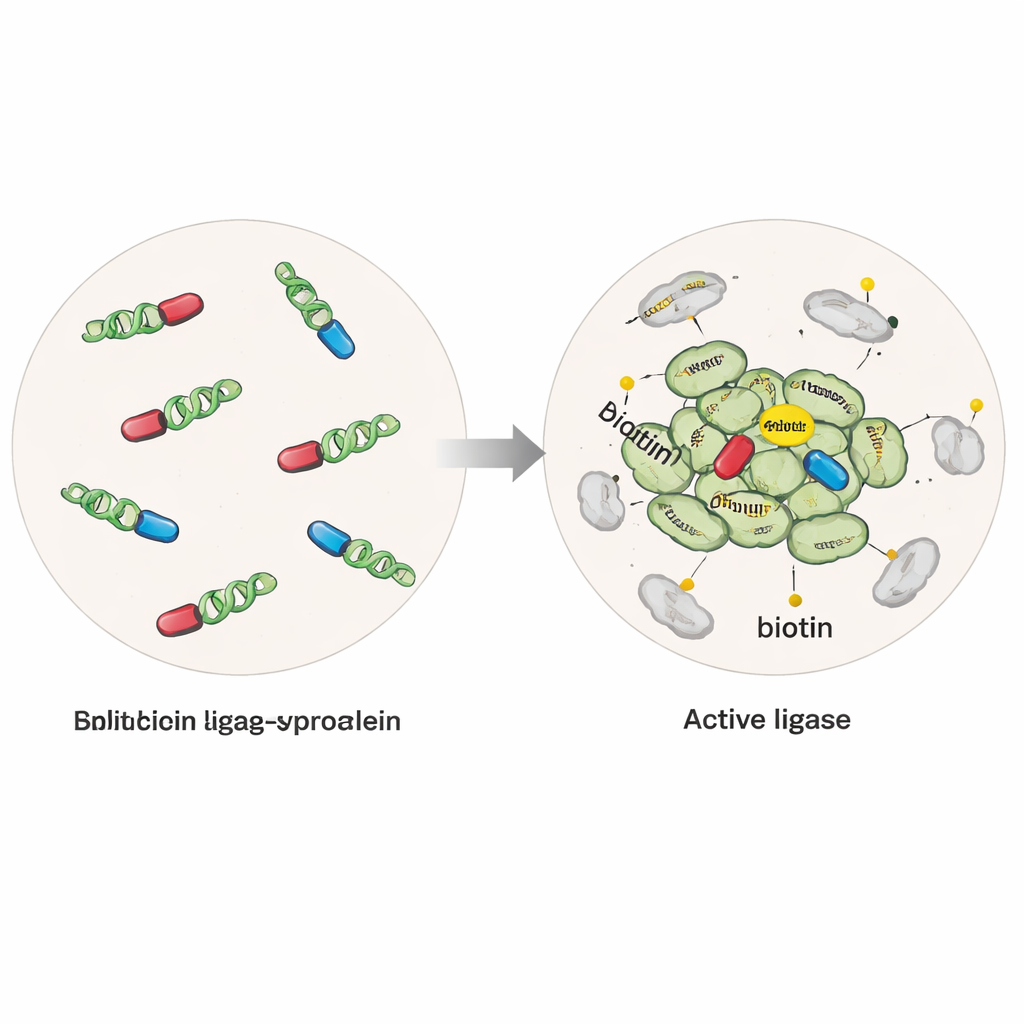
Een moleculair “label” dat buren verlicht
De onderzoekers hebben menselijke cellen zodanig gemodificeerd dat ze alpha‑synucleïne produceren dat is gefuseerd aan een gemodificeerde enzym dat een klein biotinetagje kan aanhechten op elk eiwit binnen een paar miljardsten van een meter. In één versie was het enzym intact en actief zodra alpha‑synucleïne aanwezig was, waardoor eiwitten nabij zowel losse moleculen als klompjes werden gevangen. In een tweede, selectieve "gesplitste" versie, werd het enzym in twee inactieve helften gedeeld, elk bevestigd aan een afzonderlijk alpha‑synucleïne‑molecuul. Alleen wanneer alpha‑synucleïne‑moleculen samenkwamen in multimeren of oligomeren, verenigden de helften zich tot een actief enzym, waardoor het labelen specifiek rond deze vroege aggregaten werd aangezet. Door zuivere alpha‑synucleïnefibrillen aan de cellen toe te voegen, kon het team ook ziekteachtige aggregatie opwekken en normale versus pathologische toestanden vergelijken.
Het in kaart brengen van nabije eiwitten
Nadat er tijd was gegeven voor het labelen, trokken de onderzoekers alle biotine-gelabelde eiwitten naar beneden en identificeerden ze met massaspectrometrie, een techniek die eiwitten met hoge precisie weegt en telt. Over alle condities vonden ze 1.277 verschillende eiwitten, en na zorgvuldige filtering beperkten ze dit tot 581 die waarschijnlijk echt dicht bij alpha‑synucleïne lagen. Door de intacte en gesplitste enzym‑systemen te vergelijken, konden ze eiwitten onderscheiden die hoofdzakelijk met losse moleculen geassocieerd zijn van diegenen die multimeren verkiezen. Ze vergeleken ook cellen met en zonder toegevoegde fibrillen om te zien hoe de lokale eiwitomgeving van alpha‑synucleïne verandert zodra aggregatie wordt geactiveerd.
Belangrijke cellulaire routes die in de klonten worden getrokken
De resulterende interactome‑schets wijst op verschillende belangrijke biologische thema’s. Onder normale omstandigheden zat multimerisch alpha‑synucleïne dicht bij veel membrraan‑transporteiwitten en eiwit‑modificerende enzymen — in overeenstemming met de voorgestelde rol bij het helpen van zenuwcellen om synaptische vesikels te beheren en de eiwitkwaliteit te bewaken. Verscheidene enzymen die fosfaatgroepen toevoegen, waaronder de kinasen PAK4, RIPK2 en MAP4K4, waren verrijkt nabij gezonde multimeren maar leken het contact te verliezen zodra aggregaten gevormd werden, wat suggereert dat verstoring van deze relaties ziektebevorderende vormen van het eiwit kan bevorderen. Het team detecteerde ook eiwitten die verbonden zijn met insuline‑achtige groeifactor‑signalisatie, wat klinische verbanden ondersteunt tussen insulineresistentie en de ziekte van Parkinson, en vond dat aggregatie eiwitten aantrekt die betrokken zijn bij het afvoeren van beschadigde eiwitten, zoals de 14‑3‑3 chaperonfamilie en specifieke componenten van cellulaire degradatieroutes.
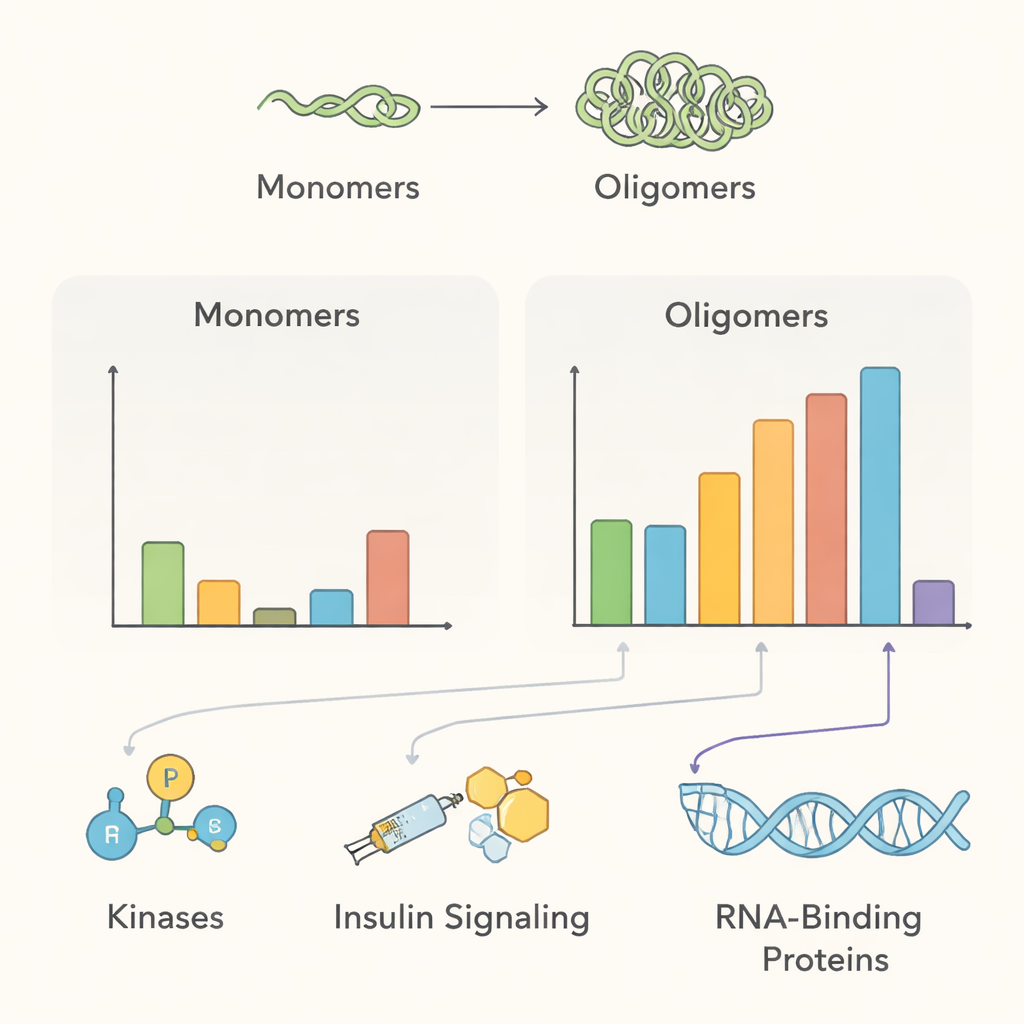
Onverwachte bruggen naar andere hersenaandoeningen
Naast de ziekte van Parkinson benadrukken de gegevens een verrassende verbinding met amyotrofische laterale sclerose (ALS) en frontotemporale dementie (FTD). Een RNA‑bindend eiwit genaamd FUS, dat in die aandoeningen verkeerde lokalisatie en aggregatie vertoont, verscheen nabij multimerisch alpha‑synucleïne onder zowel normale als aggregatiegestuurde omstandigheden. Andere RNA‑gerelateerde eiwitten veranderden ook hun nabijheid naarmate alpha‑synucleïne aggregeerde. Deze bevindingen wekken de mogelijkheid dat kleine alpha‑synucleïne‑assemblages RNA‑verwerkende eiwitten op de verkeerde plaats in cellen kunnen vasthouden, waardoor de biologie van Lewy‑lichaamziekten mogelijk wordt verbonden met die van ALS en FTD, hoewel directe fysieke interacties nog bevestigd moeten worden.
Wat dit betekent voor het begrijpen van de ziekte
Voor niet‑specialisten is de belangrijkste conclusie dat dit werk een vroege "contactlijst" oplevert van eiwitten die met alpha‑synucleïne meereizen terwijl het verandert van normale helper naar schadelijke klomp. De studie suggereert dat het verliezen van bepaalde beschermende relaties — zoals met specifieke kinasen of kwaliteitscontrole‑enzymen — net zo belangrijk kan zijn als het winnen van nieuwe toxische partners. Hoewel de experimenten in een vereenvoudigd cellair model zijn uitgevoerd en nog geen oorzaak‑en‑gevolg aantonen, wijzen ze op concrete kandidaten en routes voor vervolgonderzoek in neuronen en hersenweefsel. Op de lange termijn kan het in kaart brengen van deze veranderende eiwitbuurten strategieën sturen om beschermende interacties te herstellen, insulinegerelateerde signalering te ondersteunen of het vasthouden van RNA‑bindende eiwitten te voorkomen, en zo mogelijk het verstrijken van subtiele moleculaire veranderingen naar volwaardige Lewy‑lichaamziekten vertragen.
Bronvermelding: Fernandes, A.R., Owen, A.P., Faroqi, A.H. et al. A split biotin ligase approach reveals proteins associated with oligomeric alpha-synuclein during aggregation. Sci Rep 16, 7270 (2026). https://doi.org/10.1038/s41598-026-37551-6
Trefwoorden: alpha-synucleïne, Lewy-body-ziekte, eiwitaggregatie, proximity-proteomics, Ziekte van Parkinson